
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энергия молекул как сумма энергий различного вида движения
|
|
|
|
Зависимость теплоемкости от температуры для идеального газа
Зависимость теплоты реакции от температуры
 Реагенты Т1 Продукты Т1; DrHт1
Реагенты Т1 Продукты Т1; DrHт1

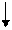 Σ׀νi׀ С рi Σ׀νj׀ С рj
Σ׀νi׀ С рi Σ׀νj׀ С рj
 Реагенты Т2 Продукты Т2; DrHт2
Реагенты Т2 Продукты Т2; DrHт2
Из изображенного цикла видно, что зависимость теплоты реакции от температуры связана с разностью теплот нагревания реагентов и продуктов реакции, которая связана с их теплоемкостью, которая в свою очередь зависит от температуры.
4.8.1.1. Связь Ср и Сv
Сv = 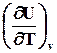 Сp =
Сp = 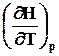
Связь Ср и Сv легко определяется для идеального газа:
dH = dU + p dV = dU + p R/p *dT = dU + RdT
(V = RT/p dV = R/p dT)
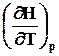 =
= 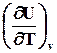 + R Þ Cp = C V + R ( 4.1 )
+ R Þ Cp = C V + R ( 4.1 )
R – работа расширения, которую совершает 1 моль идеального газа при нагревании на 1о
Внутренняя энергия – это сумма энергии частиц, составляющих термодинамическую систему. В идеальном газе отсутствует энергия взаимодействия молекул, поэтому внутренняя энергия определяется как сумма энергии химических связей в молекулах (eэлектронная) и кинетической составляющей движения молекул. Молекулы совершают различные виды движения, и приближенно общую энергию молекул можно представить в виде суммы энергии этих видов движения
e = eэлектр. + eкол. + eвращ. + eпост. = eе + ev + er + et. ( 4.2 )
Известно, что энергия микрочастиц квантована, т.е. может принимать только дискретные значения. Расстояние между этими уровнями различно для разных типов движения: Deе>>Dev>>Der > Det (Рис. 4.1).
Поступательная энергия молекул практически не квантуется, т.е. может изменяться непрерывно. Когда системе сообщается тепло, то энергия передается через хаотические соударения молекул. При столкновениях молекулы обмениваются квантами энергии, величина которых зависит от температуры – «тепловыми квантами»– kT, где k – постоянная Больцмана
k = R/N = 1,38*10-23Дж/К. ( 4.3 )


 e
e
Deе

 kT
kT

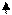

 Deν Der
Deν Der
 |
Рис. 4.1. Квантование уровней различных видов движения
При обычной температуре величина теплового кванта достаточна, чтобы изменить энергию поступательного и вращательного движения, а также наиболее слабых колебаний, но возбуждения сильных колебений, и тем более электронов не происходит
Dev>> kT > Der ( 4.4 )
Эта диаграмма позволяет примерно оценить теплоемкость простейших ве-ществ.
4.8.1.3. Одноатомный газ (He, Ar)
Молекулы одноатомного газа как точечные массы совершают только поступательное движение и имеют три степени свободы. По принципу равномерного распределения энергии по степеням свободы можно определить энергию молекул. На одну степень свободы приходится в среднем e = 1/2kT, а для 1-го моля Е = 1/2RT. Cледовательно, на 3 степени свободы одноатомной молекулы приходится
U = 3/2 RT. ( 4.5 )
Сv =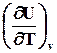 = 3/2 R ~ 3 кал/моль*K = 12,5 Дж/мольК,
= 3/2 R ~ 3 кал/моль*K = 12,5 Дж/мольК,
Cp = C V + R = 5 кал/мольК
Теплоемкость одноатомных газов практически не зависит от температуры.
Таблица 4.1.Теплоемкости Сv веществ при разной температуре (кал/мольК)
| Вещество | nt | nr | nv | 150 K | 300 К | 400 К |
| Ar | 2,92 | 2,98 | 2,98 | |||
| O2 | 4,98 | 5,03 | 6,22 | |||
| H2O | 6,04 | 7,57 |
4.8.1.4. Двухатомный газ – линейная молекула
Каждая молекула имеет 3N степеней свободы, где N –число атомов в молекуле. Для двухатомной молекулы общее число степеней свободы равно 6, из них 3 поступательных, 2 вращательных и 1 колебательная. Вращательных степеней свободы у линейных молекул только 2, так как при вращении вокруг линии связи, молекула не изменяет своего положения и это движение не может изменяться за счет передачи энергии от другой молекулы. При комнатной температуре возбуждаются только поступательное и вращательное движение – 5 степеней свободы
U = 5/2 RT.
Сv =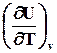 = 5/2 R ~ 5 кал/мольK = 20,8 дЖ/мольК,
= 5/2 R ~ 5 кал/мольK = 20,8 дЖ/мольК,
Cp = C V + R = 7 кал/мольК,
При повышении температуры начинает постепенно возбуждаться колеба-тельное движение, Сv → 6 кал/(моль К).
4.8.1.5. Многоатомные молекулы. Общее число степеней свободы равно 3N, из них 3 поступательных, 3 (или 2 для линейных молекул) враща-тельных и 3N - 6 (5) колебательных. Колебания тоже могут быть разными: валентные (жесткие) колебания, в которых происходит изменение длины связи, требуют большой энергии для возбуждения, и деформационные, в которых изменяются углы между связями. Последние более мягкие и требуют меньших квантов для возбуждения, и, следовательно, могут возбуждаться при более низкой температуре. В общем можно сделать такой вывод: чем сложнее молекула, тем сильнее зависимость ее теплоемкости от температуры. Нельзя получить общей теоретической формулы, выражающей эту зависимость.
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 307; Нарушение авторских прав?; Мы поможем в написании вашей работы!