
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теплоемкость твердых тел
|
|
|
|
В твердом теле единственным видом движения является колебания элементов кристаллической решетки, ячейки которой повторяются в пространстве. Твердое тело (например, металл) можно представить как набор гармонических осцилляторов, колеблющихся с одинаковой частотой n. Исследуя такую модель, Эйнштейн вывел теоретическую формулу для расчета теплоемкости твердого тела на основании статистической термодинамики
Сv = 3R (q/T)2 e q/T, где ( 4.6)
 (e q/T –1)2
(e q/T –1)2
где q = hn/k называется характеристической температурой.
При низкой температуре q/T → µ, a теплоемкость → 0
При высокой температуре q/T → 0, a теплоемкость → 3R
Закон Дюлонга и Пти для простых веществ:
Сv = суд.М = 6,3 кал/моль.К, где М - атомная масса элемента ( 4.7)
При очень низких температурах вблизи абс. нуля справедлив закон Дебая:
Сv = а Т3 ( 4.8)
4.8.3. Представление температурной зависимости теплоемкости в виде температурного ряда. Так как теоретических общих уравнений для зависимости теплоемкости от температуры нельзя вывести, то используются экспериментальные зависимости в виде степенного ряда
для органических веществ Ср = а + bТ + сТ2 + dT3; ( 4.9)
для неорганических веществ Ср = а + bТ + с' Т-2. ( 4.10)
4.8.4. Уравнение Кирхгоффа – зависимость теплоты реакции от температуры
Используя уравнения связи теплот химических реакций с изменением термодинамических функций легко вывести зависимость их от температуры
QV = DrU = 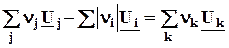 , ( 2.14,2.15 )
, ( 2.14,2.15 )
Qp = DrH = 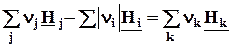 . ( 2.16 )
. ( 2.16 )
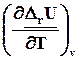 =
= 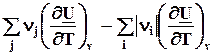 =
= 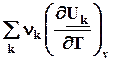 =
= 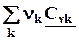 = DrСv, ( 4.11)
= DrСv, ( 4.11)
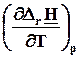 =
= 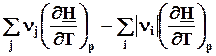 =
= 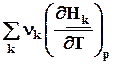 =
= 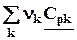 = DrСp. ( 4.12)
= DrСp. ( 4.12)
DrСp. = Dа + DbT + DcT2 + Dd T3 + Dc'T-2. ( 4.13)
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 260; Нарушение авторских прав?; Мы поможем в написании вашей работы!