
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Строение КС
|
|
|
|
1) КО – это нейтральный атом или катион, обладающий большим числом вакантных орбиталей, является акцептором неподеленных электронных пар.
Акцепторная способность тем выше, чем выше харяд и меньше размер КО.
Типичные КО – катионы d- или f-металлов (большие заряды, маленькие размеры)
d-Ме: Cu2+,Fe3+,Th4+,U6+,Ni2+
f-Ме: Ce4+, Eu2+, U+6, U+4, Pu+4
Реже – p-элементы (Al,Ga,S,N) и s-Ме (Ве)
2) L (лиганды) – нейтральные молекулы или анионы, имеющие в своем составе донорные атомы (атомы с неподеленной электронной парой)
По числу донорных атомов: Дентатность - число донорных атомов лиганда
- Монодентантные (1 электронная пара, 1 донорный атом) 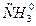 ,
,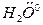 ,
,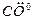 ,
,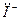 ,
,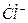 ,
,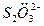 , F-, Е-
, F-, Е-
-Бидентантные (2 дон атома) CO32-, SO4, C2O42-
- Полидентантные
По заряду: - катионные [Cu(NH3)4]2+ ; - анионные [Fe(CN)6]4- ; - нейтральные [Ni(CO)4]0
КЧ – число донорных атомов, скоординированных вокруг КО;
- число сигма связей КО во вну сфере. КЧ = 2–15, но чаще 4,6,8
У Hg2+ КО=4
КЧ > Степ окисл КО. КЧ = 2*СОКО
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 432; Нарушение авторских прав?; Мы поможем в написании вашей работы!