
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Хлорофиллы
|
|
|
|
Хлорофилл – сложный эфир дикарбоновой кислоты хлорофиллина, у которой одна карбоксильная группа этерефицирована остатком метилового спирта, а другая – остатком непредельного спитра фитола. Элементарный состав хлорофилла а - С55Н72О5N4Мg и хлорофилла в – С55Н70О6N4Mg установил немецкий химик Р.Вильштеттер в 1906-1914 гг. Расшифровал структурную формулу хлорофилла немецкий биохимик Г.Фишер в 1930-1940 гг. У высших растений и водорослей обнаружены хлорофиллы а, в, с, d.
Молекула хлорофилла состоит из порфириновой «головки» и фитольного «хвоста». При этом порфириновая часть молекулы находится на поверхности мембраны тилакоидов и связана с белками, а жирорастворимая фитольная часть погружена в липидный слой. Порфириновое кольцо образовано четырьмя пиррольными кольцам и (I-IV) соединенными между собой метиновыми мостиками (α,β,γ,δ). При разрыве сложноэфирной связи и ощеплении фитола образуется соединение, называемое хлорофиллидом. Атомы азота пиррольных колец четырьмя координационными связями взаимодействуют с атомом магния. В структуре порфиринового ядра имеется также циклопентановое кольцо (V). Если в молекуле хлорофилла атом магния замещен на два атома водорода, образуется соединение буро-оливкового цвета – феофетин.

Физико-химические свойства хлорофилла.
Хлорофиллы не растворимы в воде, хорошо растворимы в этиловом эфире, бензоле, хлороформе, ацетоне, этиловом спирте. Хлорофиллы имеют два максимума поглощения света – в синей (430-460 нм) и красной (650-700 нм) областях спектра. Растворы хлорофилла в полярных растворителях обладают яркой флуоресценцией (люминесценцией). В этиловом эфире у хлорофилла а наблюдается рубиново-красная флуоресценция. Растворы хлорофиллов способны также к фосфоресценции (т.е. длительному послесвечению), максимум которого лежит в инфракрасной области.
.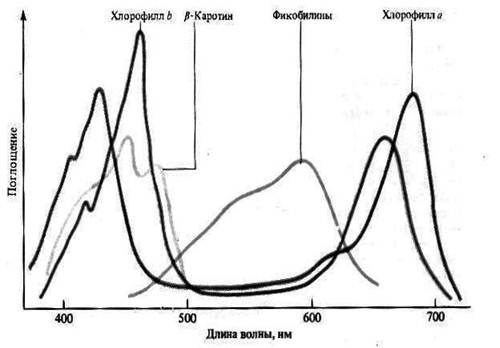
Рис. Спектры поглощения пигментов пластид.
Биосинтез молекулы хлорофилла. Синтез молекулы включает более 10 реакций. Некоторые из них требуют АТР, NADH и идут на свету. Синтез хлорофилла начинается с глутаминовой кислоты, которая превращается в аминолевулиновую кислоту. Далее две молекулы последней конденсируются и образуют порфобилиноген. Затем 4 молекулы порфобилиногена связываются и формируют протопорфирин IХ. После этого происходит встраивание магния и светозависимое формирование кольца V. На заключительной стадии синтеза происходит восстановление кольца IV и присоединение фитола.
Энергетические состояния молекулы хлорофилла.
Наиболее устойчивы те состояния атомов и молекул, в которых валентные электроны занимают самые низкие энергетические уровни и и распределены по ним согласно принципу Паули (не более 2 электронов с антипараллельными спинами на каждой орбитали). Такое состояние молекулы называют основным синглентным (Sо) энергетическим состоянием. Суммарный спин всех электронов молекулы в этом случае равен нулю. Когда молекула поглощает квант света, то за счет этой энергии электрон переходит на более высокие вакантные орбитали. Если у возбужденного электрона сохраняется то же направление спина, то молекула находится в синглентном возбужденном состоянии (S*) (рис.). Если при переходе на более высокую орбиталь, спин электрона обращается, то такое возбуждение называется триплетным (Т*). Время пребывания молекулы в возбужденном состоянии зависит от ее химического строения. Время жизни возбужденного состояния молекулы хлорофилла с сопряженными двойными связями и делокализованными π-электронами варьирует 10-10 – 10-9 с.
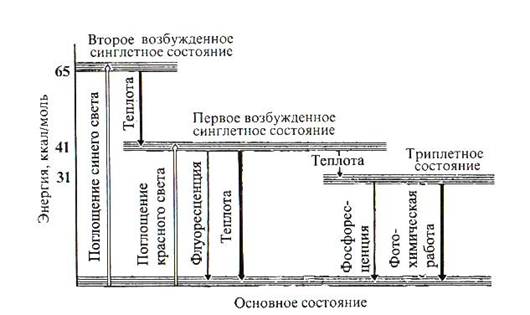
Рис. Энергетические состояния молекулы хлорофилла
Возвращение молекулы хлорофилла из синглентных в исходное состояние происходит несколькими путями: 1) флуоресценцией; 2) отдачей теплоты. Из триплетного состояния молекула может вернуться в основное энергетическое, излучив квант света более длинноволновой, чем при флуоресценции. Такое свечение называют фосфоресценцией. Более важной особенностью молекул в триплетном состоянии является способность участвовать в фотохимических реакциях, поскольку продолжительность их жизни сопоставима со скоростями химических процессов. В результате становится возможным превращение световой энергии в химическую. В этом случае флуоресценции и фосфоресценции не наблюдается.
Структура молекулы хлорофилла (она имеет 18 коньюгированных двойных связей) делает ее легко возбудимой при поглощении квантов сета и прекрасно приспособлена к своим функциям сенсибилизатора фотохимических реакций.
Таким образом, молекула хлорофилла благодаря структурным и физико-химическим особенностям способна выполнять три важнейшие функции:
- избирательно поглощать энергию света;
- запасать ее в виде энергии электронного возбуждения;
- фотохимически преобразовывать энергию возбужденного состояния в химическую энергию первичных фотовосстановленных и фотоокисленных соединений.
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 2417; Нарушение авторских прав?; Мы поможем в написании вашей работы!