
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Модель атома водорода по Бору
|
|
|
|
Первая попытка неклассической теории атома была предпринята Нильсом Бором в 1913 году. Классическое описание Н.Бор дополнил некоторыми ограничениями, накладываемыми на возможные состояния электронов в атоме. Они были сформулированы в виде постулатов. Теория Бора применима к водородоподобной системе, состоящей из ядра с зарядом Ze и одного электрона, вращающегося вокруг ядра (напр. 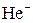 ).
).
| 1-ый постулат (постулат стационарных состояний) | Существуют некоторые стационарные состояния атома, находясь в которых он не излучает энергии |
| 2-ой постулат (правило квантования орбит) | В стационарном состоянии атома электрон, двигаясь по круговой орбите, должен иметь квантованные значения момента импульса, удовлетворяющие условию 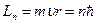 , где n = 1, 2, 3, …; m – масса электрона, , где n = 1, 2, 3, …; m – масса электрона, 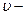 скорость электрона, r – радиус орбиты электрона, n – число, равное числу длин волн де Бройля для электрона, укладывающихся на длине круговой орбиты. скорость электрона, r – радиус орбиты электрона, n – число, равное числу длин волн де Бройля для электрона, укладывающихся на длине круговой орбиты.
|
| 3-ий постулат (правило частот) | При переходе атома из одного стационарного состояния в другое испускается или поглощается один квант энергии: 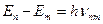 . При . При 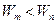 происходит излучение кванта, при происходит излучение кванта, при 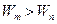 его поглощение. его поглощение.
|
Из сравнения:
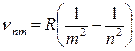 ;
; 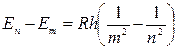 ;
;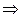
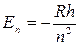 .
.
Бор считал, что движение электрона в атоме водорода происходит по круговой орбите радиуса r под действием кулоновской силы притяжения электрона к ядру, что позволило записать основной закон динамики для электрона в атоме в следующем виде: 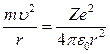 ; но, в соответствии со 2-ым постулатом Н.Бора, модуль момента импульса электрона на круговой орбите в атоме принимает дискретные значения или квантуется
; но, в соответствии со 2-ым постулатом Н.Бора, модуль момента импульса электрона на круговой орбите в атоме принимает дискретные значения или квантуется 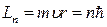 .
.
Следовательно 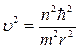 . После подстановки этого выражения в основной закон динамики:
. После подстановки этого выражения в основной закон динамики:
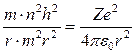 ; получаем выражение для возможных радиусов орбит электрона в атоме:
; получаем выражение для возможных радиусов орбит электрона в атоме:
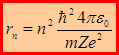 , здесь n = 1, 2, 3,…
, здесь n = 1, 2, 3,…
При n = 1 для водорода (Z = 1):
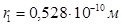 – первый боровский радиус.
– первый боровский радиус.
Полная энергия электрона в атоме:
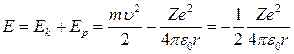 (для получения этого соотношения использован основной закон динамики
(для получения этого соотношения использован основной закон динамики 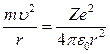 ). После подстановки в полученную формулу вместо r величины возможных радиусов rn получаем выражение для возможных дискретных значений энергии электрона в атоме:
). После подстановки в полученную формулу вместо r величины возможных радиусов rn получаем выражение для возможных дискретных значений энергии электрона в атоме:
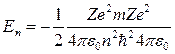 .
. 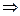
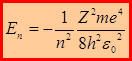 – энергия электрона в атоме квантуется. Число n называют главное квантовое число.
– энергия электрона в атоме квантуется. Число n называют главное квантовое число.
Из сравнения с 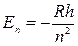 можно получить выражение для постоянной Ридберга:
можно получить выражение для постоянной Ридберга:
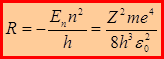 .
.
Для водорода (Z = 1): 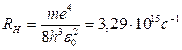 . Полученное значение хорошо согласуется со значением постоянной Ридберга, полученным экспериментально при изучении спектральных серий излучения атомарного водорода.
. Полученное значение хорошо согласуется со значением постоянной Ридберга, полученным экспериментально при изучении спектральных серий излучения атомарного водорода.
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 779; Нарушение авторских прав?; Мы поможем в написании вашей работы!