
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Первое начало термодинамики
|
|
|
|
Молекулярная физика и термодинамика
В разделе молекулярная физика и термодинамика рассматривают явления, сущность которых определяется хаотическим движением огромного числа молекул, из которых состоят тела разной природы. Изучая эти явления, применяют два основных метода. Один из них — термодинамический, он исходит из основных опытных законов, получивших название начал (законов, принципов) термодинамики. При таком подходе не учитывается внутренее строение вещества.
Другой метод — молекулярно-кинетический {cmamucтический) — основан на представлении о молекулярном строении вещества. Учитывая, что число молекул в любом теле очень велико, можно, используя теорию вероятностей, установить определенные закономерности.
Медикам данные вопросы важны для понимания энергетики организма, теплообмена биологических систем с окружающей средой, выяснения физических процессов, происходящих в биологических мембранах, и др.
Состояние термодинамической системы характеризуется физическими величинами, называемыми параметрами системы (объем, давление, температура, плотность и т. д.).
Если параметры системы при взаимодействии ее с окружающими телами не изменяются с течением времени, то состояние системы называют стационарным. Примерами таких состояний в течение небольшого отрезка времени являются, состояние внутренней части работающего домашнего холодильника, состояние тела человека, состояние воздуха в отапливаемом помещении и т. д.
В разных частях системы, находящейся в стационарном состоянии, значения параметров обычно различаются: температура в разных участках тела человека, концентрация диффундирующих молекул в разных частях биологической мембраны и т. п. В системе, таким образом, поддерживаются постоянные градиенты некоторых параметров, с постоянной скоростью могут протекать химические реакции.
|
|
|
Ясно, что в стационарном состоянии могут находиться такие системы, которые либо обмениваются и энергией, и веществом с окружающими системами (открытые системы), либо обмениваются только энергией (закрытые системы).
Термодинамическая система, которая не обменивается сокружающими телами ни энергией, ни веществом, называется изолированной. Изолированная система со временем приходит в состояние термодинамического равновесия. В этом состоянии, как и в стационарном, параметры системы сохраняются неизменными во времени. Существенно, что в равновесном состоянии параметры, не зависящие от массы или числа частиц (давление, температура и др.), одинаковы в разных частях этой системы.
Естественно, что любая реальная термодинамическая система не будет изолированной хотя бы потому, что ее невозможно окружить оболочкой, не проводящей теплоту. Изолированную систему можно рассматривать как удобную термодинамическую модель.
Мерой передачи энергии в процессе теплообмена является количество теплоты, а мерой передачи энергии в процессе совершения работы является работа.
Закон сохранения энергии для тепловых процессов формулируется как первое начало термодинамики. Количество теплоты, переданное системе, идет на изменение внутренней энергии системы и совершение системой работы:
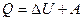
Под внутренней энергией системы понимают сумму кинетической и потенциальной энергий частиц, из которых состоит система.
Внутренняя энергия U является функцией состояния системы и для данного состояния имеет вполне определенное значение; 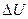 есть разность двух значений внутренней энергии, соответствующих конечному и начальному состояниям системы:
есть разность двух значений внутренней энергии, соответствующих конечному и начальному состояниям системы: 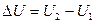
|
|
|
Количество теплоты Q, как и работа, является функцией процесса, а не состояния. И количество теплоты, и работу нельзя выразить в виде разности двух значений какого-либо параметра в конечном и начальном состояниях. В связи с этим Q и A записаны без знака приращения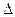 .
.
Первое начало термодинамики
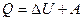
Здесь Q — количество теплоты, переданное системе; 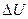 — изменение внутренней энергии системы; А — работа, совершаемая системой.
— изменение внутренней энергии системы; А — работа, совершаемая системой.
Работа, совершаемая газом при изменении объема от V1 до V2,

Где р — давление.
Для адиабатного процесса (Q = 0)
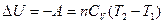 .
.
Здесь п — число молей идеального газа, СV — молярная теплоемкость газа при постоянном объеме, Т 1и Т 2— начальная и конечная температуры.
Обмен веществ в живых организмах также подчиняется первому закону термодинамики. Определение энергетического обмена между живыми организмами и окружающей средой осуществляется с помощью калориметрии, которая подразделяется на прямую и непрямую. Более распространенной является непрямая калориметрия. В этом случае о суммарном тепловом эффекте реакций, протекших в организме, судят по калорическому коэффициенту кислорода. Он показывает, какое количество теплоты выделяется при полном окислении данного вещества до углекислого газа и воды на каждый литр поглощенного организмом кислорода. Установлено, что этот коэффициент для углеводов равен 20,9, для жиров — 19,7 и для белков — 20,3 кДж. Однако в живом организме идет также синтез веществ, которые затем могут окисляться. Чтобы учесть общее количество теплоты, освобождаемое живым организмом за определенный промежуток времени, надо учитывать дыхательный коэффициент, равный отношению объемов углекислого газа к потребленному за то же время кислороду. Дыхательный коэффициент для углеводов равен 1, для белков — 0,8 и для жиров он составляет 0,7. Существует связь между дыхательным и калорическим коэффициентами (см. приложение 17). Это позволяет устанавливать расход энергии организма, зная количество поглощенного кислорода и выделенного углекислого газа.
Второе начало термодинамики. Энтропия
Первое начало термодинамики, являющееся, по существу, выражением закона сохранения энергии, не указывает направления возможного протекания процессов. Так, например, по первому началу термодинамики, при теплообмене одинаково возможным был бы как самопроизвольный переход теплоты от тела более нагретого к телу менее нагретому, так и, наоборот, от тела менее нагретого к телу более нагретому. Из повседневного опыта, однако, хорошо известно, что второй процесс в природе нереален; так, например, не может самопроизвольно нагреться вода в чайнике вследствие охлаждения воздуха в комнате.
|
|
|
Второе начало термодинамики, так же как и первое, является обобщением данных опыта.
Существует несколько формулировок второго закона термодинамики: теплота самопроизвольно не может переходить от тела с меньшей температурой к телу с большей температурой (формулировка Клаузиуса), или невозможен вечный двигатель второго рода (формулировка Томсона), т. е. невозможен такой периодический процесс, единственным результатом которого было бы превращение теплоты в работу вследствие охлаждения тела.
Все реальные процессы необратимы. Для возвращения системы в начальное состояние во всех случаях необходимо совершение работы внешними телами.
Физическую характеристику, не зависящую от процесса или перемещения, обычно выражают как разность двух значений некоторой функции, соответствующих конечному и начальному состояниям процесса или положениям системы
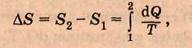
|
Аналогично, сумму приведенных количеств теплоты для обратимого процесса можно представить как разность двух значений некоторой функции состояния системы, которую называют энтропией:
где S2 и Sj — энтропия соответственно в конечном 2 и начальном 1 состояниях. Итак, энтропия есть функция состояния системы, разность значений которой для двух состояний равна сумме приведенных количеств теплоты при обратимом переходе системы из одного состояния в другое.
Количество теплоты для обратимого процесса

Изменение энтропии  при нагревании или охлаждении вещества от температуры T1 до температуры T2
при нагревании или охлаждении вещества от температуры T1 до температуры T2

где Ср — молярная теплоемкость при постоянном давлении.
|
|
|
Первый закон термодинамики как закон сохранения энергии настолько очевиден, что его применения к биологическим системам здесь не рассматриваются. Более существенно рассмотреть некоторые вопросы, связанные со вторым началом термодинамики и энтропией применительно к биологическим системам.
Биологические объекты являются открытыми термодинамическими системами. Они обмениваются с окружающей средой энергией и веществом.
Вообще говоря, живой организм — развивающаяся система, которая не находится в стационарном состоянии. Однако обычно в каком-либо не слишком большом интервале времени принимают состояние биологической системы за стационарное.
Рассмотрим в этом предположении некоторые вопросы. Для организма — стационарной системы — можно записать dS = 0, S = const, dSi > 0, dSe < 0. Это означает, что большая энтропия должна быть в продуктах выделения, а не в продуктах питания. Энтропия системы организм — окружающая среда возрастает как у изолированной системы, однако энтропия организма при этом сохраняется постоянной. Энтропия есть мера неупорядоченности системы, поэтому можно заключить, что упорядоченность организма сохраняется ценой уменьшения упорядоченности окружающей среды.
Неупорядоченность состояния системы количественно характеризуется термодинамической вероятностью WTep.
Термодинамической вероятностью называют число способов размещения частиц или число микросостояний, реализующих данное макросостояние.
Состояние системы, определяемое числом частиц в первой и второй ячейках, назовем макросостоянием; состояние системы, определяемое тем, какие конкретно частицы находятся в каждой из ячеек, — микросостоянием
Заметим, что если газу предоставить возможность расширяться, его молекулы будут стремиться равномерно занять весь возможный объем, при этом процессе энтропия увеличивается. Обратный процесс — стремление молекул занять лишь часть объема, например половину комнаты, — не наблюдается, этому соответствовало бы состояние со значительно меньшей термодинамической вероятностью и меньшей энтропией.
Отсюда можно сделать вывод о связи энтропии с термодинамической вероятностью. Больцман установил, что энтропия линейно связана с логарифмом термодинамической вероятности:
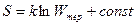
где k — постоянная Больцмана.
Второе начало термодинамики — статистический закон,
в отличие, например, от первого начала термодинамики или второго закона Ньютона.
Утверждение второго начала о невозможности некоторых процессов, по существу, является утверждением о чрезвычайно малой вероятности их, практически — невероятности, т. е. невозможности.
В космических масштабах наблюдаются существенные отклонения от второго начала термодинамики, а ко всей Вселенной, так же, как и к системам, состоящим из малого числа молекул, оно неприменимо.
В заключение еще раз отметим, что если первый закон термодинамики содержит энергетический баланс процесса, то второй закон показывает его возможное направление. Аналогично тому, как второй закон термодинамики существенно дополняет первый закон, так и энтропия дополняет понятие энергии.
При некоторых патологических состояниях энтропия биологической системы может возрастать (dS > 0), это связано с отсутствием стационарности, увеличением неупорядоченности; так, например, при раковых заболеваниях происходит хаотическое, неупорядоченное разрастание клеток.
Скорость изменения энтропии для стационарного состояния в живом организме

Здесь  — скорость изменения энтропии, связанной с необратимыми процессами в биологической системе;
— скорость изменения энтропии, связанной с необратимыми процессами в биологической системе; 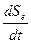 — скорость изменения энтропии вследствие взаимодействия системы с окружающей средой.
— скорость изменения энтропии вследствие взаимодействия системы с окружающей средой.
Отсюда видно, что при обычном состоянии организма скорость изменения энтропии за счет внутренних процессов равна скорости изменения отрицательной энтропии за счет обмена веществом и энергией с окружающей средой.
Поскольку, согласно принципу Пригожина, производная dSi/dt > 0, причем минимальна.
Отсюда можно сделать вывод, что скорость изменения энтропии окружающей среды при сохранении стационарного состояния организма также минимальна.
Основа функционирования живых систем (клетки, органы, организм) — это поддержание стационарного состояния при условии протекания диффузионных процессов, биохимических реакций, осмотических явлений и т. п.
При изменении внешних условий процессы в организме развиваются так, что его состояние не будет прежним стационарным состоянием.
Можно указать некоторый термодинамический критерий приспособления организмов и биологических структур к изменениям внешних условий (адаптации). Если внешние условия изменяются (возрастает или уменьшается температура, изменяется влажность, состав окружающего воздуха и т. д.), но при этом организм (клетки) способен поддерживать стационарное состояние, то организм адаптируется (приспосабливается) к этим изменениям и существует. Если организм при изменении внешних условий не способен сохранить стационарное состояние, выходит из этого состояния, то это приводит к его гибели. Организм в этом случае не смог адаптироваться, т. е. не смог сравнительно быстро оказаться в стационарном состоянии, соответствующем изменившимся условиям.
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 2042; Нарушение авторских прав?; Мы поможем в написании вашей работы!