
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Первый закон термодинамики для потока газа
|
|
|
|
ТЕМА 2
Сp - сv = R.
Pdv = RdT.
Dl = pdv.
Воспользуемся уравнением состояния в дифференциальной форме
Тогда RdT = (сp - сv)dT и, соответственно,
Эта зависимость называется уравнением Майера.
C учетом известного из курса физики уравнения Пуассона k = сp/cv получаем выражения для изобарной и изохорной удельных теплоемкостей идеального газа
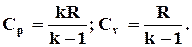
Если в выражении для первого закона термодинамики выполнить следующие преобразования
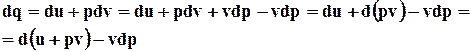
и ввести понятие энтальпии
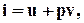
то получим уравнение для второй формы первого закона термодинамики
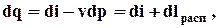
где lрасп - техническая или располагаемая работа.
Энтальпия, как и внутренняя энергия, является параметром состояния. Она всегда больше внутренней энергии на величину pv. Энтальпия включает энергию расширенной системы - рабочего тела во взаимодействии с окружающей средой. Произведение pv, имеющее размерность работы, по существу является работой по внедрению тела с объемом v в среду с давлением p. Условное начало отсчета энтальпии, как и внутренней энергии, принимают при 0K или 00С.
Приведенные ранее уравнения первого закона термодинамики не учитывают движения газа. Для движущегося газа часть тепла затрачивается на изменение кинетической энергии этого газа.
Рассматривая уравнение первого закона термодинамики для потока газа в наиболее общем виде можно получить следующее выражение
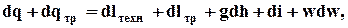
где dlтехн - техническая работа, совершаемая газом (например, в турбине, или в поршневой расширительной машине);
dqтр = dlтр - внутренний приток тепла за счет преобразования работы трения в теплоту;
gdh - изменение потенциальной энергии газа в поле сил тяжести;
 - изменение удельной кинетической энергии газа.
- изменение удельной кинетической энергии газа.
С учетом последнего замечания выражение первого закона термодинамики в дифференциальной форме приобретает вид


Это уравнение не содержит работы трения, т.к. она полностью преобразуется в тепло, которое остается в потоке газа.
Если изменение потенциальной энергии газа в поле сил тяжести мало и gdh» 0, а течение газа является энергетически изолированным от окружающей среды (dq = dlт = 0), то изменение энтальпии в таком энергетически изолированном процессе зависит только от изменения скорости газа. Тогда
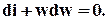
Отсюда следует, что постоянство скорости идеального газа в таком потоке предполагает и постоянство его температуры.
Для конечных изменений скорости и энтальпии уравнение приобретает вид
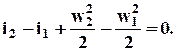
Это уравнение в газовой динамике часто называют уравнением энергии.
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 3907; Нарушение авторских прав?; Мы поможем в написании вашей работы!