
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ароматические углеводороды
|
|
|
|
НАФТЕНЫ (ЦИКЛОПАРАФИНЫ).
Все нефти содержат значительные количества циклопарафинов. Члены гомологического ряда этих углеводородов отвечают общей формуле СnН2n. Нафтенами в настоящее время называют не только производные циклопентана и циклогексана, впервые выделенные из нефти, но и полициклические полиметиленовые углеводороды нефтяного происхождения.
Нафтены присутствуют во всех фракциях, их содержание растет по мере утяжеления фракций. Только в наиболее высококипящих масляных фракциях их количество уменьшается за счет увеличения ароматических углеводородов. Из всех циклов наиболее устойчивыми являются пяти- и шестичленные циклы.
Аналогично парафинам.нафтены имеют насыщенный характер, так как кольца (циклы) углеродных атомов образуются из цепочек углеродных атомов в результате внутреннего вращения σ- углерод-углеродной связи вокруг своей оси. В присутствии сильных окислителей молекулы нафтенов окисляются с разрывом кольца, например, из циклогексана получается адипиновая кислота.
СН2
H2C СН2
H2C СН2 ОКИСЛ НООС-(СН2)4-СООН
CH2
Циклогексановые углеводороды в присутствии катализаторов (Pt, Ni, Pd) при 300°С дегидрируется в ароматические углеводороды (реакция Зелинского Н.Ф.)
Циклопентан и циклогексан, а также их гомологи с короткими боковыми цепями являются ценными составными частями бензинов, т.к. обладают хорошей детонационной стойкостью.
Содержание ароматических углеводородов (в % на фракцию) возрастает с ростом температуры кипения нефтяных фракций. Почти во всех нефтях преобладают углеводороды С6Н6 - С8Н10 (бензол, толуол и ксилолы). В керосино-газойлевых фракциях наряду с гомологами бензола присутствуют гомологи нафталина; в высших фракциях содержатся более сложные полициклические ароматические углеводороды с 3, 4 и даже 5конденсированными ядрами.
Химические свойства ароматических углеводородов определяются специфическим строением бензольного ядра.
Sp2 - гибридизация шести атомов углерода приводит к замыканию шестичленного кольца и возникновению плоской молекулы бензола. У каждого атома углерода имеется также по одному ρ -электрону и эти шесть ρ электронов образуют сопряженные π -связи и принадлежат всем атомам углерода в молекуле.
CH3 CH3 C2H5
бензол толуол n - ксилол этилбензол
CH3
Наиболее характерным типом реакций ароматических углеводородов являются реакции замещения и алкилирования.
Эта реакция имеет важнейшее промышленное значение, в частности, она является первой стадией при синтезе целого ряда присадок к маслам и
топливам, позволяет получать высокооктановые компоненты моторных топлив.
Очень важна реакция гидрирования ароматических соединений, которая лежит в основе процессов деароматизации полициклических ароматических углеводородов.
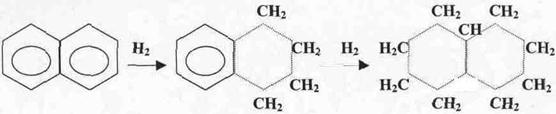
Нафталин Тетралин Декалин
Содержание ароматических углеводородов в дизельных топливах снижает полноту сгорания и вызывает значительное нагарообразование в двигателе.
Значительную часть углеводородов нефти составляют углеводороды смешанного строения, в молекулах которых имеются ароматические кольца, пяти- и шестичленные нафтеновые циклы и парафиновые цепи различной длины и строения. Такие полициклические углеводороды с короткими боковыми цепями должны удаляться из маслянных фракций в процессе их очистки, т. к. значительно ухудшают эксплуатационные свойства смазочных масел.
В углеводородах атомы водорода замещаются на атомы или группы атомов (функциональные группы), образуя различные классы органических соединений. При этом атомы - заместители и функциональные группы определяют главнейшие направления химических превращений данного класса органических соединений.
Производные углеводородов, в молекуле которых один или несколько атомов водорода замещены на атомы галогена F, Cl, Br, J, называются галогенопроизводными (R - Г). Прочность связи углерод - галоген растет от йода к фтору, поэтому фтороуглеводороды имеют высокую химическую устойчивость, например, фтороуглеводороды и смешанные галогенопроизводные нашли применение в качестве рабочих тел в холодильных установках - хладонов (фреоновСF2 Cl2, CF2ClBr и др. Из тетрофторэтилена F2С = CF2 получают полимер тефлон - химически более стойкое вещество, чем платина.
Основные реакции галогенопроизводных углеводородов сводятся к замещению атомов галогенов на другие функциональные группы, однако, подвижность атомов галогенов при углероде с двойной связью невелика, поэтому они не способны к реакциям замещения, но широко используются в промышленности для получения полимерных материалов (например, СН2 =СН-С1 - хлористый винил).
n CH2 = CH - Cl - CH2 - CH -
Cl n
Сера присутствует в нефти в виде свободной серы и различных соединений, например H2S, R - SH (меркаптаны); R - SMe (меркаптиды); R - S - R'
(сульфиды); R - S - S - R' (дисульфиды);
HC CH тиофен и его производные; CH2 CH2 тиофан и его
производные
HC CH CH2 CH2
S S
полициклические серосодержащие соединения различной структуры и др.
Кислород входит в состав нефти в виде карбоновых и нафтеновых кислот, фенолов, смолисто-асфальтеновых веществ. В небольших количествах встречаются кетоны, альдегиды, эфиры, реже ангидриды, спирты.
Спирты - это производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильные группы. Общая формула спиртов R (ОН)п. Одноатомные спирты - алкоголи, двухатомные -гликоли, трехатомные - глицерины.
Из-за полярности связи кислород - водород (- О - Η) молекулы спиртов полярны.При воздействии щелочных металлов спирты образуют алкоголяты:
C2H5OH+Na C2H5ONa+l/2H2
При замещении водорода ароматического кольца на группу ОН" образуется фенол. Под влиянием бензольного кольца полярность связи кислород - водород возрастает, поэтому фенолы диссоциируют в большей степени, чем спирты, и проявляют кислотные свойства.
Атом водорода в гидроксогруппе фенола может быть замещен на катион металла под воздействием основания:
OH ONa
+NaOH +H2O
атомы галогена замещают в бензольном ядре атомы водорода, находящиеся в о- и n- положениях относительно ОН- группы.
При окислении и каталитическом дегидрировании спиртов можно получить альдегиды и кетоны, соединения, содержащие карбонильную группу C = 0
+O O R
R - CH2OH R - C + H2O; R - CH - OH + O C = O + H2O
(+H) H R R
первичный спирт альдегид вторичный спирт кетон
Сернистые соединения всех видов являются вредными примесями в
нефтепродуктах, т.к. вызывают сильную коррозию аппаратуры; повышают
токсичность нефтепродуктов; снижают октановые числа бензинов и т.д. В
настоящее время основным методом очистки нефтепродуктов от серы является их каталитическое гидрирование (гидроочистка).
Окисление третичных спиртов происходит лишь с разрывом связи между
Окисление третичных спиртов происходит лишь с разрывом связи между атомами углерода.
Связь кислород - углерод карбонильной группы альдегидов сильно поляризована, поэтому альдегиды характеризуются высокой реакционной способностью. Они являются хорошими восстановителями, легко вступают в реакции замещения, присоединения, конденсации и полимеризации.
Кетоны обладают меньшей реакционной способностью, так как карбонильная группа менее полярна.
Продуктами окисления альдегидов являются обычно кислоты, содержащие в молекуле то же число атомов углерода, что и исходные альдегиды.
R - C- H + O R - С - ОН
O O
В качестве окислителя пользуются аммиачным раствором оксида серебра [ Ag (NH3)2 ] ОН, при этом происходит реакция «серебряного зеркала», широко используемая в практике:
O O
R - С + 2[Ag (NН3)2]ОН R - С +3NH3 + H2O + Ag
H ONH4
Кислотные свойства карбоксильной группы обусловлены отщеплением протонов связанным с поляризованностью связи О - Н, вызванной смещением электронно плотности от атома углерода к атому кислорода карбоксильной группы.
O O
-C+ - O- - H+ R - C R - C + Η+
O-0 OH  O
O
Все кислые вещества, выделяемые из нефти экстрагированием щелочи, называются нефтяными кислотами, основную часть которых составляют нафтеные кислоты (т. е. кислоты, в состав которых входят нафтеновые циклы). Наибольшее количество их содержится в соляровых и масляных дистиллятах. В бензинах и керосинах содержатся алифатические (карбоновые) кислоты, содержащие от С1 до C6 атомов. В нефти присутствуют и более высокомолекулярные кислоты, имеющие общие формулы СnН2n-4Ο2 и CnH2n-8O2.
Пo химическим свойствам нафтеновые кислоты близки к карбоновым кислотам. Они способны образовывать все характерные для кислот производные, например:
O O O
а) Амиды:R - С + NH3 R - C H2O + R - C
OН ONH4 NH2
O O
б) Ангидриды: R - C + R -C (RCO)2O + NaCl
ONa Cl
O O
в) Сложные эфиры: R - C + ROH H2O + R - C
OH O
O
г) Соли: R - C + NaOH R - COONa + H2O
OH
Нефтяные кислоты образуют соли не только с щелочами, но и с оксидами металлов. В присутствии воды и при повышенных температурах они реагируют непосредственно с металлами, также образуя соли, и коррозируют металлическую аппаратуру. Легче всего они разрушают свинец, цинк, медь, а в меньшей степени, железо и алюминий. Таким образом, нефтяные кислоты являются вредными примесями и подлежат удалению из нефтепродуктов в процессе их очистки.
Основная масса азотистых соединений нефти концентрируется в высококипящих фракциях и остатках, например, аминогруппа очень активно вступает в различные реакции, проявляя основные свойства:
R - NH2 + HCl [R-NH3Cl]
Большинство азотистых соединений склонно к многочисленным реакциям, в том числе к окислению, конденсации, полимеризации. В процессах переработки нефти и при эксплуатации двигателей азотистые соединения играют отрицательную роль: усиливают процессы лакообразования в цилиндропоршневой группе:, при хранении топлив (дизельное, мазут) часть азотистых соединений является источником интенсивного образования смолисто - асфальтеновых веществ.
|
|
|
|
|
Дата добавления: 2013-12-14; Просмотров: 757; Нарушение авторских прав?; Мы поможем в написании вашей работы!