| Назва закону (рівняння)
| Формулювання
| Математичний вигляд
| Примітка
|
| Закон Бойля -Маріотта (1662, 1676)
| При постійній температурі об’єм газу обернено пропорційний його тиску.
| Т=соnst;
р1∙V1 = р2∙V2
|
|
| Закон Шарля (1787)
| При сталому тиску об’єм газу прямо пропорційний температурі.
| 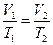 , P=const , P=const
|
|
| Закон Гей-Люссака (1802)
| При сталому об’ємі тиск газу прямо пропорційний температурі.
|  , V=соnst , V=соnst
| Об’єм газу при зміні його температури на 10С змінюється на 1/273 частину того об’єму, який він займав при 00С. (абсолютний О К або –2730С)
V=0 при ОК.
|
| Закон Авогадро
(1811)
| У рівних об’ємах будь-яких газів за однакових умов міститься однакова кількість молекул.
| 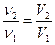 , P=const
Т=соnst; , P=const
Т=соnst;
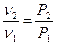 , V=соnst
Т=соnst , V=соnst
Т=соnst
| За н.у. молярний об’єм різних газів становить 22,4л/моль
ρ = 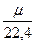 , ρ – нормальна густина газу, г/л
ν = , ρ – нормальна густина газу, г/л
ν = 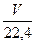 , кількість речовини, моль , кількість речовини, моль
|
| Об’єднаний газовий закон (клапейрон, 1834)
| -
| 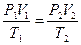

| Дозволяє обчислити параметри певного газу в 2-х його різних станах.
Нормальні умови:
Р0 = 1,01∙105Па
Т0 = 273К
Зведення об’єму газу до н.у.
|
| ?Температура характеризує середню енергію поступового руху середньої частинки тіла, що складається із необмеженої багато чисельної кількості частинок (середньостатистична властивість).
|
| Назва закону (рівняння)
| Формулювання
| Математичний вигляд
| Примітка
|
| Закон Дальтона (1801) закон парціальних тисків
| Загальний тиск суміші газів, що хімічно не взаємодіють один з одним, дорівнює суміші їх парціальних тисків.
| Р = 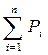 Рі = хі ∙ Р (Т = const)
Рі – парціальний тиск;
Р – загальний тиск газової суміші.
Рі = хі ∙ Р (Т = const)
Рі – парціальний тиск;
Р – загальний тиск газової суміші.
| Парціальний тиск – це той тиск, який створював би газ, якби займав весь об’єм суміші при тій самій температурі та відсутності інших газів.
хі – молярна частка і-го компонента суміші газів.
|
| Рівняння стану ідеального газу
| Встановлює функціональну залежність тиску, об’єму, температурі та кількості газу
| РV = νRТ
| ν – кількість газу, моль;
R – універсальна газова стала, 8,31Дж/(моль∙К);
Р – тиск, Па;
Т –температура, К
|
| Рівняння Клапейрона-Мендєлєєва
| -
| РV =  RT RT
| V – об’єм газу, м3
μ – молярна маса, г/моль
m – маса газу, г
Дозволяє обчислити молярну масу газу
|
| | | | | | |

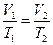 , P=const
, P=const
 , V=соnst
, V=соnst
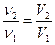 , P=const
Т=соnst;
, P=const
Т=соnst;
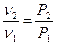 , V=соnst
Т=соnst
, V=соnst
Т=соnst
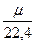 , ρ – нормальна густина газу, г/л
ν =
, ρ – нормальна густина газу, г/л
ν = 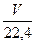 , кількість речовини, моль
, кількість речовини, моль
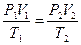

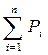 Рі = хі ∙ Р (Т = const)
Рі – парціальний тиск;
Р – загальний тиск газової суміші.
Рі = хі ∙ Р (Т = const)
Рі – парціальний тиск;
Р – загальний тиск газової суміші.
 RT
RT