
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Водневий електрод. Будова, принципи роботи, призначення
|
|
|
|
| Стандартний водневий електрод – це платинова пластина, занурена у розчин сірчаної кислоти з активністю іонів водню, що дорівнює одиниці при температурі 298К. Платинова пластинка насичується воднем під тиском 101,3 кПа = 1атм. Схематично стандартний водневий електрод записують так: Рt, H2 │ 2H+ (Рн2 = 101,3 кПа; а Н+ = 1 моль/л). На електроді відбувається реакція: 2Н3О+ + 2е- «Н2 + 2Н2О Рівняння Нернста для потенціалу водневого електрода при 298К і Рн2 = 101,3 кПа має вигляд: Еводн = Е0 + 0,059 lg a (Н3О+). Враховуючи, що Е0водн = 0,00В остаточно одержуємо: Еводн = 0,059 lg a (Н3О+). Для визначення стандартних електродних потенціалів складають таке гальванічне коло: Рt, H2 │ 2H3О+ ││ Меn+│Ме ЕРС (електрорушійна сила) цього кола є величиною позитивною, дорівнює алгебраїчній різниці електродних потенціалів: ЕРС = е+ ‑ е-, де е+ і е- ‑ потенціали позитивного та негативного електродів. Оскільки Е0водн = 0,00В, то ЕРС = Е0Меn+│Ме | 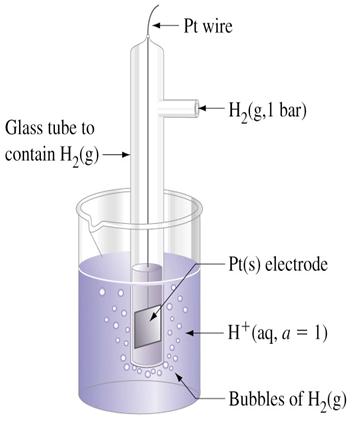
|
· Якщо потенціал металевого електроду має позитивне значення, то запис електрохімічного кола має вигляд:
(-)Рt, H2 │ 2H3О+ ││ Cu2+│Cu (+)
Н2 + 2Н2О -2e - ® 2Н3О+
Cu2+ +2e - ® Cu0
Сумарна реакція: 2Н2О + Н2 + Cu2+ ® 2Н3О+ + Cu0 ЕРС = Е0 Cu2+│Cu = + 0,34В
· Якщо потенціал металевого електрода має негативне значення і гальванічне коло для визначення стандартного потенціалу записується так:
|
|
|
|
|
Дата добавления: 2013-12-14; Просмотров: 6840; Нарушение авторских прав?; Мы поможем в написании вашей работы!