
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция 13. 1. Полипептиды window.top.document.title = "13.4
|
|
|
|
1. Полипептиды window.top.document.title = "13.4. Полипептиды";
При взаимодействии аминогруппы одной и карбоксильной группы другой α-аминокислот возникает амидная или пептидная связь. В основе образования пептидной связи лежит реакция конденсации
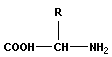 +
+ 
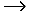
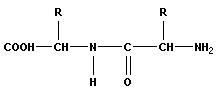 +
+ 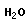
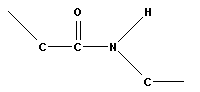
В пептидной группировке π-электроны делокализованы, что создает возможность для образования двух изомерных форм:
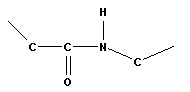
| 
| |
| транс- | цис- |
Более устойчива транс-форма, именно она присутствует в натуральных белках.
Валентные углы и межатомные расстояния во всех пептидных группировках практически постоянны, но зависят от природы расположенных по бокам пептидной цепи радикалов R.
В названии пептида слева указывается аминокислота со свободной аминогруппой (N – концевая аминокислота), справа – аминокислота со свободной карбоксильной группой (C – концевая аминокислота).
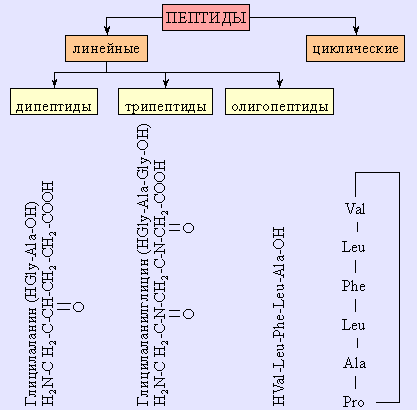
|
| Рисунок 13.2. Классификация пептидов. |
2. Белки window.top.document.title = "13.5. Белки";
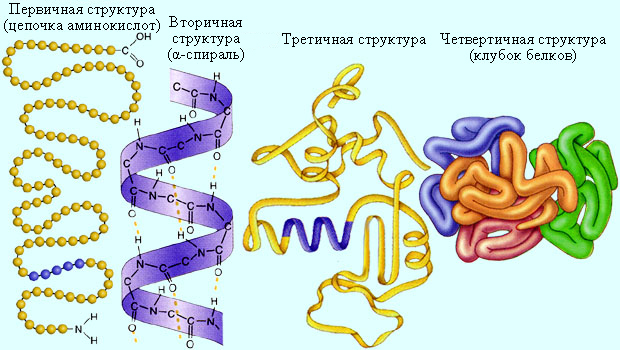
Белки – высокомолекулярные соединения, образующиеся в результате связывания отдельных полипептидных цепей водородными связями. Все белки подразделяются на глобулярные и фибриллярные. Глобулярные белки компактны, обладают сферической и приближенными к ней формами. Глобулярный белок диаметром 2,5 нм представляет собой полипептидную цепь длиной до 50 нм, свернутую в клубок. Фибриллярные белки обычно вытянуты и входят в состав тканей, мышц, волос. Полипептидные цепи такого белка, свернутые в винтовую спираль, ориентированы параллельно друг другу. На рис. 13.3 приведена структура нити мышечного белка. Одной из важнейших вторичных структур является α-спираль, впервые найденная Л. Полингом и Р. Б. Кори.
|
| Рисунок 13.3. Структура нити мышечного белка. |
Белковую природу имеют многочисленные ферменты, которые катализируют реакции определенного типа. Ферментам свойственна высокая избирательность, наибольшая активность при нормальной температуре организма, зависимость ферментной активности от pH. Ферменты разделяются на шесть классов:
1. Оксидоредуктазы – катализируют окислительно-восстановительные процессы.
2. Трансферазы – катализируют перенос химических групп (радикалов).
3. Гидролазы – катализируют гидролитические процессы.
4. Лиазы – обеспечивают присоединение по двойным связям или их образование.
5. Изомериазы – участвуют в процессах изомеризации.
6. Синтетазы – обеспечивают реакции конденсации двух молекул с участием фосфатных групп.
Для обеспечения каталитической функции многие ферменты содержат в молекуле небелковую часть – кофактор. Кофакторами могут быть органические вещества или ионы биометаллов, а также....
3. Витамины и гормоны window.top.document.title = "13.7. Витамины и гормоны";
Витамины – биохимически активные низкомолекулярные органические и биокоординационные соединения, необходимые для обеспечивания жизненно важных функций организма. Недостаток того или иного витамина приводит к тяжелым заболеваниям. Известны около 20 соединений, относимых к витаминам. Витамины делятся на водо- и липидорастворимые и относятся к нескольким группам, обозначаемым прописными буквами латинского алфавита A, B, C, D, E, K.
Витамины группы А – производные 4-(2',2',6-триметилгексен-1')-бутен-3-ОН-2.
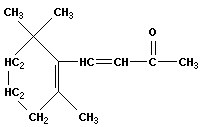

|
| Рисунок 13.6. Особенно богата морковь каротином – провитамином А, который образно называют «витамином роста». |
Они образуются только в животных организмах, но из предшественников, синтезируемых растениями. Такие каротиноподобные провитамины содержатся в шпинате, моркови. Витамины группы А содержатся в молочных продуктах, животном жире, яйцах, но особенно много их в рыбьем жире. Наиболее важные витамины группы А – ретинол (А1), ретиналь (A1-альдегид), ретиноевая кислота (A2) и др.
Первым из витаминов был открыт витамин B, а в 1926 г. была установлена его структура.
Витамины группы B – азотсодержащие гетероциклические соединения, отвечающие за процессы роста (B1, B2), нормальное развитие кожи (B6), кроветворную способность (B12). Простейшим является 3-пиридинкарбоновая кислота (иногда называемый PP), наиболее сложным – B12, относящийся к биокоординационным соединениям.
Хорошо известный витамин C – аскорбиновая кислота – относится к группе витаминов C – производных L-гулоновой кислоты. Собственно витамин C в лактонном виде имеет формулу
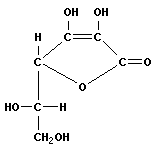
Эта группа витаминов обладает многофункциональным действием (наиболее известное – противоцинготное).
Витамины группы D препятствуют развитию рахита. Некоторые из них могут синтезироваться из веществ-предшественников в коже под действием солнечного света, другие поступают с пищей.
Витамины группы E регулируют процессы размножения, а витамины группы K – свертываемость крови.
Гормоны вырабатываются железами внутренней секреции (эндокринными) и регулируют обменные процессы в организме.
Известно более 40 гормонов, объединяемых в три группы: производные аминокислот, пептидные и стероидные. К первой относятся адреналин, ко второй инсулин, к третьей – мужские (производные андростана R = CH3) и женские (производные эстрона R = H) половые гормоны:
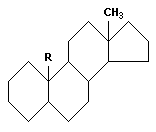
К стероидам относится холестерин
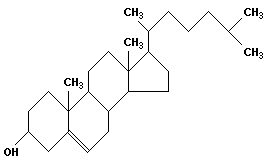
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 362; Нарушение авторских прав?; Мы поможем в написании вашей работы!