
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вопрос 3. Равновесие в процессах адсорбции
|
|
|
|
Независимо от природы адсорбционных сил количество вещества, адсорбированного единицей массы или объема определенного адсорбента, зависит от природы поглощенного вещества, температуры, давления и количества примесей в фазе, из которой поглощается вещество.
Зависимость между равновесными концентрациями поглощенного вещества в твердой и газовой или жидкой фазе в общем виде выражается уравнением
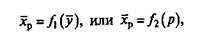 (1)
(1)

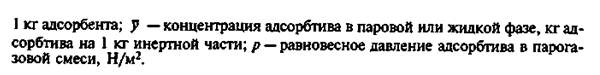
Зависимости, описываемые уравнениями (1), называются изотермами адсорбции. На основании законов химической термодинамики найдены конкретные выражения изотерм адсорбции, называемые изотермами Лэнгмюра:
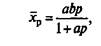 (2)
(2)
или Фрейндлиха:
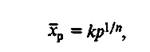

Адсорбции способствуют пониженная температура и повышенное давление над адсорбентом, а также отсутствие примесей в фазе над адсорбентом.
Вид изотермы адсорбции зависит от многих факторов: удельной площади поверхности адсорбента, объема пор, структуры адсорбента, свойств поглощаемого вещества, а также от температуры процесса. На рис. 21.1 изображены пять основных типов изотерм адсорбции. Тип 1 характерен для микропористых адсорбентов. Начальные выпуклые участки изотерм типов 2 и 4 также связаны с микропорами. Последующую форму изотерм определяют полимолекулярная адсорбция и капиллярная конденсация. Вогнутые участки на изотермах 3 и 5 характерны для систем адсорбент — адсорбтив, когда силы взаимодействия молекул адсорбтива с адсорбентом меньше сил межмолекулярного взаимодействия для молекул адсорбтива. Эти изотермы встречаются сравнительно редко.
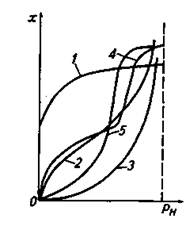
Рис. 1. Основные типы изотерм
Установлено, что при адсорбции из паровой или жидкой фазы нескольких веществ адсорбируются все вещества, однако равновесная концентрация каждого будет ниже, чем при адсорбции индивидуального вещества.
Существуют различные теории адсорбции, каждая из которых удовлетворительно описывает экспериментальные данные в определенных условиях. М.М.Дубинин рассматривает процесс адсорбции микропористым адсорбентом как процесс заполнения микропор адсорбтивом. Полученные им уравнения адсорбции для газов и паров в широком диапазоне температур характеризуют зависимость равновесной концентрации адсорбтива от структуры пор адсорбента. Такие уравнения имеют сложный характер. Одно из полученных М. М. Дубининым уравнений
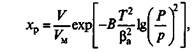 (3)
(3)

Адсорбция сопровождается уменьшением давления пара поглощаемого вещества в исходной смеси и выделением теплоты, поэтому в соответствии с принципом Ле-Шателье количество адсорбированного вещества возрастает с понижением температуры и повышением давления. Таким образом, понижение давления и повышение температуры способствуют обратному процессу — десорбции.
Количество выделяющейся при адсорбции теплоты (кДж/кмоль) определяют экспериментально. При отсутствии опытных данных оно может быть вычислено по уравнению
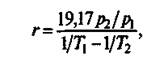 (4)
(4)
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 540; Нарушение авторских прав?; Мы поможем в написании вашей работы!