
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Эфирлену
|
|
|
|
Эфирлену реакциясы деп-барлық күрделі эфирлер түзетін процестерді атаймыз.Эфирленуді қышқылмен спирттің бірге дегидратация процесі деп қарастыруға болады.
RCOOH+R/OH=ROOR/ +H2O
Жалпы әдістерден басқа күрделі эфирлерді алуды келесіден көрсетуге болады:
1.Карбон қышқылдарының хлорангедридімен спирттердің әрекеттесуінен
СН3-СОСL+C2H5OH→CH3-COOC2H5+HCL
2.Жоғарғы қысымда,H2SO4 қатысында карбон қышқылдарының олефиндермен әрекеттесуінен.
СН3СООН+СН3-С=CH2→CH3COOCH2-CH-CH3
│ │
CH3 CH3
Карбон қышқылдарының,олефиндердің спирттермен бірге эфирленуі келесі жағдайларда жүреді.
а)Олефиндерден спирт алу стадиясы болмайды;
б)Судың бөлінуі қажет емес;
в)Олефиннің мөлшері карбон қышқылына қарағанда көп болса,тазалық дәрежесі жоғары эфир алуға болады;
г)Реакция жылдамдығы жоғарылайды.
3.Кейбір эфирлену процестерінің көрсеткіштері.
| Алынатын эфир. | Этилен:қышқыл қатынасы, моль:моль | Температура, 0С | Қысым, атм | Реакция уақыты, сағ | Эфирге қышқылдың конверсия дәрежесі |
| Этилацетат | 3,89:1 | 77,3 | 86,9 | ||
| Этилпропионат | 7,33:1 | 105,5 | 79,4 | ||
| Этилбутират | 10,20:1 | 133,6 | 81,5 |
Үшінші кестеден көбіне сірке қышқылының жеңіл эфирленетіні көрінеді.Қышқыл молекуласындағы көміртек атомының көбеюнен,эфирдегі қышқылдың конверциялану дәрежесі төмендейді.
3.СО-нің спирт және олефинмен әрекеттесуінен.
СО+СН3ОН+СН2=СН2→СН3-СООС2Н5
Бұл синтезді екі жолмен жүзеге асыруға болдады.Газ тәрізді СО-н және қышқылдық катализаторды қолданып,процесті 700-1000атм. және 200-3000С-та жүргізеді.Егер көміртегі оксидінің көзі ретінде карбонилдерді қолдансақ мысалы Ni(CO)4онда реакция сол температурада қысымды 150 атм-ға дейін төмендеткенде жүреді.
4.Альдегидтің екі молекуласын Тишенко реакциясы бойынша конденсацияланады.
2CH3COH →CH3COOC2H5
Бұл жолмен зауықтық маштабта этилацетатын алады.Катализатор-алюминий этилаты мен хлористі алюминий қоспасы және кішкене мөлшердегі мырыш этилаты.Процесті 00С-та этилацетатың этил спиртіндегі қоспасына ацетальдегид және катализатор қосып жүргізеді
Альдегидтің конверсия дәрежесі 98%-ке жетіп шығын 97-98%-ті құрайды.
5. Кетеннің спиртпен әрекеттесуі.
СН2=С=O+C4H9OH→ CH3COOC4H9
Реагирлеуші зат массасынан 0,25% мөлшерінде күкірт қышқылын акатализатор ретінде қолданып,жоғарғы шығынды эфир алады.
6.Күрделі эфирлерді карбон қышқылының ангидридіне әрекеттесу қабілеті төмен спирттерді қосып алу.
(R-CO)2O+2R′-OH→2RCOOR′+H2O
(R-CO)2O+R′-OH→RCOOR+RCOOH
Бұл әдіспен кең қолданылатын ацетат,пропионат және целлюлзаның ацетобутиратын алады.
Алкил-қышқылды байланысты және олефиндерден тура синтез арқылы эфир алу реакциясы. Жоғарыда қарастырған ацил-қышқылды байланысты реакциядан басқа алкил-қышқылды байланыстың түзілуі және ыдырауы нәтижесінде эфирлену және күрделі эфир түзілуіп жүруі мүмкін.Оларда жиі аралық карбокатионның пайда болуы жүреді,және оларға алкил-қышқылды байланыстың поляризациялануы немесе карбкатионның тұрақтылығынан болатын спирттер мен қышқыл компоненттерінің құрылысы тән.Осы себепті кейбір күрделі эфирлер әсіресе күкірт эфирі және арилсулфоқышқылы белгілі алкилдеуші агент болып табылады.
Карбон қышқылдары жағдайында күрделі үшіншілік спирт эфирлері синтезі кезінде изоолефиндер түзіледі.
H
RCOO(CH3)-3↔RCOO< +H+↔+RCOOH↔ C(CH3)3-+H+↔(CH3)2C=CH2
C(CH3)3
Процестің кері бағыты карбон қышқылдары мен олефиндерден тура синтез арқылы эфир алуға негізделген.Реакция эндотермиялық және экзотермиялық мінездемесін олефиндердің гидратациясы және спирттердің эфирленуінің есебіне қарауға болады:
RCH=CH2+H2O→RCOOH-CH3+RCOOH→RCOO-CHR-CH3+H2O
Олефиндердің реакцияласу қабілеті аралық тұрақты карбкатиондарға бағынышты және қатар бойынша өзгереді.
(CH3)2C=CH2>CH3-CH=CH2>CH2=CH2
Реакцияласу қабілеті төмен этилен,тепе-теңдік процесс жүруіне сай келмеген жағдайда өте жоғары температура қажет етеді.Сондықтан реакцияны көбіне пропилен және оның гомологтарына қолданылады.
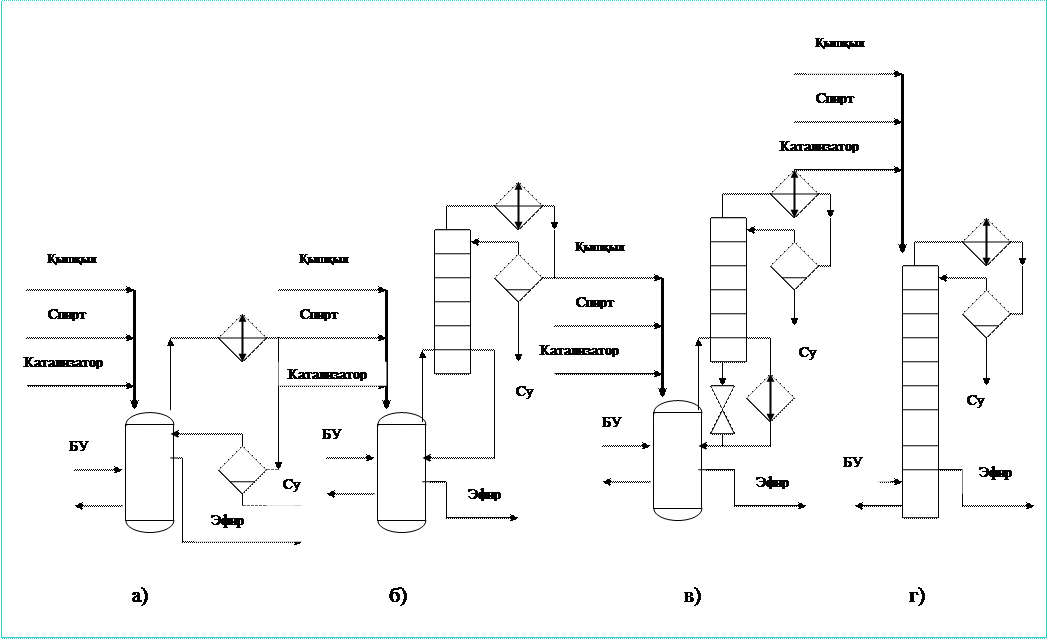
Типтік мысал ретінде жеңіл қайнайтын этилацетат эфирің техникалық схемасын қарастырамыз.(37 суретте берілген).Напорлы бактен 1 сірке қышқылы,этанол және катализатор ретінде күкірт қышұылынан тұратын бастапқы реагенттер қоспасы расходаметр арқылы үздіксіз реакцияға түседі.Ол бірінші жылу алмастырғышқа 2 түседі, сосын реакциялық колоннадан шығатын бу арқылы қыздырады және сосын жоғары эфиризатор тарелкесіне 4 барады.Куб колонкасының көмегімен этил ацетатпен бірге спирт буынан түзілген өткір бу және су колоннадан айдалады,ал сұйықтық тарелкамен төмен қозғалып сумен молаяды.Реакциялық массаның эфиризаторға келу уақытын және бастапқы реагенттер қатынасын,кубтық сұйықтық аз мөлшерде реагирленбеген сірке қышқылыннан тұратындай етип алады (онда әліде күкірт қышқылы қалады).Бұл сұйықтықты кубтан шығарады және бейтараптап канализацияға жібереді.
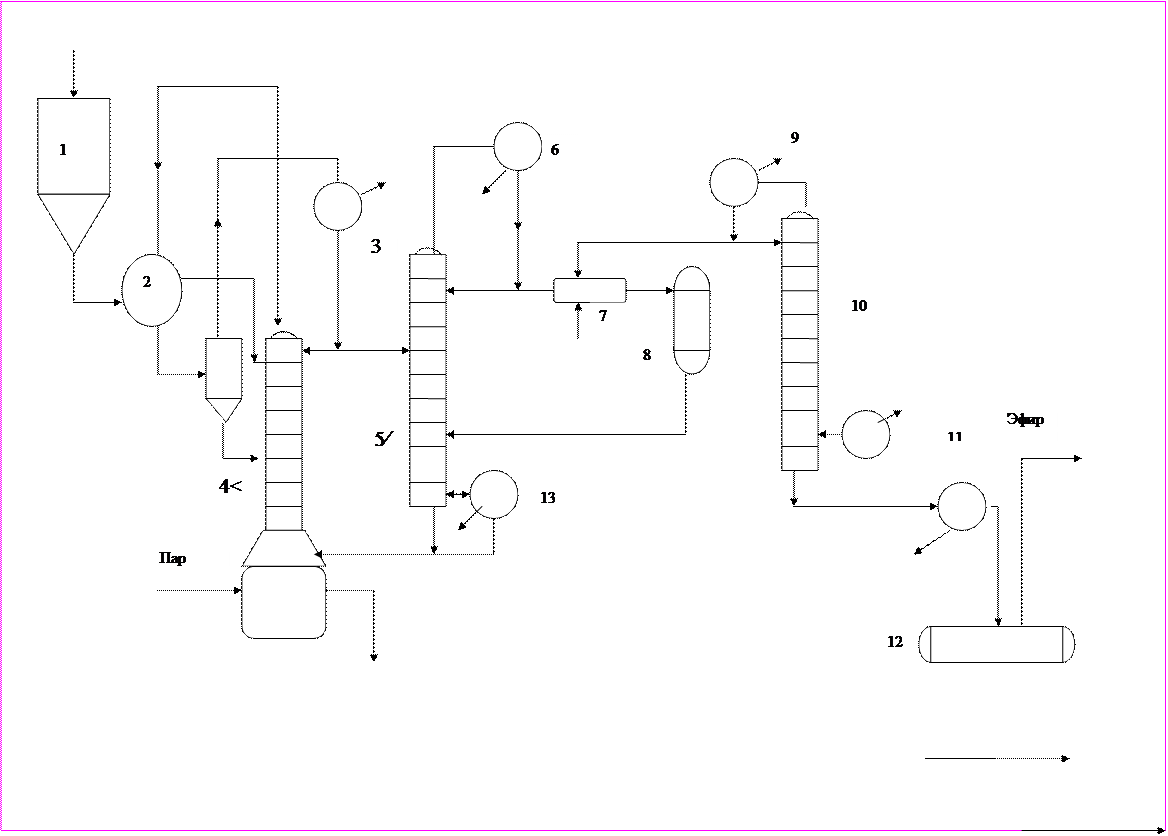
37.Сурет.Үздіксіз этилацетат өндірісінің техникалық схемасы.
1-напорлы бак;2-жылу алмастырғыш;3-конденсатор;4-эфиризатор;5,10-ректификациялық колонналар;6,9-дефлегматор-конденсаторлар;7-араластырғыш;8-сеператор;11-тоңазыт
Лекция 10
Олефиндер мен ацетиленнің гидротациялануы
Олефиннің гидротациялануынан көптеген өнімдер алынады.
Этанол С2Н5ОН – 78,30С-да қайнайтын,ауамен қоспасы 3-20% концентрациялық аралықта жарылғыш,сұйықтық болып келеді.Сумен ұоспасы 78,10С қайнайтын 95,6% спирттен тұратын азеотропты қоспа береді.Этанолдың бұндай ректификаты әдетте техникада қолданылады.Этанол органикалық синтезде кең қолданылатын өнімге жатады.Ол жақсы бірақ қте қауіпті ерітінді,көп жағдайда тағамдық және медициналық шаруашылықта,сұйық ракеталық двигателдерде қайнатқыш ретінде,антифриз ретінде және т.б қолданылады.Органикалық синтезде аралық өнім ретінде этанол,күрделі зфирлер,хлороформ,хлраль,диэтил эфирі,ацетальдегид қолданылады.Сірке қышқылын алуда негізгі арлық өнім этанол болып табылады.Соңғы уақытқа дейін этанолды алудың негізгі көзі-крахмал,картоп болды.
(С6Н10О5)x+xH2O→xC6H12O5 C6H12O6+H-→2C2H5OH+2CO2
Синтетикалық этанолды этиленді гидратациялап алады.
қолданылады,бірақ оның кемшілігі жоғары өртқауіптілік қасиеті.Диэтил эфирінің шектеулі мөлшері медицинада қолданылады.
2С2Н5ОН→(С2Н5)2O+H2O
Изопропонол СН3СНОНСН3 – сумен араласқан сұйықтық (қайнау температурасы 82,50С) оның буы ауамен қоспасында 2-12% концентрацияда жарылғыш қауіпті.Сумен қоспасы 88% спирттен тұратын азеотропты қоспа және 80,30С-та қайнайды.Изопропонол еріткіш ретінде көп жағдайда этанолды ауыстырушы болады.Сонымен бірге одан көптеген күрделі эфирлер және ацетон т.б алады,және ол синтетикалық жолмен дәлірек пропиленнің гидротациясымен жүреді.
Этилен мен пропиленнің күкірт қышқылымен абсорбциясы 2 типті аппаратта орындалады.Біріншісі (31сурет,а) валды дискісі көп арластырғышы бар көлденең абсорбер болып табылады.Абсорбердің ішкі кеңістігінің1/3 шамамен Н2SO4 толған,ол диск айналған кезде тұман түзеді және бұл фазаның контактсын жоғарылатады.Реакция жылуын циркулирленген рубашкеде сумен жояды.Бұл аппарат периодты жұмыс жасайды,бірақ абсорберлердің каскадын қолдану үздіксіз процеске айналдырады.
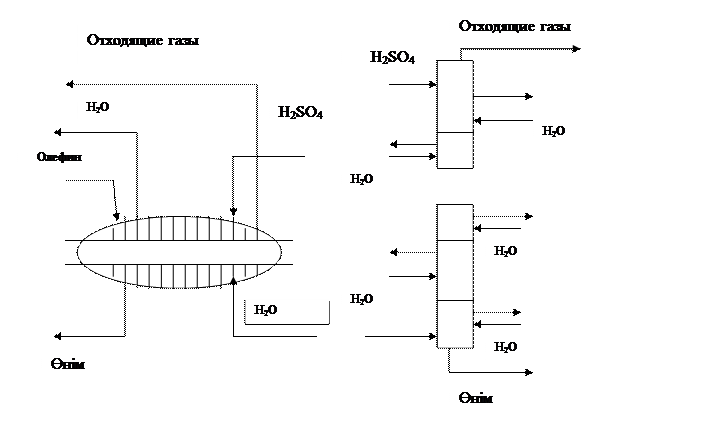
Прогресивті үздіксіз жұмыс жасайтын колонна тәрізді 20-25 қалпақшалы тәрелкеде жоғары дәрежелі сұйықтығы бар аппарат(31сурет,б) әр тарелкедегі сұйықтық қабатында трубалық тоңазытқыш орналасқан,ол шығатын жылуды салқын су арқылы қамтамасыз етеді.Колоннаның жоғары тарелкасына керекті концентрациялы жаңа күкірт қышқылы жіберіледі.Ол кубтан берілген құрамдағы реакциялық массадан шығады.
Бірінші сатыда алынған реакциялық масса сулфаттардың гидролиздену сатысына түседі.Сұйықтықты сумен араластырып,қатты буда ысытады.Оларды суытып бөліп,90% шығыммен спирт алады.Гидролизден қалған күкірт қышқылының концентрациясы 40-50% болады.Оны амонисулфатын алу үшін қолданады немесе абсорбцияға қайтару үшін коцентрлейді.
Этанол өндірісі. Реагенттің конверция дәрежесінің төмендігінен,жоғары температурада және этиленнің тура гидротациясының қысымы заттардың айналуы және энергия экономиясы туралы сұрақтарға негізгі мән береді.Берілген процесс схемалары бір-бірінен синтез және барлық өнімді жуу дәрежесі үшін керекті су буының шығуына байланысты ерекшеледі.Сәйкес параметрлердегі су буын жиірек басқа жақтан немесе осы қондырғының трубалық пешінде алады. Соңғы жағдайда техникалық судың су айналымын ұйымдаастыруға болады.Бұндай процесс схемасы 32 суретте көрсетілген.
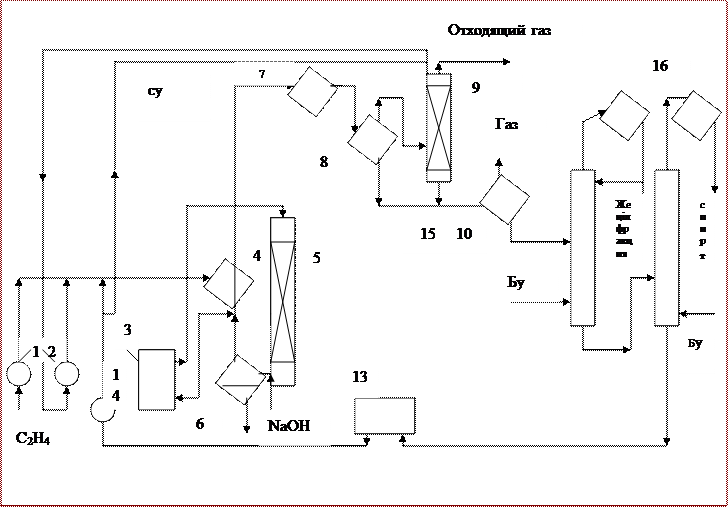
Жаңа этанол компрессорды 1 8МПа-ға дейін төмендетеді және айналдырғыш компрессорда 2 сулы конденсатпен араластырады және жылу алмастырғышта 4 ыстық реакциялық газдармен қыздырады.Сосын қоспаны қосымша трубалық пеште 3 280-3300С-қа дейін қыздырып,реакторға 5 жібереді.
Фосфор қышқылынан тұратын реакциялық газдарды алдымен NaOH-тың сулы ерітіндісінде бейтараптайды.Түзілген фосфорды мұз бөлгіште 6 бөліп алады.Газ жылу алмастырғышқа 4 пайдаланады.Сулы тоңазытқышта 7 қосымша салқындатқаннан кейін, сеператор 8 арқылы жоғары қысымда сұйық және газ фазаларды бір-бірінен айырады.Газ әлі абсорберде 9 сумен ұсталып қалатын спирт буларынан құралады.Спирттен босаған газ компрессор көмегімен айналады,бірақ оны көп инертті қоспаның жинақталуымен құтылу үшін отынды газ жолына тастайды.Сеператордан 8 кейінгі сулы конденсатты және абсорбердегі 9 Сұйықтыты дроссерлеп,төменгі қысымды сеператор 10 арқылы отын ретінде қолданатын газды ерітінділерді бөліп алады.Сеператордан 10 диэтилэфир,ацетальдегид және төмен молекулалы этилен полимерінен тұратын 15%-тік этонолдың сулы ерітіндісі ағып шығады. Бұл ерітінді 11 және 12 колонналарға тазарту үшін салынаы.Біріншісінде ұшқыш диэтилэфирін жіне ацетальдегидті айдайды.Куб колоннасында 12 ионалмастырғышты 13 тазарту үшін.этилен гидротациясын ұйымдастыру үшін су қалады.
Карбон қышқылдарының дегидратациясы. Бұл процесс басқа дегидратация реакцияларына қарағанда ерекше жағдайда жүреді.Осы жағдайда ішкі және молекулааралық дегидратация нәтижесіде өнім ретінде кетен және сірке ангидриді табылады.
CH3-COOH→CH2=C=O+H2O
2CH3-COOH→(CH3CO)2O+ H2O
Бұл реакциялар экзотермиялық және олардың тепе-теңдігі ангидрид түзген кезде 500-6000С-та, ал кетен түзген кезде 7000С-та оңға ығысады.кетен түзген кезде тепе-теңдіктің тура бағытқа ығысуына төменгі қысымда әсер етеді.Екі реакцияда қышқыл типті гетерогенді катализатор немесе бөлінген қоспаға қышқылда жеңілгидролизденетін
эфир түрінде қосуға болатын фосфор қышқылының булары қатысында жүреді.Реакция механизмін жалпы басқа дегидратация процестеріне қолдануға болады.
CH3-COOH→ CH3-COOH+ +Н-→ CH2-C+=O + H2O-
CH2=C=O→ CH2-C+=O+ CH3-COOH →(CH3CO)2O+ H2O
Кетен- 410С температурада сұйықтыққа конденсирленетін,өткір иісті газ.Жоғары әрекеттесушілік қабілеті бар,сірке қышқылы және оның туындыларымен әрекеттеседі.Көбіне сірке қышқылымен әрекеттесіп,сірке ангидридін береді.
CH2=C=O→CH3-COOH →(CH3CO)2O+ H2O
Сірке ангидриді өткір иісті сұйықтық,қайнау температурасы 1410С.Ол органикалық синтездің маңызды өнімі болып табылады.Қиын жолмен алынатын –фенол ацеттары үшіншілік спирт ацеттарының,соның ішінде целлюлоза және волокн ацетаттары сонымен қатар,сірке қышқылының эфирінің синтезі кезінде ацетирлеуші зат ретінде кеңінен қолданылады.Сірке ангидридін бұрын сульфурил хлоридпен натрий ацетатынан хлор әдісі бойынша бөліп алады.
SO2Cl2 +4CH3COONa→2(CH3CO)2O+Na2SO4+NaCl
Процесс технологиясы. Дегидратация процесі екі әдіспен орындалады:сұйық және газ фазада.
Газ фазалы процестің температурасын жоғарлатқанда өнім мен бөлінетін реагенттің тұрақтылығы жеткіліксіз болса,сұйық фазалы дегидратация қолданылады.Бұл хлорекс,диоксан,морфолан синтезіне жатады,бірақ сұйық фазаға сәйкес қанықпаған заттарды нитроспирттер,гидроксиальдегидтер және гидроксикетондарды газ фазасында да жиі дегидратациялауға болады.Катализатор ретінде күкірт қышқылын (70%концентрлі),фосфор қышқылы,кальций фосфаты немесе магний сульфакатионы болып табылады.Процесті 100 0С-тан 160-2000С-қа дейінгі температурада және қарапайым қысымда жүргізеді.
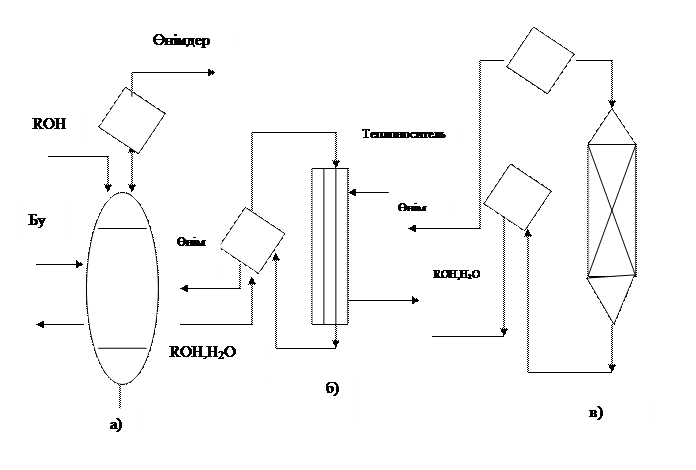
Сұйық фазалы дегидротацияны (35а суретте) көбіне үздіксіз екі әдіспен жүзеге асырады.Олардығң ішінен бірі болып бұл процесті бүтін қанықпаған зат немесе жай эфир және суда жеңіл қайнайтын азеотропты қоспа беретін катализаторлы ерітіндіні қолданбай-ақ үздісіз жүргізеді.Ректорды бумен қыздырып және аппаратқа үздіксіз бөлінетін органикалық реагент салады.Реактордың үстінде конденсатор орналасқан,оның көмегімен катализатор концентрацияны тұрақты ұстап,конденсат қайтымдылығын қалыпына келтіреді.
Екінші әдісті нитроолефиндер, қанықпаған альдегид, және кетон және тағы басқа заттар түзетін жылдам,жеткілікті суды бөлу реакциясына және қайтымсыз тәжірибелік зерттеулерде қолданады.Ол трубалық реакторда төмен температурада жүргізуге негізделген.
Лекция 11
Химиялық реакция жылдамдағына әсер ететін шарттар
Химиялық реакция жылдамдыға әсер ететін шарт жағдайлар мыналар мұнда ең бастысы әрекеттесетін заттардың табиғатына байлансты. Мұнан сыртай еттесетін заттардың концентрациясы, қысым, температура, катализатор, ортаның әсері бөліп табылады. Әдетте температура өскен сайын химиялық реакция жылдамдығы артады. Температура өскенде Реакция жылдамдығының кемуі өте сирек кездеседі. Температура өскенде реакцияға қатынасқан зат молекуласының энергиясы артып, нәтижесінде энергиясы төмендеу бір бөлім молекула активтенген молекулаға айналатындықтан, реакцияға қатынасқан зат молекуласындағы активтенген молекуланың проценті артып, өнімді соқтығысудың саны көбейеді де химиялық реакция жылдамдығы артады. Вант – Гофф ережесі төмен температураларда ертінділерде өтетін процестер үшін ғана анықталған жуық ереже температура өскен сайын тұрақты болып қалмайды, ол кеміп, мәні бірге жақындайды реакция жылдамдығына температураның әсерін Вант – Гофф ережесіне қарағанда дәлрек көрсететін Аррениус теңдеуі
Температураның реакция жылдамдығына әсері
Әдетте температура өскен сайын химиялық реакция жылдамдығы артады. Температура өскенде реакция жылдамдығының кемуі өте сирек кездеседі.
Реакция жылдамдығы кинетиканың негізгі заңы бойынша мына формуламен анықталады﹕ W﹦K﹒Cn1A﹒Cn2B
Осыдан температураның жылдамдыққа әсері консентрацияның немесе дәреже көрсеткіштің, немесе жылдамдық константасының К өзгеруімен байлансты деуге болады. Температураның реакция жылдамдығына әсерін қарастырғанда, оның жылдамдық константасына әсері болатынын есте ұстауымыз қажет.
Реакцияның Т + 10 градус температурадағы константасының жылдамдықтың температуралық коэффициенті γ деп аталады.
γ﹦КТ+10 / KT
Температуралық коэффициентінің практика жүзінде анықталған мәні екі мен төрттің арасында жатады, яғни температураны әрбір 10 градусқа көтергенде химиялық реакцияның жылдамдығы 2-4 есе өседі. Бұл Вант – Гофф ережесі деп аталады.
Вант – Гофф ережесі төмен температураларда ертінділерде өтетін процестер үшін ғана анықталған жуық ереже температура өскен сайын тұрақты болып қалмайды, ол кеміп, мәні бірге жақындайды реакция жылдамдығына температураның әсерін Вант – Гофф ережесіне қарағанда дәлірек көрсететін Аррениус теңдеуі﹕
lnk = -B/ T + C
мұндағы В және С зерттелетін реакцияға тән, температураға тәуелсіз тұрақты шамалар.
Температура өскенде реакцияға қатынасқан зат молекуласының энергиясы артып, нәтижесінде энергиясы төмендеу бір бөлім молекула активтенген молекулаға айналатындықтан, реакцияға қатынасқан зат молекуласындағы активтенген молекуланың проценті артып, өнімді соқтығысудың саны көбейеді де химиялық реакция жылдамдығы артады.
Қысымның химиялық реакция жылдамдығына әсері
Газдар жөнінен айтқанда, температура тұрақты болғанда белгілі мөлшердегі газдың өзіне түскен қысымға кері пропорционал болады. Атап айтқанда, егер газдың қысымы бұрынғыдан екі есе артса, газдың көлемі кішірейіп, бұрынғы көлемнің жартысындай болады. Бірлік көлемдегі молекула саны бұрынғыдан екі есе көбейеді. Сондықтан қысым артса, бірлік көлемдегі реакцияға қатынасқан заттың концентрациясы артқандықтан химиялық реакция жылдамдығы артады. Керісінше қысым кемісе, газдың көлемі ұлғайып, концентрациясы төмендейтіндіктен химиялық реакция жылдамдығы да кемиді.
Егер реакцияға қатынасқан зат қатты зат, сұйықтық немесе ерітінді болса, оларға қысымның әсері аз болады. Реакция жылдамдығы өзгермейді деп қарауға болады
Лекция 12
Спирттердің гидрогалгенденуі – ОН-тобының хлор немесе бром атомдарына араласуынан тұрады Ол спирттерге HCL (HBr) әсерінен, экзотермиялық реакция жүреді.
СН3ОН+НХ↔СН3Х+Н2 О
Үшіншілік, екіншілік және жоғары біріншілік спирттер жағдайында, реакцианы сұйық фазада катализатор қатысынсыз,тепе-теңдік судың немесе хлор туындысының айрылуынан жүреді.Реакция механизмі ОН-тобының келесі нуклеофильді араласуынан тұрады.
ROH + HX ↔ ROH2 +X- → RX + H2O
Басқа жағдайларда әсіресе төменгі біріншілік спирттерде,кейде судың әкету ролін атқаратын тепе-теңдікті оңға ығыстыратын катализаторлар керек етіледі.Этилбромиді алыну үшін Н2SO4(конц) қолданылады. Ол бір мезгізгілде НBr-ды NaBr-нен генерирлейді.
С2Н5ОН+NaBr+H2SO4→ C2H5Br+NaHSO4+H2O
Сұйық фазалы процестер үшін кейде ZnCL2 тұз қышқылындағы қаныққан ерітіндісі,газ фазалы процестерде ZnCL2 ұсақ таратушылары қолданылады.ZnCL2 ролі апротонды қышқыл сияқты спирт молекулаларын белсенділеуден немесе күшті қышқыл H2ZnCL4-ң спирт түзіуінен тұрады.
R
> O: ZnCL2
R
Спирттердің гидрохлорлануынан алынған көптоннажды өнім – хлорметан СН3CL.Оны сусыз HCL және газ фазадағы метанолдың гетерогенді катализатормен 200-3500С температурасында тепе-теңдік HCL артық (20-50%)жағына жылжуымен алады.Реакцияны қозғалмайтын гетерогенді катализаторлы қабаттытрубалық немесе адиабаталық реакторда жүргізеді.Өзгергіштік реогенттен СН3CL.Н2Ожәне қосымша диметил эфирінен тұратын реакция өнімін салқындатады:бұл кезде тұз қышқылы мен метанол сұйықтыққа айналады.Соңғысы айдап және реакцияға кері қайтарады.Газ тәрізді қоспаны СН3ОН мен НCL-дан сумен және сулы сілтімен тазартады.Сосын хлорметанды диметил эфирінен концентрлі күкірт қышқылымен тазартып,нейтралдап,кептіреді және қысымда конденсирлейді.Хлорметанның синтезі үшін бұл әдіс метанның хлорлануынан басымырақ және экономикалық тиімдірек.
Бірінші(1) 55-650С салқындатуды ұстайтын колоннаға спирт және тұз қышқылының хлормен 2 сатыдағы қоспаны жібереді.Хлорацетальалдегид олардың ацетолдары мен жартылай ацетолдарынан тұратын сұйық қоспаны 2-ші 900С-та жұмыс жасайтын сумен хлор жіберілетін калоннаға ағызады.Суды белгілеу – спирттің толық қолданылуын қамтамасыз ететін ацетол гидролизінен болады.
Екіншілік калоннадан шыққан өнім – хлоральгидрат,жартылай ацетол хлориді,және дихлорацетальдегидтің қоспасынан тұрады.Оны концентрлі H2SO4-да гидраттары мен
ССL3CH(OH)2 +H2SO4→ CH3CHO+H2SO4+H2O
Хлоральды күкірт қышқылынан тұндырады және қайтадан айдап, дихлорацетальдегид хлорлануынан тұратын жеңіл фракцияны алады.Алынған өнім 97-98% тазалықта болады.
Сl2
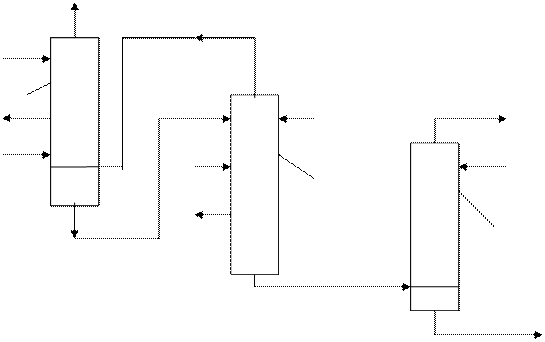
 3
3
H2SO4
Cурет1.Хлораль алуға арналған реакциялық тізбек.
1,2-реакциялық колонналар.3-жуғыш колонна.
Қышқыл туындыларының синтезі. Алифатты қатардағы хлор карбонды қышқылдарды әдетте карбонды қышқылдардың хлорлануымен алады. Бұл реакция карбонды қышқылдармен ангидридтер және хлорангидридтер беруге қабілетті,катализатор болып табылатын заттармен катализденеді.Олардың әсіресе хлорангидридридтердің хлормен тез жеткілікті өзара әрекеттесуінен түсіндіріледі және ангидридтің пайда болуымен айрылуы нәтижесінде хлоркарбонды қышқыл түзіледі.
CH3-COCL+CL2→CLCH2+HCL+CH3COOH↔CLCH2-CO-O-CO- CH3+HCL↔CLCH2-COOH+CH3-COCL
Реакция жүйелі өнімнің көміртек атомына көршілеш корбоксил тобымен орын басуы пайда болуымен қабаттаса жүреді.
CH3COOH+CL2↔CH2CLCOOH+CL2↔CHCL2COOH+CL2↔CCL3COOH
CH3CH2COOH+CL2↔CH3CHCLCOOH+CL2↔CH3CCL2COOH+HCL
Тотықтыру арқылы хлорлау. Бұл процесс негізіне белгілі Дикон реакциясы жатады.
2HCL+5O2→H2O+CL2 -∆H0298=43,5кДж∕моль
Экзотермиялық реакция болғандықтан оның температурасын төмендеткенде тепе-теңдік оңға ығысады,бірақ әзірге белгілі катализаторлар СиСL2 негізінде тек 200-40000С-да жұмыс істеуге мүмкіндік береді.Бұл жағдайда хлорлану процестері өтеді,ал екі процесс бір аппаратта жүрсе HCL және О2 көмегімен бастапқы қалпына келмейтін хлорлы тотықтыру болады.
RH+HCL+0.5O2→RCL+H2O
Негізгі реакциядан басқа, қосымша көмірсутектердің тотығуы, хлортуындылардың сулы буда гидролизденуі,гидрохлорлау жүреді.Осы себепті процесті тек қана тұрақты негізгі заттар үшін қолданады.Оларға метан, этилен,бензол аз дәрежеде этан жатады.Бірінші рет оны бензолдың хлорланып тотығу арқылы фенол алуда қолданды,бірақ бұл өзінің мағынасын жоғалтты.Тек сонғы уқытта бұл әдіс төменгі ароматты хлор туындыларының синтезі үшін қолданыла бастады.
Метанның хлорланып тотыгуында реагенттердің қатынасымен әртүрлі құрамды қоспа алынады да тек орын басу реакциясы жүреді(CH2CL2,CHCL3,CCL4).Бұл кезде метанның оксихлоридпен тура хлорлануы түзілген HCL қатысында комбинирленіп нәтижесінде хлор толығымен қолданылады.Мысалы:
CH4+4CL2→CCL4+HCL; CH4+4HCL-2O2→CCL4+4H2O
210-2800C этиленді хлорлап тотықтырғанда орын басу емес,хлордың екі байланыспен қосылуы жүреді.Бұл жағдайда хлорлануға хлорды емес,HCL және О2-нің әсерінен регенерирленетін СиCL2-не қолдану керек.
CH2=CH2+2CuCL2→CLCH2-CH2CL+Cu2CL
Cu2CL2+2HCL+0.5O2→2CuCL2+H2O
Процестің негізгі ерекшелігі реакторға жылу алмасуды ұйымдастыруы жоғарғы экзотемиялықында.Көбіне жалған сұйылған катализаторлы реакторлар қолданылады:оларға салқын реагенттер түседі,ал артық жылуды ішкі жылу алмастырғыштан алады,және статционарлы қабатты реакторлар қолданылады.Оларды ацителенді гидрохлорлауда суреттелген,қабтамалы құбырлы аппараттарда қолданады.
|
|
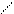
 ….ГАЗ РЕЦИКЛ
….ГАЗ РЕЦИКЛ 
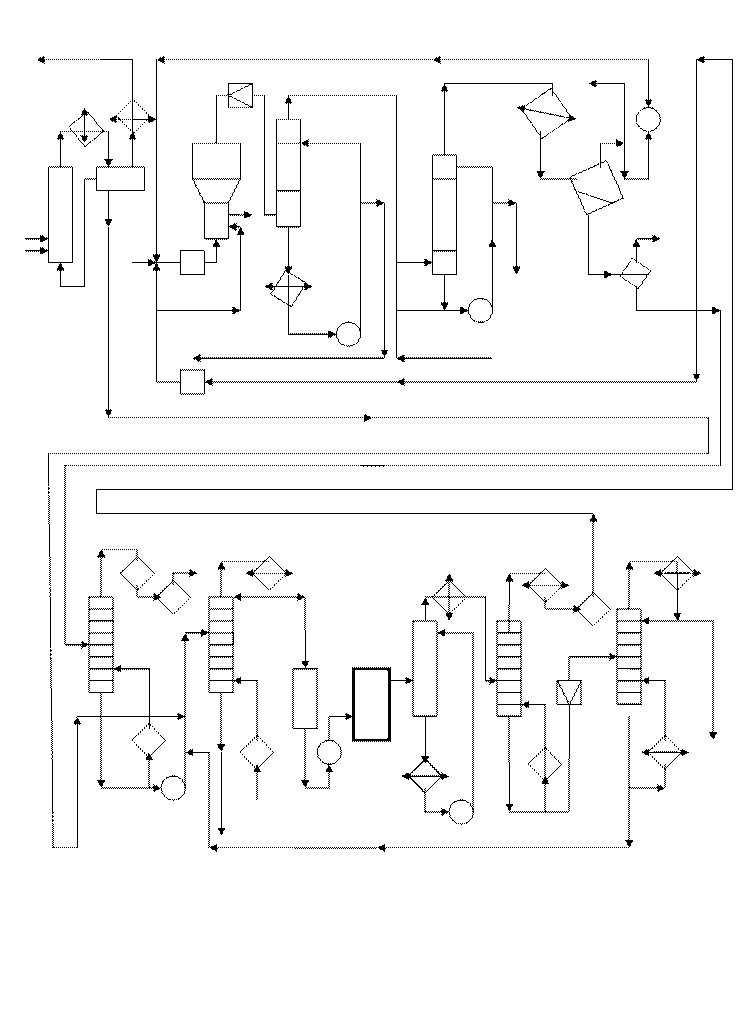
Сурет20.Комбинирлі әдіспен винвлхлориді синтезінің техникалық схемасы.
1-хлоратор2-конденсатор тоңазытқыш,3-жинақ,4,5-реактор,6,20-үздіксіз араластыратын тоңазтқыш, 7,10-тоңазтқыштар,8-айналдырғыш, насос,9-скруббер, 11,12-сеператорлар,13-компрессор,14-жүзеге асыратын колонна,15-су қайнатқыш, 16,21,22-ректификациялық колонналар, 17-сыйымдылық,18-насос,19-трубалық пеш,23-дросселді вентиль.
Көміртектің хлортуындыларын көп арзандату мақсатында шикі зат ретінде этан немесе оның этиленмен қоспасы алынады.Басқа әдістер конбинерлеуге немесе тура және тотықтыру арқылы хлорлауға,тұз қышқылын бөліп алуға және басқа реакциялармен қосылып жүруге негізделген.Бір өндірісте жүзеге асырылатын процесс(21-сурет) реакторда этанды тура хлорлау және тұз қышқылын хлортуындыларынан бөліп алу қосарланып жүреді.Қондырғыда 2 өнімнен бірінші сатыда мақсатты хлоролифендер(винилхлорид және винилиденхлорид) шығады,ал қалған зат этанға айналмаған этилен және тұз қышқылын реакторына бағытталады.Мұнда ауадан ажыратылмаған хлорэтан аынады,және реакторға қайтарылады.Процесс винилхлоридті өндірістік метилхлороформ және барлық мақсатсыз хлорорганикалық заттар три және тетрахлорэтиленді тотықтыру арқылы хлорлауды гидрохлорлап комбинерлейді.

21Сурет.Этанның немесе оның этиленмен қоспасының комбинерлі қайта өңдеу блох-схемасы.
1-термиялық хлорлау немесе дегиидрохлорлау,2-ректификация,3-тотықтыру арқылы хлорлау,4-гидрохлорлау,5-тотықтыру арқылы хлорлау немесе дегидрохлорлау.
Лекция 13
Химиялық рекцияның кинетикалық параметрлері
Химиялық реакцияның кинетикалық параметрлері
жылдамдық константасы, меншіктік жылдамдық, активтену
энергиясы оньң жүру механизмімен тығыз байланысты. Бұл
кинетикалық параметрлердің термодинамикалық функциялардан (энтальпия, энтропия жэне Гиббс энергиясыньң өзгерістері) басты айырмашылығы болып табылады. Химиялық реакциялардьң барлығы дерлік, оның ішінде гетерогенді реакциялар, күрделі механизмімен өтетіні белгілі.
Жылдамдыққа әсер факторлардың бipeyi ғана өзгеріп, басқалары тұрақты болған жағдайда кинетикалық параметрлерді анықтау жеңілірек. Кинетикалық тәжірибені одан әpi жеделдету үшін ұнтақталған минералдық формасы және көлемі жағынан бірдей түрлерін зерттеген дұрыс. Егер epiткiш минералға қарағанда көп мөлшерде алынған болса,(ергіштің мөлшері стехиометрлік мөлшерінен кемінде он есе артық болуы қажет) жылдамдық константа және жылдамдық параметрлерін тәжірибеден анықтау үшін формальді кинетиканың тесттері қолданылады. Бұл жағдайда реакция барысында epiткiш концентрациясының өзгepici өте болмашы болатындықтан оны елемеуге болады. Сонда еру жылдамдығының epiткiш концентрациясына тәуелдігінің түpi (егер реакцияның peті бipгe тең болса) диффузиялық режим деп тәуелдікке ұқсас болады. Процестердің кинетикалық параметрлерін яғни жылдамдық константасын, меншікті жылдамдығын және активтену энергиясын есептеудің практикалық және теориялық маңызы өте зор.
Дистиллятты майларды өндіру
Әр түрлі мақсаттарда қолданылатын минералды мұнай майларын мазуттарды атмосфералық айдау қалдықтарынан алады.Кез келген майды өндіру процесі 3 кезеңнен тұрады:1) шикізатты дайындау – бастапқы майлы фракцияларды алу; 2) бастапқы майлы фракциялардан компоненттерді алу; 3) компоненттерді араластыру және майлардың тауарлық маркаларын алу үшін қоспалар қосу.
Шикізатты дайындау кезінде мазуттарды вакуумде айдайды.Майларды өндіру үшін пайдаланылатын фракцияларды алыну әдістеріне қарай екі топқа бөледі:дистилляттық – мазутты вакуумды айдау кезінде бөлінетін айдандылар (300-400 °С,360-420 °С,420-450 °С) және қалдық – мазуттың вакуумдық айдау қалдығы,яғни гудрон (500° С жоғары).Осыған сәйкес,дистилляттық майлы фракцияларды өңдеу кезінде алынатын майларды – дистилляттық майлар,ал гудроннан алынатын майларды – қалдық майлар деп атайды.
Бастапқы майлы фракциялардан алынатын компоненттерді өндіру – күрделі де,көп сатылы процесс.Әрбір сатының негізгі мақсаты майлардың тұтынушылық қасиеттеріне теріс әсер ететін қосылыстардың белгілі бір топтарынан толық немесе жартылай тазарту. Мұнайлы фракциялардан барлық қышқылдық қосылыстарды,қанықпаған көмірсутектерді,ішінара күкіртті және шайырлы қосылыстарды,қысқа бүйір тізбектері бар полициклді ароматты көмірсутектерді,қатты парафиндерді бөліп алып тастау қажет.
Бастапқы майлы фракциялардан майлардың компоненттерін өндіру негізіне жоғарыда көрсетілген қажетсіз компоненттерді таңдамалы тазарту әдістері жатады.Бұл әдістер физикалық – еріткіштермен экстракциялау,температура төмендегенде ерітіндіден тұнбаға түсіру;физика-химиялық – адсорбция;химиялық – күкірт қышқылымен әрекеттестіру,гидротазалау болуы мүмкін.
Гудронда шайырлы-асфальтенді заттардың мөлшерінің көп болуына байланысты дистиллятты майларды өндіруге қарағанда қалдық майларды өндіру күрделі болып саналады.Вакуумдық айдау кезінде алынған гудронды ең алдымен деасфальтизациялайды,яғни құрамындағы шайырлы-асфальтенді заттарды бөліп тастайды. Деасфальтизат таңдамалы еріткіштер фенол немесе фурфуролмен тазалауға жіберіледі.Таңдамалы тазалау мақсаты – қалдық шайырлы-асфальтенді заттардан және қысқа бүйір тізбектері бар полициклді ароматты көмірсутектерден тазарту болып табылады.Деасфальттау және таңдамалы тазарту орнына жұп еріткіштермен тазалауды қолдануға болады.
Таңдамалы тазалау рафинатынан ацетон,дихлорэтан және т.б. сияқты таңдамалы еріткіштер көмегімен қатты парафиндерді тұнбаға түсіруге болады.Парафинсіздендіру өнімін аяғына дейін адсорбциялау немесе гидротазалау жолымен кондицияға келтіреді.
Дистиллятты майлы фракцияларды,әдетте деасфальттаудың қажеті жоқ.Дистиллятты және қалдық майларды өндірудің қалған жалпы сұлбасы ұқсас.
Жоғары сапалы майларды сонымен қатар,майларды депарафиндеудің жанама өнімдері – парафиндер мен гачтарды гидроизомерлеу арқылы да алуға болады.
Майлы фракцияларды шайырлы заттардан тазалау нәтижесінде майлардың түсі өзгеріп,олар түссіз бола алады.Шайырлы заттардан және қысқа тізбектері бар полициклді ароматты көмірсутектерден тазалау майлардың кокстелуінің кемуіне және тұтқырлық индексінің артуына жағдай жасайды.Шайырлы заттардан және қанықпаған көмірсутектерден тазарту майлардың айтарлықтай термототығуға тұрақтылығын арттырады.Қышқылдық қосылыстардан тазарту коррозиялық активтілігін төмендетеді,ал майлардың құрамынан қатты көмірсутектерді бөлу қату температурасының төмендеуіне алып келеді.Майларды өндірудің технологиялық процестерінің тиімділігі майлардың қажетті сапалық көрсеткіштеріне жетумен және сонымен бірге,мақсатты өнім шығымымен сипатталады.
Тауарлық маркадағы майларды жеке компоненттерге қоспалар қосу арқылы араластырып дайындайды.Мысалы, тауарлық майлардың төрт маркасын үш компоненттен алуға болады:
1-компонент 2-компонент 3-компонент
(350-420°С) (420-500°С) (500°С жоғ.)
Тұтқырлығы,мм2/с
50°С кезінде............ 14,4 42,1 -
100°С кезінде.......... 4 7,5-8,1 22-24
Тұтқырлық индексі.. 87 83 84
Қату температ.,°С.... -30 -30 -23
Бұл компоненттерден алынатын тауарлық майлардың құрамы % (масс.)
1-компонент 2-компонент 3-компонент
Автотрактор майы
АС-6........................42 68 -
АС-10.......................- 70 30
Авиамай МС-20......- 12 88
Ұршықты 2..............100 - -
Тауарлық майларды дайындау компаундирлеу қондырғысында жүзеге асырылады.Егер жеңіл,орташа және ауыр дистиллятты,сонымен бірге қалдық компоненттер болса,онда майдың кез келген сорттарын дайындауға болады.Компоненттердің ара қатынастарын мұнай өнімдері қоспасының тұтқырлығы компоненттердің тұтқырлығына және соңғы тауарлық майдың тұтқырлығына байланысты анықтауға арналған номограмма бойынша анықтайды.Әрбір жеке жағдайларда,компоненттердің ара қатынасы дайын майдың лабораториялық анализдеріне сәйкес дәлденеді.
Лекция 14-15
Парафинді таңдамалы еріткіштер қолдану арқылы майсыздандыру.
Таңдамалы еріткіштерді қолдану арқылы гачтар мнен петролатумдарды майсыздандырудың үздіксіз процесі майларды парафинсіздендіру процесіне ұқсас.Айырмашылық тек температуралық режимде болады.Төменде өнімділігі 260 т/тәулік болатын парафинді майсыздандыру қондырғысы жұмысының режимі келтірілген:
Ара қатынасы
еріткіш:сүзгілеуден бұрынғы шикізат (4,5-5):1
еріткіш:I сатыдағы парафин.........................4:1
Температура,°С
ерітінді..............................................................80
сүзгілеу..............................................................
I сатыдағы........................................................0-1
II сатыдағы.......................................................5-6
Ерітінді қысымы,МПа....................................1,2
Гачты майсыздандыру қондырғысының материалдық балансы [%(масс.)]
Түскен Алынған
Гач......................100 Парафин ерітіндісі
Еріткіш...............500 парафин тазартылған....56
еріткіш...........................132
Май ерітіндісі
Барлығы...600 май қалдықтары............44
еріткіш.........................368
Барлығы............................600
Майлардың парафинсізденуі мен гачтың майсыздану процестері көбінесе бір қондырғыда жүргізіледі.Майларды парафинсіздендіру қондырғысының I саты сүзгісінде гачты алғаннан соң,оны II және III саты сүзгілерінде майсыздандыруға жібереді.Майларды парафинсіздендіру мен гачтарды майсыздандыру процесін құрамдастыру еріткіштерді регенерациялаудың бір бөлімін ғана жасауға,құрал-жабдықтар мен қызмет көрсетушілердің санын азайтуға мүмкіндік береді.
Майсызданған шикі парафин түсі,иісі,ароматты көмірсутектер мен шайырлы заттарының мөлшері боынша ГОСТ талаптарын қанағаттандырмайды,сондықтан да оны келесі әдістердің бірімен қосымша тазалау қажет:
1) күкірт қышқылдық тазалау,оны одан ары қарай ағартқыш топырақтармен перколяция әдісімен тазалайды;
2) алюмосиликатты катализатор ұнтағында үздіксіз адсорбциялық тазалау;
3) 4 МПа қысым мен 330ºC температура кезінде алюмокобальтмолибден катализаторында гидротазалау.
Тауарлық парафин сапасын жақсарту үшін қоспалар қолданады,мысалы полиэтилендік балауыз.
Дайын парафинді (сұйық,сіріңкелік) арнайы формалағыш машиналардың плиталарына құйған соң,темір жол цистерналары арқылы немесе қағаз қаптарда тасымалдайды.Парафинді автоматты құю және буып-түю линиясы болады.
Пластикалық майлағыштар
Көп жылдар бойы машиналар мен механизмдердегі үйкеліс пен тозуды азайту үшін,сонымен қатар,металдарды коррозиядан қорғау үшін пластикалық майлағыштарды қолданып келеді.Біздің эрамызға дейінгі 3400 жылдардың өзінде ежелгі Египетте қоюланған майлағыштарды қолданғаны белгілі болған.Бірақ та,тек соңғы жылдары пластикалық майлағыштар өндірісі қарқынды дами бастады және олардың ассортименті айтарлықтай ұлғайды,ал олардың әлемдік өндірісі мен тұтынуы 2-3 есеге дейін өсіп,миллион тоннаға жетті.Бұл әрине,айтарлықтай дәрежеде техниканың дамуы мен оның жаңа салаларының пайда болуымен түсіндіріледі.
Пластикалық майлағыштарға деген ерекше қызығушылық майлағыш майлар жұмыс істей алмайтын,күрделі тұтыну жағдайларында жұмыс жасауға жарамды түрлі қасиеттері бар майлағыш композицияларды алу мүмкіндігімен ынталандырылады.Мұндай жағдайларға жоғары динамикалық жүктемесі бар (тісті және шынжырлы берілісті) немесе үйкеліс түйінінде май тұрмайтын,айналу жылдамдығы жоғары механизмдерді,коррозиялайтын орталарды,вакуумды,сонымен қатар,майлағыш майларды жеткізу қиын механизмдердің жұмысын майлағыштар қамтамасыз етуі тиіс жағдайларды жатқызады.
Пластикалық майлағыштар – мазь тәрізді өнімдер,кәдімгі температуралар кезінде аққыштығы жоқ,майлағыш майларға арнайы,негізінен майлардың аққыштығын шектейтін қатты майда дисперсті қоюландырғыштарды қосу жолымен дайындалатын,майлағыш материалдардың ерекше класы болып табылады.Майлағыштар – қоюландырғыш бөлшектерінен түзілген,кеңістіктік құрылымы бар,коллоидтық жүйелер.Сұйық фаза қатты бөлшектердің тартылыс күші әсерінен жартылай қатты күйде ұсталады,сонымен бірге механикалық түрде қоюландырғыш кристалдардың ішіне кіреді.Электрондық микрофотография,сонымен қатар,рентгеноструктуралық анализ нәтижесінде көпшілік майлағыштардың талшықты құрылымды болатындығы анықталды.Тұрақтандырғыштар (стабилизаторлар) деп аталатын кейбір заттар (су және басқалар) коллоидты құрылымның беріктігін анықтайды.
Майлағыштар дайындау үшін қажетті шикізаттар
Майлағыштарды өндіру үшін сұйық фаза ретінде негізінен мұнай майларын пайдаланады,сонымен қатар,синтетикалық майларды және мұнай мен синтетикалық майлар қоспасын пайдаланады.Синтетикалық майлардан көбінесе,күрделі эфирлерді, полиалкиленгликольдерді,кремнийорганикалық сұйықтарды қолданады.Синтетикалық майлардың кең қолданылуы олардың таптырмайтындығымен және қымбаттылығымен шектеледі. Бензотөзімді майлағыштар үшін сұйық фаза ретінде майсана майы қолданылады.
Пластикалық майлағыштардың қасиеттері қоюландырғыш табиғатына айтарлықтай байланысты болады.Осы белгісі бойынша майлағыштарды 3 негізгі типке бөледі.
1.Қоюландырғыш ретінде қатты заттар болып табылатын,майда балқу температурасына жақын температурада еритін және майлармен балқу температурасы кезінде шын ерітінділер түзетін майлағыштар.Мұндай қоюландырғыштарға қатты көмірсутектер:парафин,церезин,петролатум,балауыз жатады.Негізінен қорғағыш майлағыштар ретінде қолданылатын бұл майлағыштардың пластикалық шегі салыстырмалы түрде аз,қоюландырғыштың балқу температурасы шектелген болып келеді.
2.Қоюландырғыш ретінде қатты заттар қолданылатын, майлармен әрекеттеспейтін,бірақ оларда коллоид түзіп, диспергирленетін майлағыштар.Мұндай қоюландырғыштарға сабын жатады.Бұл типке қазіргі кезде қолданылатын және жасалатын барлық майлағыштардың 85-90%-ы жатады.Сабынның катионына байланысты майлағыштардың бірнеше топтары бар.
Бірнеше топқа сілтілік металдар (Na,Li) сабындарынан дайындалатын майлағыштар жатады.Бұл майлағыштар тіпті қоюландырғыштың жоғары емес концентрацияларында [5-6% (масс.)] да тұрақты.Қоюландырғыш концентрациясына және сабынның органикалық радикалының табиғатына (қаныққан немесе қанықпаған май қышқылдарынан,өсімдік немесе жануар майларынан,синтетикалық май қышқылдарынан) байланысты бұл майлағыштар 100-ден 200ºC-ге дейінгі және одан жоғары температуралар кезінде аққыш күйде болады.Балқығаннан соң және салқындағаннан кейін олар қайта пластикалық құрылымына келеді,яғни олар термиялық қайтымды деген сөз.Литийлік майлағыштар аязға төзімді болады.Натрийлік майлағыштардың кемшілігі олардың суға төзімділігінің нашарлығы болып табылады.
Екінші топқа сілтілік-жер металдар (Ca,Ba) сабындары негізінде дайындалатын майлағыштар жатады.Олар сабынның мөлшері 8-10% (масс.) болған кезде аса тұрақты болады.Егер бұл майлағыштардың негізгі тұрақтандырғышы су болса,онда 100ºC дейін қыздырғанда, олар суды жоғалтып,бұзылады.Мұндай майлағыштың мысалы,кальцийлік майлағыш – солидол болып табылады.Бұл майлағыш суға төзімді,оны ылғал ортада қолдануға болады.
Алюминийлік,қорғасындық және мырышты сабындардан жасалған майлағыштар өте сирек қолданылады.Сабындық майлағыштар негізінен антифрикциялық майлағыштар ретінде,сопымен бірге қорғағыш қасиеттері де бар.
Майлағыштардың қасиеттерін жақсарту үшін бір уақытта сілтілік және сілтілік-жер металдар (Na,Ca) катиондарында дайындалған сабындарды қолдануға болады.Сонымен қатар,құрамында бір түрлі катионы бар жоғары және төмен молекулалық май қышқылдарының комплексті сабындары да қолданылады.Мысалы,комплексті кальцийлік майлағышты минералды майларды стеарин және сірке қышқылдарының кальцийлік сабындарымен қоюландыру арқылы алады.
Қоюландырғыштар ретінде термиялық тұрақты және бейорганикалық өте майланған заттар болып табылатын майлағыштар.Мұндай заттарға мочевина, күйе, слюда, силикагель,күкіртті молибден жатады.Бұл майлағыштар қазіргі уақытта сабындық және көмірсутектік майлағыштарға қарағанда,айтарлықтай қымбат және сабындық майлағыштар қолданылмайтын жағдайларда, мысалы,агрессивті орталарда,қолданылады.
Майлағыштардың сапасы қоюландырғыштың қасиеттері мен концентрациясына,сонымен қатар,қоюландырылатын майдың қасиеттеріне:оның тұтқырлығы мен химиялық құрамына байланысты.Майлағыштардың коллоидтық құрылымының беріктігін тұрақтандырғыштар – су, сілтілер, жоғарғы және төменгі молекулалық органикалық қышқылдар және олардың тұздары,спирттер,эфирлермен жақсартуға болады.Майлағыштардың қасиеттерін жақсарту үшін сонымен қатар,қоспалар да пайдаланылады.
Майлағыштарды өндіру процесі периодты немесе үздіксіз болуы мүмкін.Майлағыштарды көп ассортиментте,бірақ ірі емес партиялармен шығаратын зауыттарға периодты,яғни кезеңді қондырғылары болғаны тиімді;майлағыштардың бір сортын ірі партиялармен өндіруді үздіксіз етіп жасағаны тиімді.
Жұмыс жағдайындағы майлағыштардың жұмыс істеу жағдайы туралы жақсы мәліметтерді құрылымдық-механикалық қасиеттері береді:шекті жылу кернеуі немесе аққыштық шегі – майлағыштың пластикалық деформациясын,яғни оның аққыштығын тудыруға қажетті күш.Шекті жылу кернеуі температураға тәуелді және жоғарғы температуралар кезінде майлағыштардың жұмыс қабілетін,тамшы таму температурасына қарағанда дәл сипаттайды.
Ауа оттегісінің,қыздырудың және басқа да факторлардың әсері қоюландырғыштың да,майдың да тотығуын және бұзылуын тудырады.Сабындық майлағыштарда тұрақтылығы аз компонент сабын,ал қорғағыш майлағыштарда – май болып табылады. Майлағыштарда металды коррозиялайтын қышқылдар, сонымен қатар шайырлы және көмірлі шөгінділер пайда болады.
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 5948; Нарушение авторских прав?; Мы поможем в написании вашей работы!