
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Цикл Карно
|
|
|
|
Различают прямой цикл, или цикл тепловой машины, и о братный цикл, или цикл холодильной машины. При круговом процессе мы получаем от системы работу за счет эквивалентной затраты тепла. После окончания цикла тело возвращается в свое первоначальное состояние, его внутренняя энергия не изменилась. Поэтому работа цикла может совершиться только за счет внешних источников, подводящих к рабочему телу теплоту. Без затрат невозможно получить работу. Механизм, позволяющий осуществить круговой процесс, т.е. переход тепла в механическую работу, называется тепловой машиной. (например паровая машина и двигатель внутреннего сгорания).
Сади Карно был предложен цикл идеальной тепловой машины. Рабочий цикл состоит из двух равновесных изотермических и двух равновесных адиабатических процессов. В машине отсутствуют всякие потери на теплопроводность, лучеиспускание, трение и т.д. С машиной связаны два больших резервуара: нагреватель (теплоотдатчик), имеющий температуру Т1 и холодильник (теплоприемник), имеющий более низкую температуру Т2. Резервуары имеют большую емкость, поэтому отдача или получение ими теплоты не изменяет их температуры. Рассмотрим работу этой идеальной тепловой машины (рис.39).
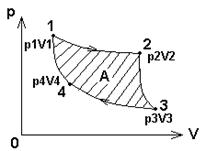 Машина состоит из цилиндра, заполненного рабочим веществом (идеал. газ). Поршень цилиндра может перемещаться вертикально. Прямой цикл состоит из четырех процессов:
Машина состоит из цилиндра, заполненного рабочим веществом (идеал. газ). Поршень цилиндра может перемещаться вертикально. Прямой цикл состоит из четырех процессов:
1) изотермическое расширение газа от объема V1 до объема V2 при температуре Т1;
2) адиабатическое расширение его до объема V3 с понижением температуры до Т2;
3) изотермическое сжатие его до объема V4 при температуре Т2;
Рисунок 39 4) адиабатическое сжатие его до объема V1 и
начальной температуре Т1.
На участке 1-2 газ совершил работу А1 за счет полученной теплоты Q1 и
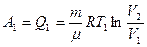 (1)
(1)
На участке 2-3 – работу А’ за счет своей внутренней энергии. На участке 3-4 внешние силы совершили работу А2 и газ отдал часть теплоты холодильнику Q2=A2
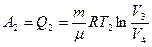 (2)
(2)
и на участке 4-1, внешние силы совершили работу А’’, повысив его внутреннюю энергию. Газ вернулся в исходное состояние, т.е. изменение внутренней энергии ∆U=0. Согласно первому началу термодинамики Q=∆U+A,
количество теплоты, полученное газом, совершает работу Q1-Q2=A1+A’-A2-A’’
т.к. |A’|=|A’’| - протекают при одинаковом интервале температуры.
Q1-Q2=A1-A2=А,
где А – суммарная работа (положительная). При адиабатическом процессе А= CV(T1-T2),
тогда:
А= Q1-Q2 (3)
Тепловая машина не может все полученное количество теплоты целиком переводить в работу. Таким образом:
А<Q1 (4)
Невозможен механизм, который все полученное от нагревателя количество теплоты целиком переводил бы в работу, часть этого количества теплоты должна быть отдана холодильнику. Это формулировка второго начала термодинамики. А формулы (3) и (4) – его математические выражения. Первое начало термодинамики устанавливает количественные соотношения между теплотой, работой и изменением ∆U, но он не определяет направления течения процессов, которые устанавливает второе начало термодинамики. Схема тепловой машины приведена на рис.40.
 |
|
|
 |  | ||||
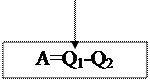 |
Рисунок 40.
Воображаемый механизм, превращающий все количество теплоты в работу, называется вечным двигателем второго рода. Вечный двигатель второго рода невозможен – формулировка также второго начала термодинамики.
Обратный цикл Карно можно назвать холодильной машиной и он состоит из процессов
1) адиабатическое расширение от объема V1, до объема V4 с понижением температуры до Т2;
2) изотермическое расширение от объема V4 до объема V3 при температуре Т2;
3) адиабатическое сжатие от объема V3 до объема V2 с повышением температуры до Т1;
4) изотермическое сжатие до объема V1 при температуре Т1;
При таком цикле холодильник отдает идеальному газу количество теплоты Q2, а нагреватель получает количество теплоты Q1. Таким образом происходит передача тепла от более холодного тела к более горячему.
Согласно Клаузиусу «теплота не может сама собой переходить от менее нагретого тела к более нагретому». (это одна из первых формулировок первого начала термодинамики). Т.е. для такого перехода теплоты требуется затрата работы внешнего источника, как это происходит в холодильной машине.
Кельвин (Томсон) «Невозможно построить тепловую машину, которая переводила бы в работу теплоту наиболее холодного из имеющихся в системе тел». Такой машиной была бы машина, превращающая в работу теплоту воды в океане. (Объем воды ~1370 млн. км3. 1500 лет. Вращать станки и машины для всего мира, понизив температуру на 0,1º)
Тепловую машину принято характеризовать коэффициентом полезного действия η (К.П.Д.), который определяется как отношение совершаемой за цикл работы А к полученному за цикл количеству теплоты Q1 от нагревателя:
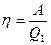 или
или 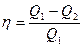 (5).
(5).
Формулировка второго начала термодинамики: «К.П.Д. идеальной тепловой машины, работающей по циклу Карно, зависит только от температуры нагревателя и холодильника».
Во всех машинах Q2>0 т.е. η<1. Карно писал:» нельзя построить тепловую машину с К.П.Д., равным единице (100%). Если это можно было сделать, то был бы получен вечный двигатель второго рода (perpetuum mobile).
В случае, когда Q2=0, то температуру рабочего тела нужно было бы довести до температуры абсолютного нуля, которую должен иметь холодильник., но реальные машины имеют в лучшем случае температуру холодильника порядка 100°С, т.е. 373°К. Поэтому К.П.Д. тепловых машин (лучших) не превышает 0,4-0,5 (некоторые типы двигателей внутреннего сгорания).
Формула К.П.Д. обратимого равновесного цикла Карно имеет вид:
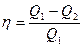
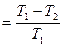 (10).
(10).
В реальных процессах, осуществляющих тепловую машину, всегда имеются потери тепла на трение, теплопроводность и т.д., тогда
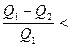
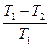 (11),
(11),
объединим оба выражения (10) и (11) в одно:
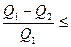
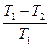 (12),
(12),
где знак равенства относится к случаю обратимого (равновесного) цикла, а знак неравенства – к случаю необратимого.
Выражение (12) приведем к виду:
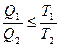 или
или 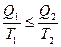 ; или
; или 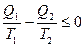 .
.
Условимся количество теплоты, отданное телу нагревателем, считать положительным, а количество теплоты, отданное телом холодильнику – отрицательным, тогда
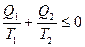 (13)
(13)
или в общем виде:
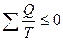 (14) – неравенство Клаузиуса.
(14) – неравенство Клаузиуса.
Отношение 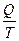 количества переданной теплоты к абсолютной температуре, называется приведенной теплотой.
количества переданной теплоты к абсолютной температуре, называется приведенной теплотой.
Неравенства (13) или (14) гласят: « при круговом процессе Карно сумма приведенных теплот не может быть больше нуля» (она <0 – для необратимого цикла (процесса) и 0 – для обратимого).
Рассмотрим произвольный круговой процесс, который можно разбить на весьма большое число элементарных циклов Карно. И неравенство Клаузиуса можно представить так:
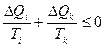 .
.
суммируя для всего кругового процесса, получим:
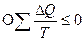 (15)
(15)
знак ○ указывает, что сумма в (15) берется для всего кругового процесса. Это основное неравенство второго начала термодинамики Клаузиуса.
И для бесконечно узких циклов обратимого цикла Карно сумма заменяется (превращается) интегралом (это криволинейный интеграл)
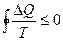 (16).
(16).
Если криволинейный интеграл по замкнутому контуру равен нулю, то под интегралом стоит полный дифференциал функции.
 13.3 Энтропия
13.3 Энтропия
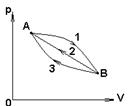
Рассмотрим обратимый цикл (рис. 41). А и В – произвольные состояния. Можно доказать, что сумма приведенных количеств тепла при переходе из состояния А в состояние В не зависит от пути, по которому совершается переход. Таким образом
Рисунок 41
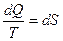 (17), где S – функция состояния тела, введена
(17), где S – функция состояния тела, введена
Клаузиусом и названа им энтропией. (греческое слово «энтропос» - поворот, возвращение).
Изменение энтропии ∆ S при переходе из состояния А в состояние В равно:
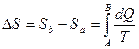 (18),
(18),
где Sa и Sb – энтропия в начальном и конечном состояниях системы. Размерность энтропии – Дж/град. Каждое состояние тела характеризуется определенным значением энтропии S. По формуле (18) можно вычислить только разность энтропии для двух состояний тела.
Клаузиусом получены следующие положения, которые мы принимаем без доказательства:
а) энтропия системы, состоящей из нескольких тел, равна сумме энтропий этих тел.
б) если в изолированной системе происходят необратимые процессы, то ее энтропия возрастает.
в) энтропия изолированной системы не может уменьшаться ни при каких процессах.
Математически эти выражения записываются в виде неравенства Клаузиуса:
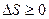 (19).
(19).
Все реальные процессы являются необратимыми. Поэтому в изолированной системе все процессы ведут к увеличению ее энтропии. Это положение называется принципом возрастания энтропии.
Рассмотрим физический смысл энтропии. Из формулы К.П.Д. видно, что для получения наибольшей работы температура нагревателя должна быть как можно выше. Переданное количества тепла телу считают положительным, следовательно и изменение энтропии тоже положительным. И энтропия тела возрастает. Если передача теплоты происходит при более низкой температуре нагревателя, то К.П.Д. будет ниже, а возрастание энтропии больше, т.к. температура в выражении для энтропии входит в знаменатель. Поэтому энтропию можно рассматривать как меру обесцененности энергии тела. Или иногда употребляют: энтропия есть мера тепловой неработоспособности тела. При возрастании энтропии – увеличивается беспорядок в состоянии системы, т.е. энтропия – мера беспорядка состояния системы.
Вопросы для самоконтроля
1. Что называется круговыми процессами (циклами)?
2. Проанализируйте прямой и обратный циклы.
3. Возможен ли процесс, при котором теплота, взятая от нагревателя, полностью преобразуется в работу?
4. Сформулируйте второе начало термодинамики.
5. Дайте понятие энтропии.Как изменяется энтропия изолированной системы при процессах: 1) обратимых; 2) необратимых?
СПИСОК ЛИТЕРАТУРЫ
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2306; Нарушение авторских прав?; Мы поможем в написании вашей работы!