
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Силикаты в стеклообразном состоянии
|
|
|
|
Общее определение стекла дано комиссией по терминологии АН СССР:
«Стеклом называют все аморфные тела, получаемые путем переохлаждения расплавов независимо от их химического состава и температурной области затвердевания и обладающие в результате постоянного увеличения вязкости механическими свойствами твердых тел, причем процесс перехода из жидкого состояния в стеклообразное должен быть обратимым.»
На основе этого определения силикатными стеклами называются изотропные тела, являющиеся продуктом затвердевания силикатных расплавов при их переохлаждении.
4.1. Гипотезы строения стекол
Создание исчерпывающей теории стекол является задачей, решение которой не найдено до сих пор. Существует несколько гипотез строения стекол, распространение из которых получили две: неупорядоченной бесконечной сетки и кристаллитная.
Структурно-координационная гипотеза Захариасена-Уоррена предполагает, что стекло представляется в виде неупорядоченной бесконечной непрерывной объемной сетки, в узлах которой расположены ионы, атомы или атомные группы (рис.10).
Согласно этой гипотезе структура кварцевого стекла построена из связанных друг с другом кремнекислородных тетраэдров, для которых наблюдается ближний порядок и отсутствует дальний порядок, то есть тетраэдры расположены произвольно на расстоянии, большем, чем два межатомных расстояния.
Стекло сложного состава с катионами натрия, калия, кальция по этой гипотезе имеют в своей основе неупорядоченный объемный кремнекислородный каркас. Катионы металлов размещаются неупорядоченно в пустотах между кремнекислородными тетраэдрами, при этом для размещения катионов часть связей между тетраэдрами нарушается.
Таким образом, структурно-координационная гипотеза предполагает гомогенное строение стекла, так как в стекле нельзя выделить каких-либо структурно-упорядоченных областей, что не всегда подтверждается экспериментальным материалом.
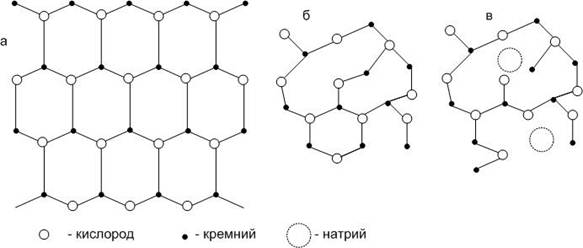 |
Рис.10. Схемы структурных решеток:
а – кристаллического кварца, б – кварцевого стекла, в – натрийсиликатного стекла
По кристаллитной гипотезе Лебедева А.А. стекло представляет собой сложную микрогетерогенную систему, составной частью структуры которой являются кристаллиты-субмикрокристаллические образования с определенной степенью упорядоченности структурных элементов (рис.11).
В отличие от кристаллов решетка кристаллитов значительно искажена, причем степень деформации решетки переменна даже для объема одного кристаллита: в центральной части кристаллита его структура близка структуре кристаллов, при переходе к периферийной области степень упорядоченности нарушается. Размер кристаллитов составляет 1,5 … 6 нм, соответствующих температурных условиях кристаллиты могут увеличиваться в размерах и образовывать зародыши кристаллов.
Следует также отметить, что химический состав кристаллитов определяется прежде всего химическим составом стекла и изменяется с изменением последнего.
Экспериментальный материал последних лет позволяет утверждать, что кристаллитная гипотеза детальнее объясняет структуру стекла.
Рис.11. Схема кристаллитной структуры кварцевого стекла
Способность жидкостей при охлаждении образовывать стекла варьируется в зависимости от химической природы в чрезвычайно широких пределах. Численно стеклообразующую способность жидкостей можно характеризовать с помощью критической скорости охлаждения. Чем эта скорость меньше, тем легче жидкость переходит в стекло. Критические скорости для известных стеклообразующих веществ лежат в пределах от нескольких десятых градуса в год до десяти миллионов градусов в секунду. Жидкости с особо низкими критическими скоростями почти невозможно закристаллизовать.
Какие же жидкости можно перевести в стеклообразное состояние? В первую очередь расплавы ряда чистых оксидов и их смесей в бесконечном числе вариантов. Относительно легко переводятся в стекла многие расплавы: галогенидные, нитратные и др. Широкий класс стеклообразующих веществ представляет собой органические полимеры, особенно имеющие в структуре сложные по конфигурации молекулы. В стеклообразном состоянии могут быть легко получены органические вещества, молекулы которых содержат небольшое число атомов, например сахароза. Стеклообразная сахароза это известный всем леденец. И наконец, в последние годы получил широкий размах исследования металлических стекол, сплавов различных металлов, переведенных в стеклообразное состояние в результате особо быстрого охлаждения.
Таким образом, в стеклообразном состоянии могут находиться вещества различного химического типа с разными видами химических связей. Стекла могут быть прозрачными и ²глухими², хорошими проводниками электрического тока и диэлектриками, очень твердыми и чрезвычайно мягкими. Но многие структурные и термодинамические особенности, специфическое упруговязкое поведение и некоторые другие свойства характерны именно для веществ в стеклообразном состоянии.
Следовательно, в качестве основных условий образования стекол можно выделить следующие:
1) физическим условием образования стекла является быстрое охлаждение расплавленного вещества;
2) обязательным условием образования стекла является способность вещества образовывать протяженную трехмерную пространственную сетку, в которой отсутствует строгая периодичность расположения структурных элементов, а энергия сетки сравнима с энергией кристаллической решетки.
Указанным условиям удовлетворяют оксиды-стеклообразователи с формулой общего состава от R2O3 R2O5: оксиды кремния и бора, фосфора и лития и т.п. Модификатороми структуры являются оксиды калия и натрия, кальция и бария, свинца, которые вводятся в состав стекла для придания ему заданных свойств.
Способность к стеклообразованию у силикатов увеличивается по мере снижения отношения кремния к кислороду. Поэтому в ряду ортосиликаты: полевые шпаты: кварц труднее всего в стекло переходят ортосиликаты.
4.2. Общие особенности стеклообразного состояния
Независимо от химического состава вещества в стеклообразном состоянии имеют ряд общих особенностей.
Стекла – метастабильные неравновесные системы, характеризующиеся избытком внутренней энергии. Исходя из этого, процесс кристаллизации стекол имеет экзотермический характер. Длительное существование стекол в метастабильном состоянии объясняется их высокой вязкостью, которая препятствует процессу диффузии и переориентации структурных элементов.
Стекла имеют изотропный характер, объясняющийся однородностью их структуры.
Для стекол характерна способность к постепенному и обратимому затвердеванию при переходе из расплавленного в твердое состояние без появления новой фазы при одновременном непрерывном изменении своих свойств.
Стекла не имеют температуры плавления. Изменение вязкости проявляется в широком интервале температур. Хрупкие свойства, характерные для твердого состояния, проявляются для стекол любой химической природы при вязкости около 1012Па*с.
Температуру, соответствующей этой вязкости, называют температурой стеклования Tg (рис.12). Температура, при которой стекла проявляют свойства текучих жидкостей, получила название температуры текучести Tf.
Для стеклообразного состояния характерно наличие температурного интервала Tg-Tf, в котором происходит резкое, но непрерывное изменение свойств стекла. Интервал получил название аномального интервала стекла.
Для технических стекол Tg находится в пределах 420 … 560 градусов, Tf - в пределах 680 … 700 градусов.
Величина аномального интервала стекла зависит от химического состава стекла и его тепловой истории: скорости охлаждения, полноты отжига и т.п.
Кристаллизационная способность стекол зависит от двух основных параметров: скорости образования центров кристаллизации (СОЦК) и скорости роста кристаллов (СРК), зависимости которых от температуры приведены на рис.13.
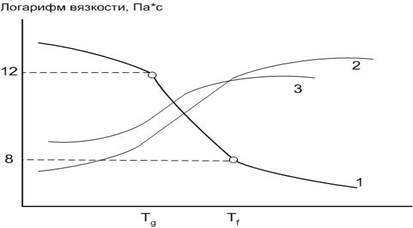 |
Рис.12. Зависимость свойств стекла от температуры:
1 – вязкость, 2 – теплоемкость, 3 – КЛТР
4.3. Кристаллизационная способность силикатных стекол
В метастабильной зоне перегрева (1) СОЦК незначительна, а СРК также невелика из-за большого теплового движения. В этой зоне кристаллизация стекол практически не протекает. При понижении температуры процесс кристаллизации будет протекать самопроизвольно. Изменение вязкости расплава будет неоднозначно влиять на СОЦК и СРК, поэтому их температурные максимумы не совпадают. Стекло имеет хорошую кристаллизационную способность, если Т1 приближается к Т2, то есть площадь зоны (2) максимальна.
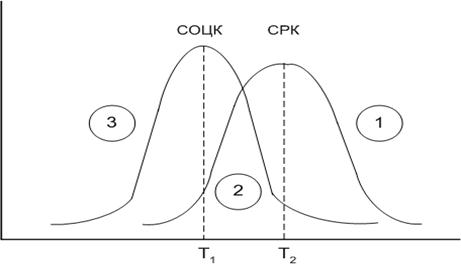 |
Рис.13. Кристаллизационная способность стекол
В области низких температур (3) высокая вязкость системы препятствует возникновению центров кристаллизации, скорость роста кристаллов практически равна нулю, кристаллизация невозможна и расплавы при этом переходят в стекло, а не кристаллическое состояние.
Кристаллизация силикатных расплавов и стекол используется при получении строительного материала ситалла.
К ситаллам относятся материалы, получаемые при обильной мелкокристаллической объемной кристаллизации стекла. Структура ситаллов представляет собой закристаллизованные стекла с размером кристаллов 0,1 … 0,3 мкм, между которыми располагаются тонкие прослойки стекла.
Мелкокристаллическая структура ситаллов создается за счет специальной термической обработки, которая заключается в двухступенчатой изотермической выдержке при температурах СОЦК и СРК. При температуре максимального образования центров кристаллизации в объеме стекла добиваются получения большого количества зародышей кристаллов, рост которых обеспечивается второй ступенью выдержки. Регулирование длительности выдерживания при постоянной температуре позволяет регулировать соотношение в ситаллах кристаллической и стеклообразной фазы.
Мелкокристаллическая структура ситаллов обеспечивается также введением в состав стекла добавок катализаторов кристаллизации (золото, серебро, платина, оксид хрома, рутил, фторид кальция и т.п.), а также облучением стекол рентгеновским и ультрафиолетовыми лучами.
Ситаллы имеют повышенную механическую прочность и твердость, термостойкость и используются в качестве облицовочного материала.
В практическом отношении эффективными являются шлакоситаллы, получаемые на основе побочных продуктов промышленности – огненно-жидких доменных шлаков.
Контрольные вопросы
1. Что называется стеклом?
2. В чем заключается различие структурно-координационной и кристаллитной гипотез строения стекла?
3. В чем отличие кристаллов от кристаллитов?
4. Каковы основные условия образования стекол?
5. Назовите основные особенности стеклообразного состояния.
6. Какой температурный интервал называется аномальным? В чем его физический смысл и как величина интервала влияет на технологию изготовления строительных изделий из стекла?
7. Какими параметрами определяется кристаллизационная способность стекол?
8. Опишите режим термообработки шлаковых расплавов для получения шлакоситаллов.
Основная литература [1, 11]
Дополнительная литература [2, 13]
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1417; Нарушение авторских прав?; Мы поможем в написании вашей работы!