
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диффузия и ее виды
|
|
|
|
Диффузией называется процесс переноса вещества из одной части системы в другую в результате беспорядочного движения частиц. Различают следующие виды диффузии:
самодиффузия – диффузия частиц одного вещества, протекающая при отсутствии градиента каких-либо движущих сил;
концентрационная диффузия – перемещение вещества под воздействием градиента концентрации. Эта диффузия называется нисходящей, поскольку вещество перемещается из участков, в которых его концентрация больше, в участки, где его концентрация меньше;
термодиффузия – перенос вещества под воздействием градиента температур. Термодиффузия обусловлена возникновением градиента химического потенциала диффундирующего вещества в температурном поле. Вещество перемещается из частей системы, в которых его химический потенциал больше,
в части, в которых его химический потенциал меньше. При этом концентрация вещества изменяется в обратном направлении и диффузия называется восходящей;
реактивная диффузия – перемещение вещества в участки системы, где оно образует с другим компонентом раствора химическое соединение, т.е. диффундирующее вещество выводится из исходной фазы в обособленную (например, диффузия углерода в участки образования карбидов, диффузия легирующих элементов – в участки, где образовались интерметаллиды). К реактивной диффузии относится также перераспределение углерода между аустенитным швом и ферритно-перлитным основным металлом: углерод диффундирует в аустенит, в котором его растворимость выше.
Концентрационная диффузия является наиболее простым случаем и наиболее изучена.
Процессы концентрационной диффузии описываются уравнением законов Фика:
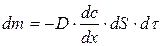 , (11)
, (11)
где 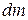 – количество продиффундировавшего вещества; dS – площадь сечения диффузионного потока, dτ – время
– количество продиффундировавшего вещества; dS – площадь сечения диффузионного потока, dτ – время 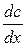 – градиент концентрации, отрицательный потому, что диффузия идет от большей концентрации к меньшей; D – коэффициент диффузии,
– градиент концентрации, отрицательный потому, что диффузия идет от большей концентрации к меньшей; D – коэффициент диффузии,  .
.
Закон Фика справедлив для малых концентраций диффундирующего вещества, далеких от концентрации насыщения.
Процесс диффузии аналогичен распределению тепла посредством теплопроводности. Количество вещества соответствует количеству тепла, а концентрация – температуре. Поэтому второй закон диффузии может быть выведен аналогично уравнению теплопроводности:
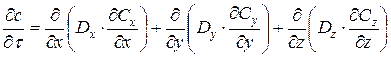 . (12)
. (12)
Уравнение (12) выражает второй закон Фика в самом общем виде в предположении, что коэффициент диффузии зависит от концентрации элемента и различен в различных направлениях. Если считать коэффициент диффузии не зависящим от концентрации, а тело – изотропным, т.е. полагать, что 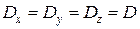 , то выражение (12) упростится:
, то выражение (12) упростится:
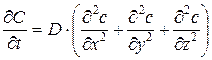 (13)
(13)
или
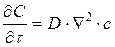 , (14)
, (14)
где 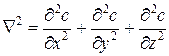 .
.
В простейшем случае линейной диффузии по оси х, когда концентрация по оси y и z постоянна, 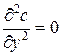 и
и  . Для этого случая получим
. Для этого случая получим
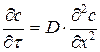 . (15)
. (15)
Интегрирование уравнения (15) дает зависимость концентрации диффундирующего вещества от координаты х и времени τ:
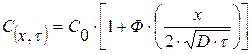 , (16)
, (16)
где 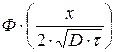 – функция Крампа от аргумента
– функция Крампа от аргумента 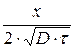 ; её можно найти по таблице для заданных значений х; D; τ.
; её можно найти по таблице для заданных значений х; D; τ.
Расчет развития диффузионных процессов на основании второго закона Фика сохраняется для жидких и твердых сред, но коэффициенты диффузии будут значительно меньше, чем для газообразных систем.
Для газообразных систем коэффициенты диффузии вычисляются на основании кинетической теории газов:
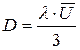 , (17)
, (17)
где λ – длина свободного пробега; 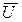 – средняя скорость движения газовых молекул.
– средняя скорость движения газовых молекул.
Коэффициенты диффузии в жидкостях могут быть рассчитаны по уравнению Стокса:
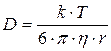 , (18)
, (18)
где k – постоянная Больцмана; Т – температура; η – коэффициент вязкости среды; r – радиус частицы.
Коэффициент диффузии в жидкостях на несколько порядков меньше, чем в газах. Для твердых кристаллических тел коэффициенты диффузии еще меньше.
Коэффициент диффузии значительно меняется в зависимости от температуры процесса, концентрации диффундирующего вещества, свойств среды, наличия в сплаве третьего компонента.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 18349; Нарушение авторских прав?; Мы поможем в написании вашей работы!