
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вода в цеолитах
|
|
|
|
Вода в минералах. Классификация. Вода в цеолитах
Вода в минералах. Классификация
Относительно воды в минералах в литературе существуют самые различные термины и классификации. Остановимся вкратце на них, чтобы было ясно, относительно какой из разновидностей воды идет речь. По литературным данным вода в минералах бывает:
– конституционная,
– кристаллизационная,
– вода твердых коллоидов,
– межплоскостная,
– межслоевая,
– гигроскопическая,
– физически связанная,
– химически связанная,
– цеолитная,
– адсорбционная.
Вода конституционная находится в кристаллической решетке минерала в виде ионов ОН1–, реже Н1– и оксония Н2О+; она переходит в молекулярное состояние лишь при разрушении структуры минерала. При нагревании выделение конституционной воды у каждого минерала происходит в определенном интервале температур от 300 до 1000 °С.
Кристаллизационная вода находится в решетке в виде нейтральных молекул Н2О, занимающих определенные места. Выделение кристаллизационной воды при нагревании происходит при температуре ниже 300 °С. Различаются два типа кристаллизационной воды. Типичная кристаллизационная вода выделяется в узком интервале температур с полным разрушением и перестройкой структуры минерала с изменением его физических свойств: показатель преломления, удельный вес и др.
Цеолитная вода может выделяется постепенно, в большом интервале температур, и вновь поглощаться при изменении условий, без нарушения физической однородности вещественного состава, но с изменением всех его физических свойств (например, прозрачности, показателя преломления и т. д.).
Молекулы адсорбционной воды находятся на поверхности кристаллических частиц и легко удаляются при нагревании.
|
|
|
Различают межплоскостную воду, адсорбированную на поверхности отдельных слоев в минерале, воду твердых коллоидов (затвердевших гелей) и гигроскопическую воду, механически примешанную к минералу, которая при нагревании полностью удаляется при температуре 105–110 °С. Межплоскостная вода в минералах – вода, характерная для некоторых минералов слоистой структуры (например, монтмориллонита, слюд). Молекулы этой воды располагаются иногда в несколько слоев между нейтральными слоями решетки. По своему типу она приближается к кристаллизационной, а по поведению близка к цеолитной воде, но, в отличие от последней, при выделении ее объем минерала уменьшается, а удельный вес и показатель преломления увеличиваются.
Адсорбционная вода – молекулы связаны с поверхностью кристаллических частиц, образуют вокруг частиц гидратные оболочки.
Такое большое разнообразие терминов по определению воды в минералах вносит большую путаницу, и порой сложно определить, с какой водой имеем дело. Нужна более строгая классификация воды и более современный метод ее отнесения. Наиболее надежными методами являются метод ЯМР и метод ИК-спектроскопии, которые позволяют классифицировать ее по энергии связи с минералом.
Горные породы характеризуются влагоемкостью и водоотдачей. Влагоемкостью называется способность горных пород вмещать и удерживать определенное количество воды. Высокой влагоемкостью обладают глины; средней – мелкие пески; слабой – галечники. Влагоемкость, определяемая силами молекулярного притяжения на поверхности частиц пород, зависит от диаметра этих частиц. Так, например, влагоемкость частицы диаметром 1 мм равна 1,6 %, а диаметром менее 0,005 мм – 45 %.
Водоотдача – отношение количества воды, которое может отдать порода, к общему содержанию воды в ней. Здесь зависимость диаметрально противоположна: процент водоотдачи тем больше, чем крупнее частицы породы. Так, у галечников она максимальная, а у глин минимальная.
|
|
|
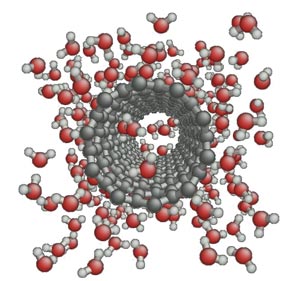

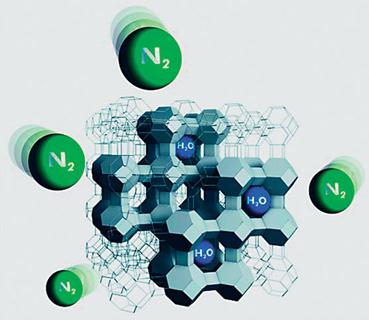
Все цеолиты по своему химическому составу являются водными алюмосиликатами кальция, натрия, бария, калия. Вопрос о том, в каком виде заключается в силикатах вода, еще далеко нельзя считать решенным. Дело в том, что вода, заключающаяся в них, выделяется из них при различной температуре: у одних при нагревании до сравнительно низкой температуры, у других же только прокаливанием можно выделить всю воду (напр., у натролита вся вода может быть удалена только нагреванием до 300°). Интересно то, что лишенные воды цеолиты. способны во влажном воздухе снова возмещать потерянную воду, причем все прежние физические свойства тоже восстановляются.
Если тонкий обломочек цеолита ввести в самое горячее место пламени паяльной трубки, то он очень быстро сплавляется, после чего вода из продолжающих нагреваться внутренних частей минерала не может выйти на воздух, она вздувает это новообразованное стекло, и кусочек цеолита перед паяльной трубкой начинает увеличиваться в объеме, изгибаться, местами в нем появляются боковые вздутия, а иногда и довольно большие выросты. Эта особенность минерала, свидетельствующая о его легкоплавкости и содержании в нем воды, и дала название всей минеральной группы.
Присутствие воды – характернейший признак цеолитов – можно обнаружить и иначе. Если на дно пробирки насыпать порошок цеолита и осторожно нагреть его так, чтобы верхняя часть пробирки осталась холодной, то очень скоро вода, выделяющаяся из нагревающегося цеолита, в виде капель осядет на холодных стенках пробирки.
Вода в цеолитах имеет еще одну особенность. Если нагревание цеолита относительно невелико и не превышает 300–400°, то из цеолита постепенно выделяется значительная часть содержащейся в нем воды. При этом структура цеолита не разрушается, и если после охлаждения или в процессе охлаждения минерал будет помещен во влажную атмосферу, он снова очень активно поглощает воду и восстанавливает все свои свойства. Такая легко отдаваемая и вновь восстанавливаемая вода в структуре минерала получила даже название «цеолитной воды».
|
|
|
Своеобразны и некоторые другие свойства цеолитов. Они, например, как оказалось, очень легко подвергаются так называемому ионному обмену; в результате обработки цеолита растворами, содержащими какой-либо катион (металл), присутствующие в составе минерала щелочи и щелочные земли могут заменяться этим новым катионом, даже таким, как серебро.
Причина этих необычных особенностей цеолитов заключается в их структуре. Для структуры цеолитов, как и для структуры полевых шпатов, характерен алюмосиликатный каркас, в котором каждый ион алюминия или кремния окружен четырьмя ионами кислорода, а каждый ион кислорода, в свою очередь, связан с двумя ионами этих металлов. Избыточные отрицательные ионы (Напомним, что алюминий трехвалентен и, таким образом, может компенсировать только три, а не четыре кислородных заряда. В результате один заряд кислорода остается «избыточным») компенсируются ионами натрия, кальция или реже калия. Как в структуре полевого шпата, так и в структуре цеолитов эти ионы располагаются в плоскостях кремнекислородного каркаса. В структуре полевого шпата такие полости очень малы, тогда как в структуре цеолитов эти полости крупные и зачастую сообщаются между собой (рис. 1 и 2). В структуре многих цеолитов присутствуют и каналы, пронизывающие всю кристаллическую постройку. Отсюда и большая относительная легкость цеолитов (напомним, что плотность полевых шпатов около 2,6–2,7 г/см3, а цеолитов 2,1–2,2 г/см3, редко выше). К этим каналам и полостям у цеолитов приурочены щелочные и щелочноземельные катионы, а также молекулы воды; последние сравнительно слабо связаны с каркасом и катионами, и поэтому могут свободно удаляться по каналам без разрушения связей каркаса – это и создает способность цеолита терять воду и набирать ее обратно.
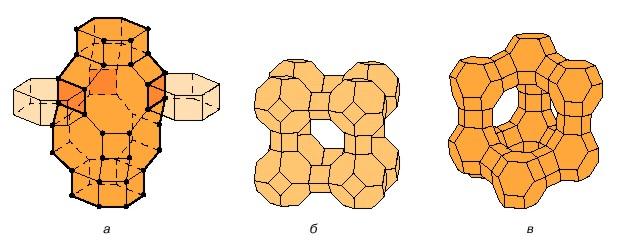



а б в
Рисунок 1 – Структурные элементы цеолитов: а – шабазит; б – синтетические кристаллы Линде Х; в – фожазит.
Прямыми линиями соединены центры соседних тетраэдров. Каждая вершина соответствует положению атома Si или Al. Видны широкие каналы, благодаря которым цеолиты используются в качестве молекулярных сит
|
|
|

 3
3  4
4
Рисунок 2 – Цеолит NaA (структура типа LTA, размер пор 0,41 нм):
1 – структура; 2 – кристаллы; 3 – молекулярное сито-5A; 4 – молекулярное сито-3А.
Способность цеолитов, потерявших воду, поглощать ее обратно из разных сред, а также молекулярно-ситовая способность – способность избирательно адсорбировать некоторые вещества, была замечена довольно давно, но только в самом начале пятидесятых годов прошлого века начала практически использоваться.
Спектры ЯМР (ядерный магнитный резонанс) цеолитной воды в большинстве природных и искусственных кристаллов семейства цеолитов и их модификаций отвечают фиксированной воде лишь при температурах, не превышающих 200–250 К. Исключение составляют узкопористые цеолиты (натролит, сколецит, томсонит и др.), для которых не фиксируется подвижность молекул воды до 350–400 К.
Интересно, что ИК-спектры узкопористых цеолитов обладают тонкой структурой, как и в случае гипса, что указывает на упорядоченность структуры кристалла в целом.
При температурах свыше 200–250 К спектры ЯМР широкопористых цеолитов резко (в сотни раз) сужаются и приобретают характерную для диффундирующей в кристаллах воды структуру. При этом существенны два факта.
Во-первых, ширина суженного спектра остается постоянной вплоть до температуры дегидратации (200–300° С и более). Это означает, что при всех температурах молекула движется по одному и тому же строго заданному структурой кристалла диффузионному пути в точности так же, как в кристаллогидратах.
Во-вторых, несмотря на низкотемпературную подвижность, сохраняются очень высокие значения температуры дегидратации. Данная особенность резко отличает цеолиты от кристаллогидратов, в которых дегидратация или плавление редко происходит при температурах заметно выше 100 °С.
Природа высокотемпературного гидратированного состояния цеолитов прояснилась только после обнаружения «двухфазного» строения цеолитной воды. Оказалось, что диффузия молекул воды в цеолитных каналах не мешает некоторой части этих молекул быть жестко связанной в цеолитных каналах. Например, в мордените, несмотря на начало диффузионного сужения спектра ЯМР при –100 °С, даже при –110° С остается около 10 % жестко связанной воды (при этом полная дегидратация имеет место лишь при 450 °С).
Было предположено, что эти жестко связанные молекулы подобно пробкам блокируют цеолитный канал, преграждая путь диффундирующим молекулам. Отсюда естественно выдвинуть изохорическую модель цеолитной воды в замкнутом пространстве каналов. Нагрев повышает давление внутри канала а вместе с давлением растет и температура «плавления» цеолитной воды. В соответствии со сказанным диффузию воды в гидратированных цеолитах можно рассматривать как изохорическое (в замкнутом объеме) плавление.
Очевидно также, что эффективность «пробок» в запирании объема каналов связана с их коллективными свойствами, вытекающими из наличия более прочных связей вода-вода в определенных участках цеолитных каналов».
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2110; Нарушение авторских прав?; Мы поможем в написании вашей работы!