
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Физический смысл энергии активации
|
|
|
|
Лекция №3
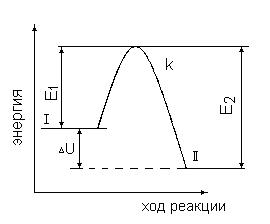
Пусть I – уровень средней энергии молекул в исходном состоянии
II – уровень средней энергии молекул продуктов
∆ u – тепловой эффект реакции.
Для того, чтобы при столкновении молекул произошла реакция молекулам необходимо иметь запас энергии, достаточный для того, чтобы преодолеть отталкивание электронных оболочек. Говорят, система должна преодолеть энергетический барьер. Уровень k – определяет этот минимальный запас энергии. Разность уровней k и I, обозначенная Е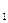 представляет собой энергию активации прямой реакции. Е
представляет собой энергию активации прямой реакции. Е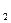 - энергия активации обратной реакции.
- энергия активации обратной реакции.
Энергия активации – это то избыточное количество энергии (по сравнению со средней энергией) которой должны обладать молекулы в момент столкновения для того, чтобы быть способными к данному химическому взаимодействию.
Не все молекулы, а только некоторые из них обладают достаточной энергией для того, чтобы произошла реакция, эти молекулы называют активными. Количество таких молекул определяет распределение Максвелла – Больцмана.
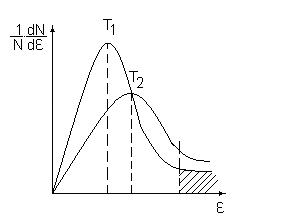
Площадь под кривой характеризует долю молекул, обладающих энергией большей, чем заданная (уровень k).
Чем больше энергия активации, тем меньше активных молекул, тем меньше скорость реакции (при прочих равных условиях температура, концентрация, порядки).
С ростом температуры скорость реакции увеличивается, так как увеличивается число активных молекул. Чем выше энергия активации, тем круче зависимость скорости от температуры.
Пример: определить во сколько раз увеличится скорость реакции при увеличении температуры от 300 кельвинов до 400 кельвинов, если энергия активации 100 кДж/моль.

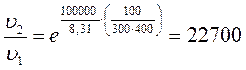
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 8123; Нарушение авторских прав?; Мы поможем в написании вашей работы!