
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химическая конденсация
|
|
|
|
Методы получения коллоидных систем.
Имеются два возможных пути получения коллоидных растворов. Один путь состоит в укрупнении частиц при агрегации молекул или ионов – такой метод называют конденсационным. Второй путь заключается в измельчении крупных частиц до коллоидной дисперсности, его осуществляют методом диспергирования.
При получении коллоидов в системе обязательно должны присутствовать вещества (стабилизаторы), образующие защитные оболочки вокруг частиц и препятствующие их слипанию, то есть коагуляции и выпадению в осадок (седиментации). Это электролиты, ПАВ, белковые соединения и т. п.
Метод конденсации.
Конденсационные методы - это способы получения коллоидных растворов путем объединения (конденсации) молекул и ионов в агрегаты коллоидных размеров. Система из гомогенной превращается в гетерогенную, т.е. эти методы сопровождаются возникновением новой фазы - дисперсной фазы. Обязательным условием является пересыщенность исходной системы.
Конденсация может протекать и как химический, и как физический процесс. В обоих случаях метод конденсации основан на образовании в гомогенной среде новой фазы, имеющей коллоидную дисперсность.
1. Получение коллоидного раствора возможно в результате химических реакций в которых образуются труднорастворимые вещества (гидролиз, окисление, восстановление, реакции двойного обмена и т. п.),. Стабилизатором обычно служит одно из реагирующих веществ. Чтобы образовался коллоидный раствор, а не выпал осадок, нужно, чтобы скорость образования зародышей была больше, чем скорость их роста. Это достигается путем вливания небольшого количества концентрированного раствора одного компонента в очень разбавленный раствор другого компонента при тщательном перемешивании.
Вещество, образующее дисперсную фазу, появляется в системе в результате химической реакции. Чтобы в результате химической реакции образовался коллоидный раствор, а не истинный раствор или осадок, необходимо соблюдение, по крайней мере, трех условий:
1) Чтобы вещество дисперсной фазы было нерастворимо в дисперсионной среде.
2) Чтобы скорость образования зародышей кристаллов дисперсной фазы была гораздо больше, чем скорость роста кристаллов.
Практически это условие выполняется, когда концентрированный раствор одного компонента вливается в сильно разбавленный раствор другого компонента при интенсивном перемешивании.
3) Чтобы одно из исходных веществ было взято в избытке, именно оно одновременно является и стабилизатором.
Методы химической конденсации очень разнообразны, в принципе любая химическая реакция, приводящая к образованию новой фазы, может быть источником получения коллоидного раствора.
2.
Реакция гидролиза
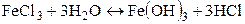 ;
;
Степень гидролиза возрастает с повышением температуры и с увеличением разведения. Возможна следующая схема строения мицелл коллоидного раствора:
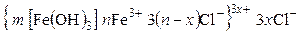 .
.
Реакция двойного обмена
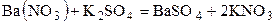 .
.
При проведении реакции в присутствии избытка нитрата бария мицелла коллоидного раствора будет иметь строение:

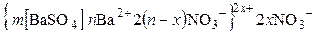 .
.
Так, красный золь золота получают восстановлением натриевой соли золотой кислоты формальдегидом:
NaAuO2 + HCOH + Na2CO3 ––> Au + HCOONa + H2O
Строение мицеллы данного золя можно представить следующей схемой:
{[Au]m· n AuO2–· (n-x) Na+}x– · xNa+
Аналогичным образом получают золь серебра из разбавленных растворов нитрата серебра. Золь серы может быть получен окислением сероводорода кислородом в водном растворе, действием на сероводород сернистого газа либо разложением тиосерной кислоты:
H2S + O2 ––> S + H2O
H2S + SO2 ––> S + H2O
H2S2O3 ––> H2O + SO2 + S
Строение золя серы можно представить схемой:
{[S]m · n HS– · (n-x) H+}x– · x H+
Золи могут быть получены также в результате реакций ионного обмена, в результате которых выделяется нерастворимая соль, образующая при определенных условиях коллоидный раствор; так получают, например, золь иодида серебра.
Процесс гидролиза различных солей может приводить к образованию коллоидных растворов нерастворимых гидроксидов или кислот; так получают, например, золь гидроксида железа(III), имеющий следующее строение:
{[Fe(OH)3]m n FeO+ · (n–x)Cl–}x+ x Cl–
2. Получение коллоидного раствора методом замены растворителя. Этот метод относится к физической конденсации. Он основан на том, что раствор вещества понемногу прибавляют к жидкости, которая хорошо смешивается с растворителем, но в которой растворенное вещество настолько мало растворимо, что выделяется в виде высокодисперсной фазы.
3. Получение коллоидного раствора при помощи конденсации паров. При понижении температуры пар становится пересыщенным и частично конденсируется, образуя дисперсную фазу. Например, при конденсации водяных паров из атмосферы в воздухе образуются туман и облака. Стойкие коллоидные растворы могут образовываться при пропускании паров какого–либо простого вещества в жидкость в результате конденсации.
Метод диспергирования.
Методы измельчения крупных образований до коллоидного состояния подразделяются на механические, физические и физико–химические.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 8457; Нарушение авторских прав?; Мы поможем в написании вашей работы!