
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция №6. «Лекарственные средства на основе элементов III группы ПСЭ»
|
|
|
|
«Лекарственные средства на основе элементов III группы ПСЭ»
К 3 группе лекарственных средств относятся В, Al, Ga, In, Tl. Последний энергетический уровень ns2np1, то есть на последнем энергетическом уровне 3 электрона. Электроны с S подуровня легко переходят на р подуровень. Элементы 3 группы способны проявлять максимальную степень окисления +3. Элементы данной группы способны проявлять восстановительные свойства. В группе сверху вниз металлические свойства увеличиваются, следственно усиливаются восстановительные свойства. Из перечисленных элементов в медицине значения имеют В и Al.
Бор и его соединения:
В природе бор (В) встречается в виде кислородных соединений. Бор входит в состав борной кислоты, которая содержится в воде, горячих источниках вулканических местностей. Его соединения обнаружили в целебных водах Баден-Бадена, в Тверской области. Широко распространены в виде соединения – бура Na2B4O7 • 10 H2O, природный борацит 2 Mg3B8O15 * MgCl2. Богатые залежи соединений на Кавказе (Апшерон). Наиболее характерны для бора кислородные соединения: метаборная кислота НВО2 и ортоборная кислота Н3ВО3.
Соединения бора используются в медицине в качестве дезинфицирующего средства, бор – микроэлемент, который играет большую роль в жизнедеятельности организма: находится в костях, зубах, мышцах, печени, костном мозге, щитовидной железе. Бор ускоряет рост и развитие организма. Бор содержится в коровьем молоке, свекле, желтке, моркови. Бор тормозит окисление адреналина, усиливает действие инсулина, тормозит синтез ферментов в кишечнике. Обмен бора в организме человека тесно связан с обменом калия. Фармакологическим препаратом является борная кислота Н3ВО3. Acidum boricum, источник получения – бура.
t°
Nа2В4О7 + 2 НCl → Н3ВО3 + NаCl + 5 Н2О
(10 Н2О)
Ортоборная кислота – бесцветные чешуйчатые кристаллы. Белый кристаллический порошок без запаха. Бромная кислота плохо растворима в холодной воде. В соотношении 1:5 растворима в спирте и медленнее в глицерине. При температуре более 1000С борная кислота способна терять воду, превращаясь в метаборную кислоту, а более 1800С образует тетраборную кислоту, но при растворении в воде все соединения образуют вновь ортоборную кислоту Н3ВО3. Раствор борной кислоты имеет слабокислую реакцию.
При нейтрализации борной кислоты гидроксидом щелочных металлов образуются соли тетраборной кислоты.
4 Н3ВО3 + 2 NаОН → Nа2В4О7 + 7 Н2О
(Н2В4О7)
солей борной кислоты не существует.
При взаимодействии борной кислоты с глицерином образуются одноосновные комплексные кислоты, имеют более выраженную кислую реакцию:

 ОН НО – СН2 СН2 – ОН НО – СН2
ОН НО – СН2 СН2 – ОН НО – СН2
/ | | |
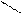 В— ОН + НО – СН → Н СН – О – – О – СН + 2 Н2О
В— ОН + НО – СН → Н СН – О – – О – СН + 2 Н2О
\ | | B |
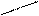 ОН НО – СН2 СН2 – О – – О – СН2
ОН НО – СН2 СН2 – О – – О – СН2
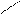 Все растворы натрия тетрабората имеют щелочную реакцию (вследствие гидролиза). Под действием сильных кислот происходит реакция нейтрализации:
Все растворы натрия тетрабората имеют щелочную реакцию (вследствие гидролиза). Под действием сильных кислот происходит реакция нейтрализации:
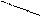
Nа2В4О7 + 2 НCl + 5 Н2О → 2 NаCl + 4 Н3ВО3
эта реакция является исходной для испытаний на подлинность и количественное определение Nа2В4О7. Подлинность борной кислоты определяется по взаимодействию борной кислоты с этанолом с образованием борно-этилового эфира, который горит ярко-зеленым цветом.
ОН НО – С2Н5 О – С2Н5
/ /
В—ОН + НО – С2Н5 → В — О – С2Н5 + 3 Н2О
\ \
ОН НО – С2Н5 О – С2Н5
Для идентификации препарата бора применяют куркумовую бумагу, которая после смачивания окрашивается в розовый или буровато-красный цвет, который после обработки аммиаком переходит в зеленовато-черный.
Количественное определение:
Основано на реакции борной кислоты с глицерином, полученную соль оттитровывают щелочью в присутствии фенолфталеина. Берут смесь свежекипяченой воды и глицерина, которую нейтрализуют по фенолфталеину. Сохранение розовой окраски свидетельствует о достижении точки эквивалентности. Количественное определение проводят метод титрования, где
индикатор – метиленовый оранжевый.
Применение:
Применяют как антисептическое средство в виде 1-3 % растворов для полосканий горла, в мазях и присыпках (в ЛОР-практике).
Хранение:
Хранят в хорошо закупоренных банках, в прохладном месте, по простому списку.
Вопросы:
- Какие соединения III группы ПСЭ представляют наибольший интерес для фармакопеи?
- Какой метод количественного определения применяют для определения содержания борной кислоты?
- Чем обусловлен цвет пламени при горении борноэтилового эфира?
- Укажите применение борной кислоты.
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 1297; Нарушение авторских прав?; Мы поможем в написании вашей работы!