
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция №10
|
|
|
|
«Спирты. Аминоспирты, их производные»
Спирты – это углеводороды, у которых один или несколько атомов «Н» замещены на группу «ОН» (гидроксильную).
Группа «ОН» - функциональная группа спиртов.
Общая формула R-(OH)n
Спирты называют еще алкоголяты.
Классификация спиртов.
I. По количеству «ОН» спирты бывают:
а) одноатомные CH3-CH2-OH – этанол
б) двухатомные СН2-СН2 - этандиол
|
ОН ОН
в) трехатомные СН2 – OH
|
СН - OH - пентантриол
|
СН2 - OH
II. По радикалу «R» спирты бывают:
а) предельные CH3-OH - метанол
б) непредельные CH2=CH-CH-CH3 - бутенол 1
|
OH
 в) ароматические
в) ароматические

 -CH2-OH
-CH2-OH
 бензиловый спирт
бензиловый спирт

 г) гетероциклические
г) гетероциклические
- СН2-ОН фурановый спирт
О
III. По расположению группы «ОН»:
а) первичные CH3-CH2-CH2-OH пропанол 1
б) вторичные CH3-CH-CH3 пропанол 2
|
OH
CH3
|
в) третичные CH3-C-CH3 2 метилпропанол 2
|
OH
В свободном состоянии спирты не встречаются, исключение составляет метанол CH3-OH (древесный уголь).
Однако в соединении с кислотами спирты встречаются довольно часто в виде сложных эфиров.
Плотность всех спиртов меньше 1, т.е. они легче воды. Первые представители ряда спиртов смешиваются с водой в любых отношениях, но с ростом углеродного скелета растворимость падает. Твёрдые спирты С15Н31ОН (цитиловый) плохо растворимы в воде.
Низшие спирты имеют приятный запах, средние спирты имеют неприятный запах, а высшие спирты запаха не имеют.
Фармакопейный интерес представляет этиловый спирт СН3-СН2-ОН Spiritus vini.
Получение:
Существует 2 способа получения:
1) биохимический – брожение. Осуществляется с участием ряда ферментов. Сбраживанию подвергаются моносахариды и полисахариды.
С6Н12О6 → 2 СН3-СН2-ОН + 2 СО2↑
Полученный таким образом спирт носит название спирт-сырец. Его очищают, после чего он носит название спирт-ректификат.
2) химический (синтетический):
а) гидратация алкенов
СН2=СН2 + НОН → СН3-СН2-ОН
б) из галоген-производных
R-Cl + NaOH → R-OH + NaCl
в) гидрирование
О
//
СН3-С + 2 [Н] → CH3-CH2-OH
\\
Н
Этанол обладает приятным запахом и вкусом. Абсолютный спирт готовят при пропускании С2Н5ОН через негашеную известь (СаО) и сульфат меди (СuSO4).
В фармации концентрацию С2Н5ОН выражают в процентах (%). Объемные проценты называют градусами.
Подлинность:
Йодоформеннная реакция
O
//
С2Н5ОН + 4I2 +6 KOH → CHI3↓ + 5KI + H-C + 5H2O
йодоформ \\
светло-желтого OK
цвета, специфический
запах
O
//
3С2Н5ОН + K2Cr2O7 + 3 H2SO4 → 3H3-C + Cr2(SO4)3 + K2SO4 + 7H2O
\
H
сине-фиолетовое
окрашивание
О
||
С2Н5ОН + СН3СООН → С2Н5-О-С-СН3 + H2O
сложный эфир
(уксусно-этиловый), фруктовый запах
Применяют:
- для приготовления настоек,
- как обеззараживающее средство в хирургии.
Этанол в небольших дозах действует опьяняюще, в больших дозах вызывает состояние, близкое к наркозу, иногда заканчивающееся летальным исходом.
В фармации широкое применение находит пропантриол или глицерин.
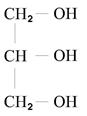
Он был открыт в 18 веке при приготовлении пластыря. В природе широко встречается в виде сложных эфиров высших органических кислот. В настоящее время его получают из пропилена (СН2=СН-СН3).
Глицерин – бесцветная, густая жидкость, сладкая на вкус, растворима в воде, спирте; нерастворима в эфире, хлороформе. Глицерин обладает слабыми кислотными свойствами.
Качественная реакция:

Количественное определение: купринометрический метод.
Наибольшее количество глицерина идет на получение нитрата глицерина.
Нитроглицерин – тринитрат глицерина.
Реакция получения нитроглицерина:

Тринитрат глицерина – тяжелая маслянистая жидкость сладкого вкуса, нерастворима в воде, но растворима в органических растворителях. При легком ударе, сотрясении, при нагревании – взрывается. Глицерин очень ядовит, но в малых дозах ценное лекарственное средство (обладает сосудорасширяющим действием). Хранят по списку «А», в прохладном месте, в проветриваемом помещении.
Аминоспирты – производные фенилалкиламинов и их синтетических аналогов. Все Аминоспирты относятся к группе алкалоидов и выполняют важную роль в организме; в качестве структурных компонентов Аминоспирты содержат пирокатехин (катехоламин).

- ОН
- ОН
Обладает биогенным действием и образуется в организме в результате метаболизма. К аминоспиртам относятся: дофамин, норадреналин, адреналин. В организме выполняют роль нейромедиаторов.
Адреналин – гормон мозгового вещества надпочечников, а дофамин и норадреналин - его предшественники. Впервые адреналин выделил русский ученый Цибульский в конце 19 века, а в 1903 году установлена его химическая формула. После адреналина установили формулу норадреналина.
Общая формула:
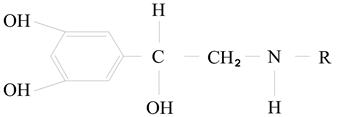
Сырье для получения – надпочечники скота. Гормоны (кортикостероиды) выделяют этанолом, извлекают дихлорэтаном, а в подкисленном состоянии остаются адреналин гидрохлорид и другие, которые осаждают ацетатом свинца. Очистка адреналина – обработка раствором аммиака, потом винной кислотой и получают адреналин тартрат.
В медицине применяют: адреналин гидротартрат – Adrenalini hydrotartrat:
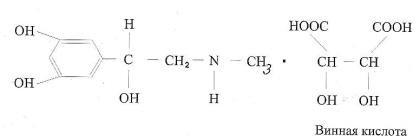
Норадреналин – Noradrenalini hydrotartrat:

Винная кислота
Физические свойства: белые или слегка сероватые порошки без запаха. В медицинской практике применяют аналоги: мезатон и изадрин.
Наличие в молекуле адреналина 2-х ассиметричных атомов углерода обуславливает существование оптических изомеров. Применение находят как D- так и L-изомеры: L-изомеры в 12 раз активнее D-. Наличие первичной формы (норадреналин) или вторичной формы (адреналин) обуславливает их основные свойства и способность образовывать соли, в виде которых они и применяются в медицине. Соли гидрохлориды и гидротартраты получаются друг из друга (замена винной кислоты на соляную и наоборот). Продукты растворимы в воде, нерастворимы в хлороформе, эфире, малорастворимы в этаноле. Как фенолы дают качественную реакцию образования фенолятов. Способны окисляться под действием «О» и света, образует окрашенные продукты окисления.
Цветные реакции на адреналин и его аналоги основаны на окислении продуктов:
1) НТД рекомендует цветную реакцию с FeCl3 – изумрудно-зеленое окрашивание, которое переходит в вишнево-красное под действием аммиака. Мезатон даст фиолетовый цвет.
2) Адреналин и норадреналин восстанавливают серебром и аммиачным раствором, дают положительную реакцию с реактивом Фелинга.
3) Адреналин + 1,2 динитробензол – реакция основана на окислении продуктов в щелочной среде, окислением продуктов в ортохинон.
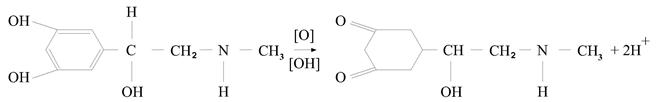
Добавление щелочи дает желто-зеленую флюоресценцию.
4) Под действием хлорамина изадрин - малиновое окрашивание, а мезатон - желтое.
5) Адреналин и норадреналин можно отличить друг от друга по реакции окисления 0, 1 М раствором йода в 2 М буферного раствора. Один буферный раствор рН= 3,5, а другой рН= 6,5. Адреналин – кремово-красное окрашивание. Норадреналин – красно-фиолетовое окрашивание.
6) Все продукты вступают в реакцию азосочетания с образованием окрашенных азосоединений:
1) с альфонитроза β-нафтанолом – красно-бурое окрашивание;
2) с KIO3 в кислой среде – вишнево-красное окрашивание;
3) с нингидрином – желтое (мезатон - красно-фиолетовое).
7) Используют: спектрофотометрический метод.
Количественное определение: по ГФ определение проводят методом неводного титрирования: в среде ледяной уксусной кислоты титруют 0,1 М раствором HClO4 – хлорной кислоты с индикатором кристаллическо-фиолетового или метиленового фиолетового.
Мезатон – броматометрический метод. Мезатон и Изадрин можно определять аргентометрией, т.к. они гидрохлориды.
Хранение: список Б, в защищенном от света месте, в хорошо укупоренной таре из оранжевого стекла или в запаянных ампулах. Для стабилизации к инъекционным растворам адреналина и норадреналина добавляют 0,1% натрия бисульфита, т.к. он обладает восстановительными свойствами.
Применение: в качестве сосудосуживающих средств, адреналин и мезатон расширяют зрачок. Адреналин участвует в регуляции сердечной деятельности, обмене углеводов, выделяется в кровь при стрессе, при снижении АД в результате травм, отравлений, для уменьшения кровотечения при кровопотере.
Мезатон – порошок или раствор для лечения ЛОР-заболеваний.
Изадрин – бронхорасширяющее средство при бронхиальной астме – ингаляция и в таблетках.
Структурно близки к катехоламину некоторые природные и синтетические биологически-активные лекарственные средства.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 5242; Нарушение авторских прав?; Мы поможем в написании вашей работы!