
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Взаимодействие с галогенами
|
|
|
|
Взаимодействие воды с окислителями.
Синтез воды.
Химические свойства воды.
Вода весьма реакционно-способное вещество, взаимодействует с окислами металлов и неметаллов, способна входить в состав координационных соединений в виде лигандов.
Вода подвержена электролитической диссоциации по следующим схемам:
Н2О = Н+ + ОН-
По такой схеме диссоциирует 1 молекула из 5∙109 молекул.
Протон Н+ взаимодействует с молекулой воды, образуя ион гидроксония:
Н+ + Н2О = Н3О +
Ион гидроксония в свою очередь взаимодействует с молекулой воды, образуя гидратированный ион гидроксония Н5О2+.
Н3О + + Н2О = Н5О2+
Существование гидратированных ионов играет важную роль в химических процессах, протекающих в различных системах, в том числе биологических.
Н2 + 1/2 О2 = Н2О - 242 кДж/ моль (для пара),
Н2 + 1/2 О2 = Н2О - 286 кДж / моль (для воды)
При низких температурах в отсутствие катализатора реакция протекает крайне медленно, при повышении температуры до 550°С реакция происходит со взрывом.
Вода окисляется атомарным кислородом с образованием перекиси водорода:
Н2О+О∙ =Н2О2;
Н2О + С12 = НС1 +Н С1О при низких температурах;
Н2О + 2С12 = 4 НС1 + О 2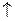 ; при повышенных температурах.
; при повышенных температурах.
4.4.Взаимодействие с углеродом.
При пропускании паров воды через раскаленный уголь образуется так называемый водяной газ:
Н2О + С = СО 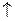 + Н2
+ Н2 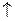 ;
;
4.5. Взаимодействие с соединениями углерода:
Н2О + СО = Н2 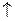 + СО2
+ СО2 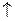
Н2О + СН4 = 3H2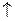 + СО
+ СО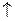 (катализаторы Ni или Со).
(катализаторы Ni или Со).
Эти реакции используются для промышленного получения водорода.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 383; Нарушение авторских прав?; Мы поможем в написании вашей работы!