
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Насыщенный пар
|
|
|
|
Рассмотрим закрытый сосуд, из которого полностью выкачан воздух, и в который налита жидкость. Часть жидкости испарится, и превратится в пар, а оставшееся ее количество будет оставаться неизменным сколь угодно долго. Но процесс испарения прекратиться не может, поэтому должен идти обратный процесс - конденсации, причем скорости процессов испарения и конденсации будут одинаковыми, т.е. система жидкость – пар достигнет состояния динамического равновесия (рис. 3.5.1).

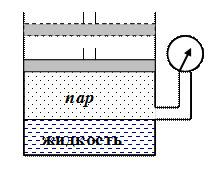
Рис. 3.5.1. Рис. 3.5.2.
Состоянием динамического равновесия между жидкостью и ее паром называется такое состояние, при котором в единицу времени через единицу поверхности число молекул испаряющейся жидкости равно числу молекул, которые конденсируются из пара в жидкость.
Пар, находящийся в динамическом равновесии со своей жидкостью называется насыщенным паром.
Пар, не достигший насыщения, называется ненасыщенным или перегретым паром.
Т.к. в открытом сосуде любая жидкость рано или поздно полностью испарится, то пар в открытом сосуде всегда будет ненасыщенным. Пар в закрытом сосуде можно считать ненасыщенным, если в нем нет следов жидкости. Ненасыщенные пары могут описываться с помощью газовых законов, в том числе и с помощью уравнения Менделеева-Клапейрона, и тем точнее, чем дальше они от насыщения.
Исследуем поведение насыщенного пара при постоянной температуре. В установке, изображенной на рис. 3.5.2, под поршнем находится жидкость со своим насыщенным паром. Если поднять поршень, то манометр в начальный момент после изменения объёма зарегистрирует уменьшение давления насыщенного пара, т.к. уменьшается концентрация его молекул (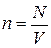 ). В результате уменьшается скорость конденсации и увеличивается скорость испарения, т.е. нарушается динамическое равновесие. Увеличение скорости испарения приводит к дополнительному испарению жидкости и увеличению концентрации молекул пара, что снова приведет к состоянию динамического равновесия при прежней концентрации. Отсюда следует, что давление насыщенного пара, температура которого не изменяется, не зависит от объёма.
). В результате уменьшается скорость конденсации и увеличивается скорость испарения, т.е. нарушается динамическое равновесие. Увеличение скорости испарения приводит к дополнительному испарению жидкости и увеличению концентрации молекул пара, что снова приведет к состоянию динамического равновесия при прежней концентрации. Отсюда следует, что давление насыщенного пара, температура которого не изменяется, не зависит от объёма.
Для описания состояния насыщенного пара нельзя пользоваться газовыми законами, т.к. с изменением объема изменяется и масса пара. Можно приближенно использовать уравнение Менделеева-Клапейрона, в котором стоят масса пара и давление насыщенного пара.
Будем теперь в установке, изображенной на рис. 3.5.2, непрерывно выдвигать поршень до тех пор, пока вся жидкость полностью не испарится; давление насыщенного пара при этом остается постоянным. При дальнейшем выдвижении поршня пар станет ненасыщенным и его давление начнет уменьшаться в соответствие с законом Бойля-Мариотта.
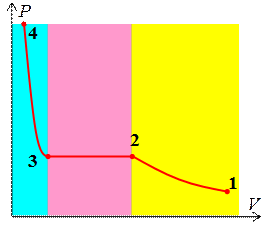
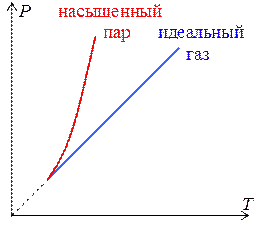
Рис. 3.5.3. Рис. 3.6.1.
Проведем сжатие ненасыщенного пара при постоянной температуре. График зависимости давления от объёма P (V) будет иметь вид, как на рис. 3.5.3. Эта кривая называется изотермой пара или изотермой Эндрюса.
Участок 1-2 изотермы Эндрюса описывает изменение давления ненасыщенного пара и изображается гиперболой 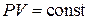 ; участок 2-3, при котором
; участок 2-3, при котором 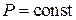 , отвечает двухфазному состоянию насыщенный пар – жидкость; участок 3-4 описывает сжатие жидкости, осуществить которое очень сложно, поэтому этот участок изображается практически вертикальной кривой.
, отвечает двухфазному состоянию насыщенный пар – жидкость; участок 3-4 описывает сжатие жидкости, осуществить которое очень сложно, поэтому этот участок изображается практически вертикальной кривой.
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 904; Нарушение авторских прав?; Мы поможем в написании вашей работы!