
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Число нуклонов в ядре атома элемента равно относительной атомной массе элемента, округленной до целого числа
|
|
|
|
Примеры:
Водород Ar = 1,001; 1 нуклон
Углерод Ar = 12,011; 12 нуклонов.
2.1.3.Нуклиды, изотопы, массовое число
Большинство элементов, содержащихся в природе, состоит из нескольких видов атомов, отличающихся значениями относительной атомной массы.
Пример. Хлор в природе встречается как смесь двух видов атомов, один из которых содержит 18, а другой – 20 нейтронов в ядре.
Каждый вид атомов (вид ядер) называется нуклидом. Нуклид – это вид атомов и ядер, отвечающий определенным числам протонов и нейтронов.
Нуклиды, принадлежащие одному элементу и однозначно определяемые числом протонов, но различающиеся по числу нейтронов, называются изотопными нуклидами, или просто изотопами.
Изотопы элемента – это нуклиды, обладающие равным зарядом ядра (числом протонов). Изотопы элемента различаются только числом нейтронов и, следовательно, общим числом нуклонов.
Пример. Ядра двух природных изотопов хлора содержат по 17 протонов, но 18 и 20 нейтронов, т.е. 35 и 37 нуклонов соответственно.
Для нуклидов точные значения относительных атомных масс всегда близки к целочисленным значениям, поэтому массы нуклидов можно сравнивать по этим значениям, называемым массовыми числами.
Массовое число нуклида равно числу содержащихся в нем нуклонов (сумме протонов и нейтронов).
Для обозначения конкретного нуклида применяется специальная символика. Слева от символа химического элемента верхним индексом указывается массовое число, а нижним индексом – заряд ядра (порядковый номер элемента). Например, изотоп хлора-18 записывается как 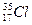 .
.
Таким образом:
Массовое число = Число нуклонов в ядре.
Порядковый номер = Число протонов в ядре или число электронов в оболочке атома.
Разность между массовым числом и порядковым номером = Число нейтронов в ядре.
2.1.4. Строение электронной оболочки атома. Энергетические уровни
Строение электронной оболочки атома определяется различным запасом энергии E отдельных электронов в атоме. В соответствии с моделью атома Бора электроны могут занимать в атоме положения, которым отвечают точно определенные (квантованные) энергетические состояния.
Число электронов, которые могут находиться на отдельном энергетическом уровне, определяется формулой 2n², где n – номер уровня, который обозначается арабскими цифрами 1-7; для обозначения энергетических уровней используются также буквы от K до Q. Максимальное заполнение первых четырех энергетических уровней в соответствии с формулой 2n² составляет: для первого уровня К – 2 электрона, для второго L – 8, для третьего M – 18 и для четвертого уровня N – 32 электрона.
2.2. КВАНТОВО - МЕХАНИЧЕСКОЕ ОБЪЯСНЕНИЕ СТРОЕНИЯ АТОМА
2.2.1. Орбитальная модель атома
Современные квантово-механические представления о строении электронной оболочки атома исходят из того, что движение электрона в атоме нельзя описать определенной траекторией. Можно рассматривать лишь некоторый объем пространства, в котором находится электрон. Поскольку электрон обладает одновременно свойствами частицы и волны, то подходом к объяснению строения электронной оболочки может быть как корпускулярная теория, так и волновая теория; обе они приводят к одинаковому наглядному представлению, сформулированному как орбитальная модель атома.
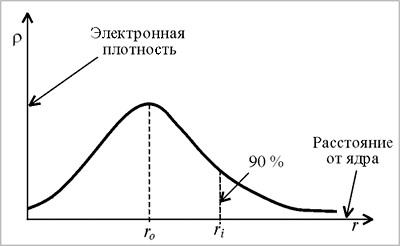
1. Обоснование орбитальной модели атома, исходящее из корпускулярного характера электрона, состоит в следующем. Как следует из рис. 2, вероятность пребывания электрона в атомном ядре равна нулю, она незначительна вблизи ядра, но быстро возрастает при удалении от ядра. На некотором расстоянии вероятность достигает максимума, а затем медленно уменьшается, ассимптотически приближаясь к нулю на расстоянии, стремящемся к бесконечности. Таким образом, невозможно ограничить то пространство, в котором может находиться электрон, т.е. нельзя (без дополнительных условий) указать размеры атома. Исходя из корпускулярного характера электрона можно говорить о 90 %-ой вероятности его пребывания в ограниченном объеме пространства, которое называется атомная орбиталь.
|
| Рис. 2. Зависимость электронной плотности (или вероятности пребывания электрона на расстоянии r ядро-электрон) в атоме от расстояния от ядра |
2. Обоснование орбитальной модели атома, исходящее из волнового характера электрона, состоит в следующем. Электрон заполняет пространство вокруг атомного ядра в форме стоячей волны, которую наглядно можно представить как электронное облако. Плотность электронного облака, понимаемого как облако электрического заряда электрона − электронная плотность – окажется различной и зависящей от расстояния ядро-электрон (рис.1). При ограничении электронной плотности до значения ~ 90 % получается та же орбитальная модель атома.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 1317; Нарушение авторских прав?; Мы поможем в написании вашей работы!