КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
На границе электрод / раствор электролита в ионных д.э.с. возникает скачок потенциала , так называемый гальвани-потенциал
|
|
|
|
При соприкосновении проводников I и II рода, т. е. на границе электрод / раствор электролита может возникать двойной электрический слой (д.э.с.). Наличие д.э.с. приводит к возникновению скачка потенциала на границе фаз.
Лекция 2.2.
Тема: Электродные потенциалы. Типы электродов.
План: 1. Возникновение скачков потенциала на границе фаз. Механизм возникновения э.д.с. электрической цепи; представления о проблемах Вольта и абсолютного скачка потенциала.
2. Строение границы электрод / раствор.
3. Величина и знак электродного потенциала. Зависимость электродного потенциала от концентрации раствора.
4. Электроды I и II рода. Электроды сравнения. Окислительно-восстановительные электроды.
1. Возникновение скачков потенциала на границе фаз. Механизм возникновения э.д.с. электрической цепи; представления о проблемах Вольта и абсолютного скачка потенциала.
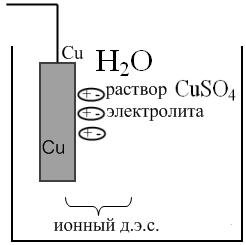
Рассмотрим пути образования д.э.с. на примере медного электрода, погруженного в раствор CuSO4 (водн.).
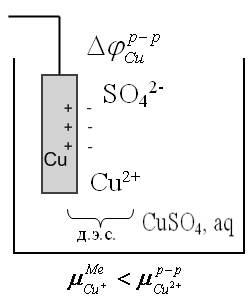
1) пусть концентрация раствора CuSO4 такова, что химический потенциал ионов Cu в металле 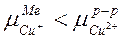 . Тогда при погружении металла в раствор часть ионов Cu2+ из раствора переходит на металл, создав на нем положительный заряд. Положительные ионы Cu2+ на поверхности электрода притянут к себе анионы из раствора SO42-. Образуется ионный д.э. с.
. Тогда при погружении металла в раствор часть ионов Cu2+ из раствора переходит на металл, создав на нем положительный заряд. Положительные ионы Cu2+ на поверхности электрода притянут к себе анионы из раствора SO42-. Образуется ионный д.э. с.
2) пусть концентрация CuSO4 такова, что 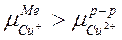 . В этом случае наблюдается обратный процесс: переход ионов Cu2+ из кристаллической решетки металла в раствор и электрод окажется заряженным отрицательно. Отрицательно заряженный электрод из раствора будет притягивать к себе катионы Cu2+ из раствора. При этом также образуется ионный д.э.с.
. В этом случае наблюдается обратный процесс: переход ионов Cu2+ из кристаллической решетки металла в раствор и электрод окажется заряженным отрицательно. Отрицательно заряженный электрод из раствора будет притягивать к себе катионы Cu2+ из раствора. При этом также образуется ионный д.э.с.
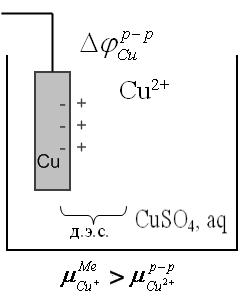 3) пусть концентрация раствора CuSO4 такова, что
3) пусть концентрация раствора CuSO4 такова, что 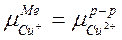 , тогда на границе электрод / раствор не образуется д.э.с.
, тогда на границе электрод / раствор не образуется д.э.с.
Раствор электролита, имеющий концентрацию, при которой химический потенциал ионов в металле и растворе одинаков, называется нулевым раствором.
Потенциал электрода, погруженного в нулевой раствор электролита, называется потенциалом нулевого заряда. Однако, несмотря на отсутствие д.э.с., величина потенциала нулевого заряда не равна нулю 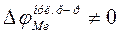 .
.
Рассмотрим основные виды скачков потенциала, возникающих на границе соприкосновения двух фаз:
1. Гальвани-потенциал (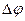 ) – это разность электрических потенциалов между двумя точками в разных фазах. Экспериментально гальвани-потенциал не определяется (т. к. это разность потенциалов между точками в разных фазах, а известно, что экспериментально определить можно между точками в одной фазе).
) – это разность электрических потенциалов между двумя точками в разных фазах. Экспериментально гальвани-потенциал не определяется (т. к. это разность потенциалов между точками в разных фазах, а известно, что экспериментально определить можно между точками в одной фазе).
Гальвани-потенциал может возникать на границе соприкосновения следующих фаз:
а) Гальвани-потенциал на границе Ме1 – Ме2
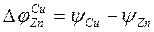
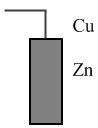 ,
,
где ψCu, ψZn – электрические потенциалы соотносящих металлов.
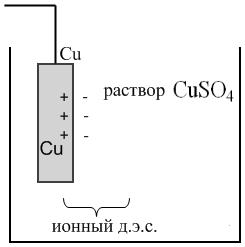 б) Гальвани-потенциал на границе Ме-раствор:
б) Гальвани-потенциал на границе Ме-раствор:
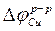 возникает в ионном д.э.с.
возникает в ионном д.э.с.
в) Гальвани-потенциал на границе Ме-диэлектрик:


 Ионный д.э.с. не образуется (
Ионный д.э.с. не образуется (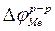 ). Нулевой водный раствор CuSO4 можно рассматривать как диэлектрик – воду. Тогда скачок потенциала на границе металл-диэлектрик (нулевой раствор) обусловлен адсорбцией диполей воды на поверхности электрода.
). Нулевой водный раствор CuSO4 можно рассматривать как диэлектрик – воду. Тогда скачок потенциала на границе металл-диэлектрик (нулевой раствор) обусловлен адсорбцией диполей воды на поверхности электрода.
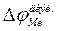 возникает в адсорбционном д.э.с.;
возникает в адсорбционном д.э.с.; 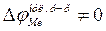 .
.
Тогда можно сказать, что потенциал нулевого заряда равен 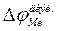 в адсорбционном д.э.с.
в адсорбционном д.э.с.
г) Гальвани-потенциал на границе Ме-вакуум.
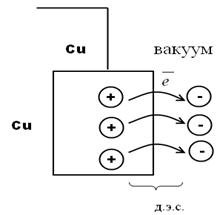 Электроны в металле обладают кинетической энергией при любых Т. Поэтому так называемый электронный газ выходит за пределы кристаллической решетки. На поверхности металла возникает избыточный отрицательный заряд, а изнутри – избыточный положительный. Это приводит к образованию на поверхности металла д.э.с. и следовательно к скачку потенциала
Электроны в металле обладают кинетической энергией при любых Т. Поэтому так называемый электронный газ выходит за пределы кристаллической решетки. На поверхности металла возникает избыточный отрицательный заряд, а изнутри – избыточный положительный. Это приводит к образованию на поверхности металла д.э.с. и следовательно к скачку потенциала  в д.э.с. (за счет выхода электронного газа).
в д.э.с. (за счет выхода электронного газа).
2. Вольта-потенциал (или контактный потенциал) ∆V – это разность потенциалов между двумя точками, находящимися в одной фазе. Измеряют экспериментально как разность потенциалов между двумя точками вблизи поверхностей двух металлов, находящихся в одной (например, вакуум или диэлектрик) фазе. Вольта-потенциал представляет собой алгебраическую сумму гальвани-потенциалов. Существуют следующие типы Вольта-потенциала:
а) Вольта-потенциал на поверхности Ме1-Ме2 в вакууме.
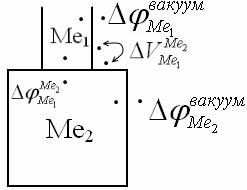 Вольта-потенциал между двумя точками на поверхности двух металлов в вакууму равен сумме внутренней и внешней контактной разности потенциалов:
Вольта-потенциал между двумя точками на поверхности двух металлов в вакууму равен сумме внутренней и внешней контактной разности потенциалов:
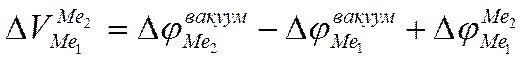
внешняя контактная разность внутренняя контактная
потенциалов между границами разность потенциалов
Ме2-вакуум и Ме1-вакуум. на границе Ме1-Ме2.
б) Вольта-потенциал на поверхности Ме1-Ме2 в диэлектрике (нулевой раствор).
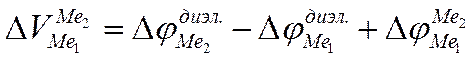
внешняя контактная разность внутренняя контактная
потенциалов разность потенциалов

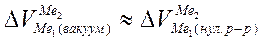
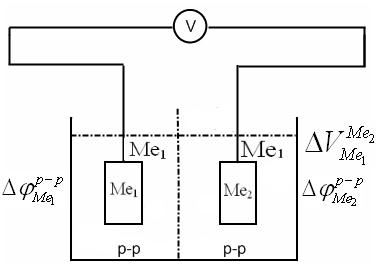
Тогда, согласно современным представлениям, с учетом Вольта- потенциала э.д.с. элемента, состоящего из электродов, опущенных в нулевые растворы (водные) равна сумме разности гальвани-потенциалов в ионных д.э.с. на границе Ме-раствор и Вольта-потенциала на поверхности Ме1-Ме2 в воде:
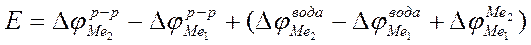
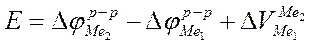
Т. к. величина 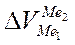 очень мала по сравнению с
очень мала по сравнению с 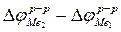 , то при записи его как правило не учитывают
, то при записи его как правило не учитывают
|
Однако знание источника скачков потенциалов еще не означает, что был сразу известен механизм возникновения э.д.с. в электрохимической цепи и сразу было получено уравнение э.д.с. в настоящем виде. Этот вопрос вызвал много споров и привел к возникновению ряда теорий.
Итак, при выяснении вопроса о механизме образования э.д.с. возникли две проблемы: так называемые проблема Вольта и проблема абсолютного скачка потенциала.
Теория Вольта. Суть теории – разность потенциалов на концах электрохимической цепи целиком сосредоточена на границе двух Ме1 и Ме2.

(електрорушійна сила дорівнює Вольта-потенціалу)
Недостатки теории: 1) отрицает наличие скачков потенциала на границе Ме-раствор; 2) учитывает зависимость э.д.с. от природы электрода, но не учла зависимость э.д.с. от концентрации электролита.
Проблема Вольта: в действительности э.д.с. элемента не может определяться только Вольта-потенциалом на границе Ме1-Ме2.
Теория Нернста. Суть теории: 1) скачок потенциала не возникает на границе Ме1-Ме2; 2) скачок потенциала возникает на границе электрод / раствор только в ионных д.э.с.: 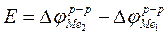 ; 3) потенциал электрода, погруженного в свой нулевой раствор (т. е. потенциал нулевого заряда) равен нулю.
; 3) потенциал электрода, погруженного в свой нулевой раствор (т. е. потенциал нулевого заряда) равен нулю.
Недостатки теории:1) не учитывает скачок потенциала на границе Ме1-Ме2, Ме – диэлектрик (вода); 2) теория объясняет зависимость э.д.с. от концентрации С электролита, но не учитывает природу металла электрода; 3) в действительности потенциал нулевого заряда равен  в адсорбционном д.э.с.; 4) если в элементе один из электродов погружен в свой нулевой раствор, то э.д.с. такого элемента равна абсолютному скачку потенциала в ионном д.э.с. второго электрода:
в адсорбционном д.э.с.; 4) если в элементе один из электродов погружен в свой нулевой раствор, то э.д.с. такого элемента равна абсолютному скачку потенциала в ионном д.э.с. второго электрода:



= 0
Проблема абсолютного скачка потенциала: в действительности э.д.с. элемента не может определяться только абсолютным скачком потенциала в ионном д.э.с., поскольку существует скачок и на границе Ме1-Ме2, и в адсорбционном д.э.с. на границе Ме-вода.
Решить проблему Вольта и абсолютного скачка потенциала удалось русскому ученому А. Н. Фрумкину. Он вывел уравнение э.д.с., в котором учел недостатки теорий Вольта и Нернста:

Согласно этому уравнению, э.д.с. элемента равна разности гальвани-потенциалов в ионных д.э.с. правого и левого электродов плюс Вольта-потенциал, что и соответствует современным представлениям.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 3572; Нарушение авторских прав?; Мы поможем в написании вашей работы!