
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ионное произведение. Водородный показатель
|
|
|
|
Произведение растворимости
Ионное произведение. Водородный показатель.
Электропроводность воды объясняется тем, что вода в очень малой степени диссоциирует, образуя ионы водорода и гидроксид-ионы:
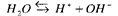
Этот процесс равновесен и, как любой равновесный процесс, его можно охарактеризовать константой равновесия, которая является константой диссоциации:
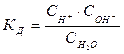 . (49)
. (49)
При комнатной температуре на ионы распадается лишь одна из 108 молекул воды.
Концентрацию молекул воды можно рассчитать, разделив массу 1л воды на массу 1 моля:
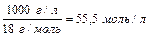 .
.
В разбавленных растворах концентрация воды изменяется очень мало и её можно считать постоянной, тогда
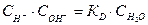 .
.
Так как СН2О - константа, то её вносят в КД и обозначают KW
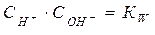 . (50)
. (50)
Эта величина называется ионным произведением воды и представляет собой постоянную величину при данной температуре.
В чистой воде при комнатной температуре концентрации ионов водорода и гидроксид-ионов равны между собой и равны 10-7.мoль/л. Следовательно,
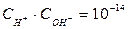 . (51)
. (51)
Константа равновесия Kw зависит от температуры и не зависит от концентраций катионов H + и анионов ОН–.
Если в воду добавить кислоту, то концентрация катионов водорода увеличится, равновесие сместится влево, а концентрация гидроксид-ионов уменьшится так, что ионное произведение воды останется неизменным.
Таким образом, в водных растворах при постоянной температуре концентрации катионов водорода и гидроксид-анионов связаны между собой. При расчетах для водных растворов электролитов используют не концентрации, а активности:
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 340; Нарушение авторских прав?; Мы поможем в написании вашей работы!