
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ионная (гетерополярная) связь
|
|
|
|
Молекула. Химическая связь.
Физика молекулы.
Молекула – это наименьшая частица вещества, обладающая основными его химическими свойствами. Молекулы представляют собой устойчивую систему атомов химически связанных в определенном порядке.
Для химической связи существенное значение имеет лишь электромагнитное взаимодействие электронов и ядер атомов, входящих в состав молекул.
Возможность образования молекулы объясняется тем, что внутренняя энергия молекулы, как устойчивой системы атомов, меньше, чем суммарная энергия атомов, образующих эту молекулу. Разность этих энергий называется энергией образования молекулы или энергией связи.
Единица измерения энергии связи - кДж/моль. Если в молекуле несколько одинаковых связей, то для разрушения каждой последующей потребуется различная энергия. В этом случае говорят о средней энергии связи.
Наиболее часто встречаются молекулы, атомы в которых связаны ионной и ковалентной связью.
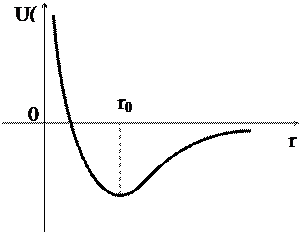 Ионная связь образуется в том случае, если один нейтральный атом способен передать другому один или несколько электронов. Между образовавшимися ионами возникает электростатическое притяжение, которое уравновешивается отталкиванием электронных оболочек.
Ионная связь образуется в том случае, если один нейтральный атом способен передать другому один или несколько электронов. Между образовавшимися ионами возникает электростатическое притяжение, которое уравновешивается отталкиванием электронных оболочек.
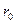 - расстояние между ионами, при котором силы притяжения и силы отталкивания уравновешивают друг друга, этому расстоянию соответствует минимальная энергия взаимодействия,
- расстояние между ионами, при котором силы притяжения и силы отталкивания уравновешивают друг друга, этому расстоянию соответствует минимальная энергия взаимодействия, 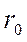 - называется длиной связи.
- называется длиной связи.
Примером ионной связи служит молекула 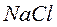 . Электронная конфигурация атома
. Электронная конфигурация атома 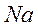 -
- 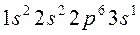 .
. 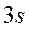 - электрон слабо связан с атомом.
- электрон слабо связан с атомом.
Энергия ионизации атома 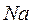 – 5,1 эВ.
– 5,1 эВ.
Электронная конфигурация атома 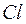 -
-  . Для завершения
. Для завершения 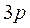 - оболочки атому не хватает одного электрона.
- оболочки атому не хватает одного электрона.
Сродство к электрону у 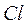 - 3,8 эВ. При сближении атом
- 3,8 эВ. При сближении атом 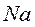 легко отдает электрон атому
легко отдает электрон атому 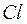 .
.
Образовавшиеся ионы  и
и 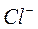 являются сферически симметричными и обладают структурой замкнутых электронных оболочек. Эти ионы притягиваются с помощью кулоновского взаимодействия, энергия которого равна
являются сферически симметричными и обладают структурой замкнутых электронных оболочек. Эти ионы притягиваются с помощью кулоновского взаимодействия, энергия которого равна 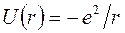 . При сближении ионов абсолютная величина энергии электростатического взаимодействия увеличивается (полная энергия системы понижается), что повышает стабильность молекулы.
. При сближении ионов абсолютная величина энергии электростатического взаимодействия увеличивается (полная энергия системы понижается), что повышает стабильность молекулы.
При достаточно малом расстоянии электронные оболочки ионов начинают перекрываться. Поскольку все 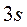 и
и 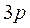 состояния обоих ионов заполнены, то в соответствии с принципом Паули некоторые из электронов должны перейти в более высокие состояния (например,
состояния обоих ионов заполнены, то в соответствии с принципом Паули некоторые из электронов должны перейти в более высокие состояния (например, 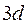 или
или 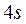 ).
).
При перекрывании электронных оболочек возникают силы отталкивания. Энергия такого взаимодействия пропорциональна 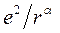 , где
, где 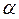 некоторое число от 8 до 12. Видно, что энергия взаимодействия определяется в основном энергией кулоновского притяжения и деформация ионов незначительна.
некоторое число от 8 до 12. Видно, что энергия взаимодействия определяется в основном энергией кулоновского притяжения и деформация ионов незначительна.
Для образования иона  требуется энергия 5,1 эВ, а при присоединении электрона к атому
требуется энергия 5,1 эВ, а при присоединении электрона к атому 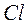 выделяется энергия 3,8 эВ. Таким образом, энергия, необходимая для образования молекулы
выделяется энергия 3,8 эВ. Таким образом, энергия, необходимая для образования молекулы 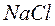 , равна 5,1 – 3,8 = 1,3 эВ. При сближении ионов до равновесного состояния (
, равна 5,1 – 3,8 = 1,3 эВ. При сближении ионов до равновесного состояния (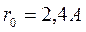 ) энергия системы вследствие электростатического притяжения понижается примерно на 6 эВ. В результате энергия молекулы оказывается ниже энергии исходного состояния на 6,0 – 1,3 = 4,7 эВ, что и представляет собой энергию связи молекулы
) энергия системы вследствие электростатического притяжения понижается примерно на 6 эВ. В результате энергия молекулы оказывается ниже энергии исходного состояния на 6,0 – 1,3 = 4,7 эВ, что и представляет собой энергию связи молекулы 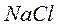 . Образование молекулы
. Образование молекулы 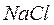 энергетически выгодно.
энергетически выгодно.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 472; Нарушение авторских прав?; Мы поможем в написании вашей работы!