
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теория метода валентных связей
|
|
|
|
Метод разработан В. Гейтлером и Дж. Лондоном. Большой вклад в его развитие внесли также Дж. Слейтер и Л. Полинг.
Основные положения метода валентных связей:
1. Химическая связь образуется двумя валентными электронами различных атомов с антипараллельными спинами. При этом происходит перекрывание электронных облаков и между атомами возникает зона с повышенной электронной плотностью. Это приводит к уменьшению потенциальной энергии системы.
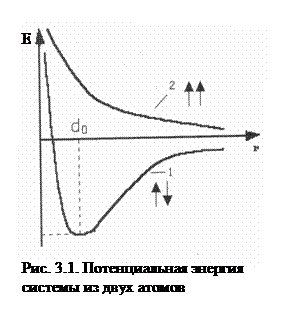 Основатели метода валентных связей Гейтлер и Лондон (1927г.) рассчитали потенциальную энергию системы, состоящей из двух атомов водорода (два протона и два электрона). Для расчета энергетического состояния электронов в молекуле водорода было использовано уравнение Шредингера для двух вариантов: а) спины электронов сближающихся атомов антипараллельны, ↑↓; б) спины электронов сближающихся атомов параллельны, ↑↑ (рис. 3.1).
Основатели метода валентных связей Гейтлер и Лондон (1927г.) рассчитали потенциальную энергию системы, состоящей из двух атомов водорода (два протона и два электрона). Для расчета энергетического состояния электронов в молекуле водорода было использовано уравнение Шредингера для двух вариантов: а) спины электронов сближающихся атомов антипараллельны, ↑↓; б) спины электронов сближающихся атомов параллельны, ↑↑ (рис. 3.1).
Проведенный расчет показал, что:
а) при сближении двух атомов водорода с антипараллельными спинами (кривая 1) на расстояние d0 система имеет минимальную энергию; cледовательно, в этом случае образуется устойчивая химическая связь с энергией Есв. и длиной связи ℓ: ℓ = 0,074 нм < 2а0 = 0,106 нм (а0 – радиус атома водорода);
б) если спины электронов паралельны (↑↑), энергия системы при любом расстоянии между сближающимися атомами больше, чем сумма энергий двух отдельных атомов (кривая 2) и образование химической связи невозможно.
2. В пространстве связь располагается по направлению, в котором возможность перекрывания электронных облаков наибольшая. Из нескольких связей, образуемых данным атомом, наиболее прочной будет та связь, у которой перекрывание атомных орбиталей наибольшее.
3. Количество электронов, отдаваемых атомом на образование связи, определяет его валентность.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 281; Нарушение авторских прав?; Мы поможем в написании вашей работы!