
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Векторная модель атомов
|
|
|
|
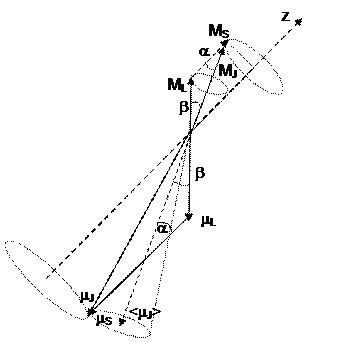 Движение электронов в других атомах (помимо H) определяется теми же квантовыми числами (можно и n, l, j, mj). Но влияние на движение электрона других электронов приводит к тому. Что его энергия зависит и от числа l (кроме n).
Движение электронов в других атомах (помимо H) определяется теми же квантовыми числами (можно и n, l, j, mj). Но влияние на движение электрона других электронов приводит к тому. Что его энергия зависит и от числа l (кроме n).
Механические и магнитные моменты атомов складываются из орбитальных и спиновых моментов отдельных электронов.
Возможны два случая:
1. Если орбитальные моменты 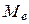 связаны между собой сильнее, чем с
связаны между собой сильнее, чем с 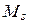 и наоборот (такая связь называется LS -связью), то все моменты
и наоборот (такая связь называется LS -связью), то все моменты 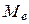 складываются в суммарный орбитальный момент атома
складываются в суммарный орбитальный момент атома 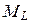 , а все
, а все 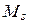 в суммарный спиновый момент
в суммарный спиновый момент 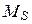 . А потом находится полный момент атома
. А потом находится полный момент атома 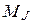 .
.
Результирующий орбитальный момент импульса для SL- связи
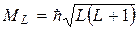
где L – орбитальное квантовое число атома.
Для двух электронов 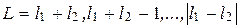
Проекция момента импульса атома на некоторое напр-е
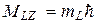
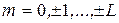
Также и для полного спинового момента

S – в зависимости от четного или нечетного числа электронов
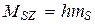
Тогда полный орбитальный момент атома


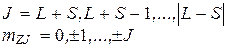
Векторная модель строится по следующим правилам. Пусть известен модель момента импульса и его одна проекция М и Мz (Мx и Мy – не определены). Следовательно, 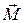 может иметь направление одной из образующих конуса (совершает прецессию).
может иметь направление одной из образующих конуса (совершает прецессию).
То, что проекция полного момента атома квантуется, было доказано опытами в 1922 году Штерном и Герлихом.
Состояние электронов в атомах позволяет объяснить принцип Паули (1925 г.): в одном и том же атоме (или другой квантовой системе) не может быть двух электронов (либо других частиц со спином 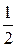 ), обладающих одинаковой совокупностью квантовых чисел. (В одном и том же состоянии не могут находится 2 электрона).
), обладающих одинаковой совокупностью квантовых чисел. (В одном и том же состоянии не могут находится 2 электрона).
Тогда кратность выражения уровня будет определяться 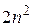
| Оболочка | |||
| На уровне с энергией | n = 1 | 2 эл. | K |
| n = 2 | 8 эл. | L | |
| n = 3 | 18 эл. | M | |
| n = 4 | 32 эл. | N | |
| n = 5 | 50 эл. | O | |
| P |
Принцип Паули дает объяснение периодической повторяемости свойств атомов.
Принцип запрета Паули
Состояние электронов в атомах позволяет объяснить принцип Паули (1925 г.): в одном и том же атоме (или другой квантовой системе) не может быть двух электронов (либо других частиц со спином 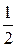 ), обладающих одинаковой совокупностью квантовых чисел. (В одном и том же состоянии не могут находится 2 электрона).
), обладающих одинаковой совокупностью квантовых чисел. (В одном и том же состоянии не могут находится 2 электрона).
В таблице все возможные квантовые состояния атома водорода и соответствующие им ориентации орбитального 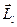 и спинового
и спинового 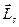 моментов электрона. Стрелками обозначены направления векторов. Учет приводит к тому, что уровни энергий, описываемые формулой (
моментов электрона. Стрелками обозначены направления векторов. Учет приводит к тому, что уровни энергий, описываемые формулой (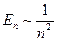 ), расщепляются на несколько уровней, соответствует нескольким значениям
), расщепляются на несколько уровней, соответствует нескольким значениям 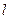 и
и 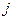 .
.
Распределение электронной плотности для состояний с заданным главным числом 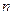 , но с разными значениями орбитального
, но с разными значениями орбитального 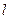 и магнитного
и магнитного  - квантовых чисел, существенно отличаются. Хотя, согласно формуле (
- квантовых чисел, существенно отличаются. Хотя, согласно формуле (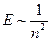 ), им соответствует одна и та же энергия (
), им соответствует одна и та же энергия ( ).
).
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 767; Нарушение авторских прав?; Мы поможем в написании вашей работы!