
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Углеводы. Спирты - производные предельных или непредельных углеводородов, в молекулах которых один или несколько атомов водорода заменены гидроксильными группами
|
|
|
|
Cпирты
Спирты - производные предельных или непредельных углеводородов, в молекулах которых один или несколько атомов водорода заменены гидроксильными группами.
Одноатомные спирты
СН4 - метан СН3 ─ ОН - метанол
СН3 ─СН3 - этан СН3 ─ СН2 ─ ОН - этанол
Многоатомные спирты
СН2 ─СН2 СН2 ─СН ─СН2
│ │ │ │ │
ОН ОН ОН ОН ОН
этиленгликоль глицерин
Подобно молекулам воды, молекулы низших спиртов связываются между собой водородными связями. Поэтому они имеют более высокие температуры кипения, чем углеводороды, производными которых они являются, и чем другие углеводороды с таким же составом и молекулярной массой, но не содержащие гидроксильных групп. Спирты практически не являются электролитами.
Химические свойства
1. Взаимодействие с металлами
2СН3 ─ СН2─ ОН + 2Na → 2СН3 ─ СН2─ ОNa + H2↑
этиловый спирт этилат натрия
Алкоголяты легко гидролизуются
СН3 ─ СН2─ ОNa + H2О → СН3 ─ СН2─ ОН + NaОН
2. Образование эфиров (взаимодействие с кислотами)
СН3 ─ ОН + НО ─ NO2 ↔ СН3 ─ О ─ NO2 + H2О
метиловый азотная метиловый эфир
спирт кислота азотной кислоты
3. Окисление (проходит легче, чем у соответствующих углеводородов)
3СН3 ─ СН2 ─ ОН + K2Cr2O7 + 4H2SO4 →3СН3─С ─Н + Сr2(SO4)3 + K2SO4 +7H2O
этиловый спирт ║
O
уксусный альдегид
5СН3─ СН─СН3 + 2KMnO4 + 3H2SO4→5СН3─ С─СН3 + 2MnSO4 + K2SO4 + 8 H2O
│ ║
OH O
изопропиловый спирт диметилкетон (ацетон)
Альдегиды и кетоны (карбонильные соединения)
В молекулах этих соединений содержится двухвалентная карбонильная группа >С=О.
Н ─С─Н СН3 ─С ─Н
║ ║
О О
муравьиный альдегид уксусный адьдегид
СН3─ С─СН3 СН3 ─СН2─С─СН3
║ ║
O O
диметилкетон метилэтилкетон
Альдегиды, в отличии от кетонов легко окисляются:
2СН3 ─С ─Н + О2 → 2СН3 ─С ─ОН
║ ║
О О
уксусный альдегид уксусная кислота
СН3 ─С ─Н + Ag2O → СН3 ─С ─ОН +2Ag
║ ║
О О
СН3 ─С ─Н + CuO → СН3 ─С ─ОН + Cu2O
║ ║
О О
Муравьиный альдегид (формальдегид) СН2=О - газ с резким запахом, хорошо растворим в воде, 40% водный раствор - формалин применяется для дезинфекции, консервирования препаратов и др., используется для производства формальдегидных смол.
Уксусный альдегид (ацетальальдегид) СН3─СН=О. Легко кипящая бесцветная жидкость (темп.кип. 210С), с характерным запахом прелых яблок, хорошо растворима в воде.
Ацетон, или диметилкетон, СН3─СО─СН3. Бесцветная жидкость с характерным запахом (темп. кип. 56,2 0С); смешивается с водой во всех соотношениях. Очень хороший растворитель многих органических веществ. Широко применяется в лакокрасочной промышленности, в производстве некоторых видов искусственного волокна, небьющегося органического стекла, кинопленки, бездымного пороха, для растворения ацетилена (в баллонах).
К углеводам относятся сахара и вещества, превращающиеся в них при гидролизе.
Углеводы подразделяются на моносахариды, дисахариды и полисахариды.
Моносахариды - простейшие углеводы, они не подвергаются гидролизу - не расщепляются водой на более простые углеводы.
Глюкоза, или виноградный сахар, С6Н12О6 - важнейший из моносахаридов; белые кристаллы сладкого вкуса, легко растворяющиеся в воде.
Глюкоза является шестиатомным альдегидоспиртом; строение ее можно представить формулой:
Н Н ОН Н Н
│ │ │ │ │
НОСН2 ─С ─ С ─ С ─ С─С=О
│ │ │ │
ОН ОН Н ОН
Фруктоза, или плодовый сахар, С6Н12О6 - моносахарид, спутник глюкозы во многих плодовых и ягодных соках; значительно слаще глюкозы; в смеси с ней входит в состав меда. Представляет собой шестиатомный кетоноспирт; строение фруктозы отражает формула:
Н Н ОН О
│ │ │ ║
НОСН2 ─С ─ С ─ С ─ С─СН2ОН
│ │ │
ОН ОН Н
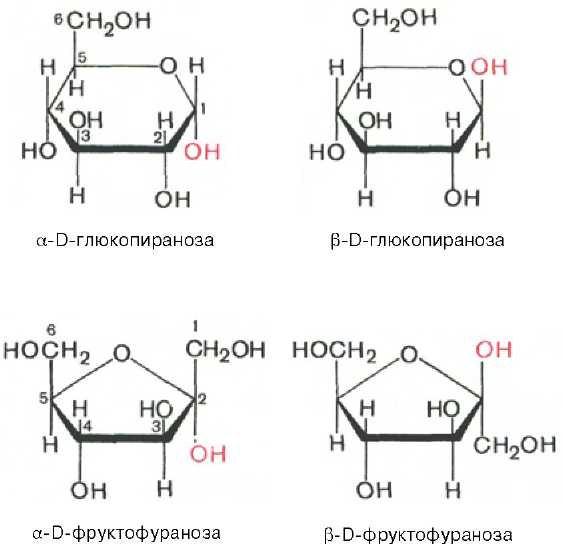
Моносахариды существуют и вступают в реакции не только в открытой цепной форме, но еще и в циклических формах. Моносахариды как альдегидо- или кетоноспирты являются соединениями со смешенными функциями, природа их усложнена возможностью внутримолекулярных взаимодействий спиртовых гидроксильных групп с альдегидной или кетонной карбонильной группой. В результате замыкается шестичленное, содержащие атом кислорода кольцо и образуются 2 циклические α- и β-формы глюкозы, отличающиеся пространственным расположением атома Н и группы ОН при 1 -ом С- атоме (для фруктозы также существуют 2 циклические формы).
Дисахариды - углеводы, которые при нагревании с водой в присутствии минеральных кислот или под влиянием ферментов подвергаются гидролизу, расщепляясь на 2 молекулы моносахаридов.
Сахароза С12Н22О11
С12Н22О11 + Н2О → С6Н12О6 + С6Н12О6
сахароза глюкоза фруктоза
Полисахариды. Эти углеводы во многом отличаются от моно- и дисахаридов - не имеют сладкого вкуса, в большинстве нерастворимы в воде; они представляют собой сложные высокомолекулярные соединения, которые под каталитическим влиянием кислот или ферментов подвергаются гидролизу с образованием более простых полисахаридов и, в конечном итоге, множества (сотен и тысяч) молекул моносахаридов. Важнейшие представители полисахаридов - крахмал и целлюлоза (клетчатка). Их молекулы построены из звеньев ─С6Н10О5 ─, являющихся остатками шестичленных циклических форм молекул глюкозы, потерявших молекулы воды; поэтому состав и крахмала, и целлюлозы выражается общей формулой (С6Н10О5)х. Различие же в свойствах этих полисахаридов обусловлено пространственной изомерией, образующих их моносахаридных молекул: крахмал построен из α-формы, а целлюлозы - β-формы глюкозы.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 777; Нарушение авторских прав?; Мы поможем в написании вашей работы!