
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Поведение полимеров в растворах
|
|
|
|
До середины 30-х годов ХIХ века существовали различные точки зрения на природу растворов ВМС. Одни исследователи считали, что растворы ВМС –истинные растворы, другие утверждали, что эти растворы являются типичными коллоидами, т. е. дисперсными системами. Разногласия объяснялись тем, что растворы ВМС обладают свойствами не только истинных растворов (самопроизвольность образования раствора, его термодинамическая устойчивость, молекулярная дисперсность, гомогенность), но и свойствами коллоидных растворов (неспособность молекул полимера проникать через полупроницаемую мембрану, низкое осмотическое давление, малые скорости диффузии молекул, светорассеяние). Когда же прояснился вопрос о размерах молекул ВМС, разногласия были исчерпаны. Оказалось, что свойства растворов ВМС, общие с коллоидными растворами, обусловлены соизмеримостью молекул полимеров и коллоидных частиц.
Полимеры, подобно низкомолекулярным веществам, в зависимости от условий получения раствора (природа полимера и растворителя, температура и др.) могут образовывать как коллоидные, так и истинные растворы. В целом растворы полимеров - это растворы молекулярного типа (истинные). Следует отметить, что вследствие больших размеров молекул и особенностей их строения, растворы ВМС обладают рядом специфических свойств:
1. Равновесные процессы в растворах ВМС устанавливаются медленно.
2. Процессу растворения ВМС, как правило, предшествует процесс набухания.
3. Растворы полимеров не подчиняются законам идеальных растворов, т. е. законам Рауля и Вант-Гоффа.
4. При течении растворов полимеров возникает анизотропия свойств (неодинаковые физические свойства раствора в разных направлениях) за счет ориентации молекул в направлении течения.
5. Высокая вязкость растворов ВМС.
6. Молекулы полимеров, благодаря большим размерам, проявляют склонность к ассоциации в растворах. Время жизни ассоциатов полимеров более длительное, чем ассоциатов низкомолекулярных веществ.
Набухание и растворение полимеров
Процесс растворения ВМС протекает самопроизвольно, но в течение длительного времени, и ему часто предшествует набухание полимера в растворителе. Полимеры, макромолекулы которых имеют симметричную форму, могут переходить в раствор, предварительно не набухая. Например, гемоглобин, печеночный крахмал – гликоген при растворении почти не набухают, а растворы этих веществ не обладают высокой вязкостью даже при сравнительно больших концентрациях. В то время, как вещества с сильно асимметрическими вытянутыми молекулами при растворении очень сильно набухают (желатин, целлюлоза, натуральный и синтетические каучуки).
Набухание – это увеличение массы и объема полимера за счет проникновения молекул растворителя в пространственную структуру ВМС. Причиной набухания является большая разница в размерах молекул растворяемого вещества и растворителя и, как следствие этого, большое различие в скоростях их диффузии. Поэтому при набухании вначале происходит практически односторонняя диффузия молекул растворителя в пространственную сетку полимера, имеющая ту же природу, что и осмос растворителя в осмотическую ячейку через поры полупроницаемой мембраны. Оба процесса вызываются стремлением системы к выравниванию концентраций компонентов.
Механизм набухания сводится к проникновению молекул растворителя в ближайшие слои полимера и сольватации соответствующих участков полимерной цепи. В результате этого макромолекулы «разрыхляются», что облегчает дальнейшее проникновение молекул растворителя и увеличение массы и объема полимера.
Различают два вида набухания: неограниченное, заканчивающееся полным растворением ВМС (например, набухание желатины в воде, каучука в бензоле, нитроцеллюлозы в ацетоне) и ограниченное, приводящее к образованию набухшего полимера – студня (например, набухание целлюлозы в воде, желатина в холодной воде, вулканизованного каучука в бензоле). Студень представляет собой пространственную сетку, состоящую из связанных между собой макромолекул полимера и заполненную молекулами растворителя.
Степень ограниченности процесса набухания и возможность самопроизвольного растворения определяются соотношением энергии связи в решетке полимера и энергии сольватации полимерной цепи с учетом энтропийного фактора.
Весь процесс набухания и растворения ВМС можно условно разделить на ряд стадий (рис. 1).
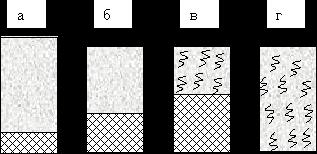
Рис 1. Последовательные стадии (а – г) растворения ВМС в низкомолекулярной жидкости
На начальной стадии (рис.1а) система состоит из двух компонентов: полимера и низкомолекулярной жидкости. Переход а→б характеризуется интенсивным проникновением молекул низкомолекулярной жидкости в структуру полимера и сольватацией полимерной цепи, сопровождающийся выделением теплоты (ΔН<0). Изменение энтропии по сравнению с энтальпийным фактором незначительно. При этом объем полимера возрастает, но общий объем системы полимер-растворитель уменьшается. Это явление называется контракцией, а выделение теплоты говорит о физико-химической природе процесса.
Переход б→в представляет собой начальный этап распределения макромолекул полимера по всему объему растворителя и характеризуется возрастанием энтропии системы вследствие роста числа возможных конформаций. Энтальпия системы если и изменяется, то незначительно. На данном этапе происходит обычно основное увеличение объема и массы полимера. Это результат дальнейшего проникновения молекул растворителя в полимерную сетку, ее разрыхление и связанное с этим частичное освобождение макромолекул. Отдельные макромолекулы начинают отрываться друг от друга и переходить в слой низкомолекулярной жидкости.
Ограниченное набухание заканчивается на стадии б или в образованием студня. Дальнейшее развитие процесса – неограниченное набухание – приводит к растворению полимера, т. е. образованию раствора ВМС (рис.1г). Переход в→г происходит в результате сил диффузии и характеризуется значительным увеличением энтропии системы. При этом макромолекулы ВМС равномерно распределяются по всему объему низкомолекулярного растворителя, образуя истинный раствор. Так как растворение полимеров главным образом обусловлено ростом энтропии, то и устойчивость растворов ВМС объясняется в основном энтропийным фактором.
Набухание и, следовательно, растворение ВМС зависят от природы растворителя и полимера, строения макромолекул полимера, температуры, присутствия электролитов, а также от рН среды (для полиэлектролитов).
Процессы набухания и растворения ВМС являются избирательными процессами. Другими словами для образования раствора ВМС необходимо его сродство с растворителем (лиофильность). Неполярные полимеры хорошо набухают (растворяются) в неполярных растворителях (каучук в бензоле или бензине) и не набухают в полярных. Полярные полимеры лучше набухают (растворяются) в полярных жидкостях (белок в воде) и не набухают в неполярных. Ввиду сродства полимера с растворителем, при набухании и растворении большая часть растворителя “связывается” в сольватные (гидратные) оболочки. Особенно это характерно для полярных макромолекул в водной среде. И поскольку макромолекулы обладают большой поверхностью, то для неограниченного набухания (растворения) даже в лиофильной системе требуется достаточное количество жидкости. Иначе процесс набухания может остановиться на стадии ограниченного набухания, т. е. образования студня.
Существенную роль в набухании играет строение макромолекул полимера. Например, полимеры с длинными жесткими цепями и большим количеством полярных групп хорошо набухают, но не растворяются даже в соответствующем растворителе (целлюлоза в воде). Если полимер растворяется в жидкости не достаточно хорошо, то также образуется студень.
Вязкость растворов ВМС
Вязкость жидкости можно определить как сопротивление жидкости передвижению одного её слоя относительно другого. Любое перемещение одной части жидкости относительно другой тормозится силами притяжения между её элементами. Иначе говоря, вязкость жидкости характеризует внутреннее трение, возникающее при перемещении слоев жидкости относительно друг друга.
Растворы ВМС только при очень больших разбавлениях (~0,01%) подчиняются законам Ньютона и Пуазейля. Характерной особенностью растворов ВМС является их высокая вязкость по сравнению с чистым растворителем даже при малых концентрациях.
Вязкостью (внутренним трением) называют свойство жидкостей оказывать сопротивление действию внешних сил, вызывающих их течение. Помимо этого растворы ВМС не являются ньютоновскими жидкостями, так как величина их вязкости (η) зависит от напряжения сдвига (р) - отношения тангенциально приложенной к образцу силы к единице поверхности (рис. 2).
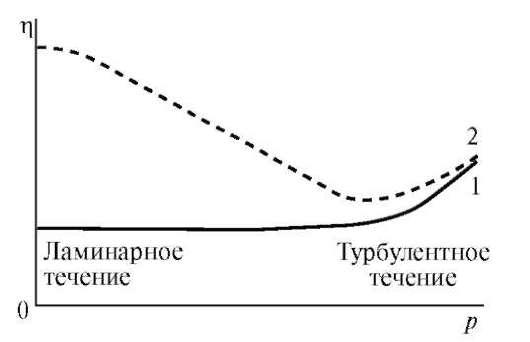
Рис. 2. Зависимость вязкости растворов низкомолекулярных веществ ньютоновских жидкостей (1) и растворов ВМС (2) от напряжения сдвига
Причины аномалии вязкости заключаются в наличии структурной вязкости у подобных систем. Структурная вязкость - это дополнительная вязкость, обусловленная добавочным сопротивлением течению со стороны внутренних надмолекулярных пространственных структур - сеток, нитей, крупных капель эмульсий. Вязкость таких систем не остается постоянной при увеличении напряжения сдвига, а резко падает, пока не достигает постоянной величины, но на более низком уровне вследствие разрушения структуры (рис. 3).
Особенно сильно это свойство проявляется у полимеров с длинными линейными молекулами, например у каучука. Растворы полимеров с той же молекулярной массой, но со сферической формой молекул имеют меньшую вязкость. Отсюда следует, что вязкость растворов полимеров возрастает пропорционально асимметрии их молекул. При одинаковой химической структуре вязкость возрастает с увеличением молекулярной массы. Она зависит также от концентрации полимера и межмолекулярных сил взаимодействия.
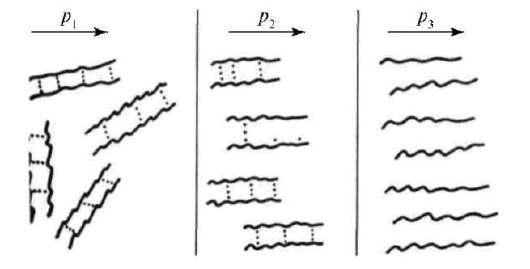
Рис. 3. Изменение структуры растворов ВМС при увеличении напряжения сдвига
Область постоянства вязкости аномально вязких жидкостей называют псевдопластической областью. Дальнейшее повышение напряжения сдвига вызывает увеличение коэффициента вязкости, что связано с турбулентностью.
Экспериментальные данные показывают, что коллоидные аномально вязкие системы могут течь и при очень малых давлениях и при этом вязкость остается постоянной, но очень высокой. Такое течение называют ползучестью.
Увеличение давления резко снижает вязкость ползучих систем, пока не наступает вторая область постоянства вязкости - псевдопластическая.
Аномалии вязкости вызываются рядом причин.
1. Структурообразование - процесс агрегации частиц коллоидных растворов, суспензий, растворов ВМС и образования пространственных легкоразрушимых структур.
2. Изменение ориентации в потоке частиц удлиненной формы и макромолекул при увеличении градиента скорости.
3. Деформация клубков макромолекул полимера или капель эмульсий в потоке.
С повышением температуры вязкость структурированных систем резко уменьшается за счет разрушения структуры. При понижении температуры доля структурной вязкости значительно увеличивается.
Агрегативная устойчивость растворов ВМС и ее нарушение
Растворы ВМС агрегативно устойчивы, как и истинные растворы. Однако при введении больших количеств электролитов наблюдается выделение ВМС из раствора. Но это не следует отождествлять с коагуляцией типичных коллоидных систем. Коагуляция золей происходит при введении сравнительно небольших количеств электролита и представляет собой обычно необратимое явление. Выделение же из раствора ВМС происходит при добавлении относительно больших количеств электролита и является обычно обратимым процессом. После удаления из осадка электролита промыванием или диализом ВМС снова способно к растворению.
Коагуляция золей происходит за счет сжатия двойного электрического слоя и исчезновения заряда на поверхности частицы. Выделение из раствора полимера при добавлении электролита объясняется уменьшением растворимости ВМС в концентрированном растворе электролита. Такое явление называется высаливанием.
Считается, что при высаливании молекулы растворенного вещества вытесняются из электрического поля введенных ионов, которые связываются с полярными молекулами растворителя. Таким образом, высаливание принципиально не отличается от выделения ВМС из раствора при добавлении нерастворителя. Как правило, высаливающее действие ионов изменяется соответственно тому порядку, в каком они стоят в лиотропном ряду. Так, катионы по мере уменьшения их высаливающей способности могут быть расположены в ряд:
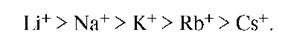
Подобный же ряд анионов имеет вид:
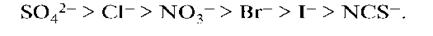
Взаимосвязь между высаливающим действием и местом иона в лиотропном ряду вполне понятна: чем больше ион способен связывать растворитель, тем больше он будет уменьшать способность среды растворять ВМС.
Высаливание лежит в основе одного из методов фракционирования ВМС, поскольку способность этих соединений выделяться из раствора весьма сильно зависит от их химической природы и резко возрастает с увеличением молекулярной массы. Особенно широко применяется фракционирование с помощью высаливания при разделении белков. При этом высаливание часто сочетают с введением в систему нерастворителя (спирт) и охлаждением раствора. Высаливание белков целесообразно проводить при значении pH, близком к изоэлектрической точке, так как при значении pH, большем или меньшем изоэлектри-ческой точки, возрастают заряд и гидратация белковых молекул и увеличивается их растворимость.
В растворах ВМС при изменении температуры, pH или при введении низкомолекулярных веществ иногда наблюдается явление коацер-вации. Это явление заключается в разделении системы на две фазы, из которых одна представляет собой раствор ВМС в растворителе, а другая - раствор растворителя в ВМС. Раствор, более богатый ВМС, обычно выделяется в виде мельчайших капелек.
Условия кристаллизации полимеров
Полимеры могут существовать в кристаллическом и аморфном состояниях. Необходимое условие кристаллизации — регулярность достаточно длинных участков макромолекулы. В кристаллических полимерах возможно возникновение разнообразных надмолекулярных структур (фибрилл, сферолитов, монокристаллов и др.), тип которых во многом определяет свойства полимерного материала. Надмолекулярные структуры в незакристаллизованных (аморфных) полимерах менее выражены, чем в кристаллических.
Незакристаллизованные полимеры могут находиться в трёх физических состояниях: стеклообразном, высокоэластическом и вязкотекучем. Полимеры с низкой (ниже комнатной) температурой перехода из стеклообразного в высокоэластическое состояние называются эластомерами, с высокой — пластиками. В зависимости от химического состава, строения и взаимного расположения макромолекул свойства полимеров могут меняться в очень широких пределах. Так, 1,4-цис-полибутадиен, построенный из гибких углеводородных цепей, при температуре около 20 °С — эластичный материал, который при температуре — 60 °С переходит в стеклообразное состояние; полиметилметакрилат, построенный из более жёстких цепей, при температуре около 20 °С — твёрдый стеклообразный продукт, переходящий в высокоэластическое состояние лишь при 100 °С. Целлюлоза — полимер с очень жёсткими цепями, соединёнными межмолекулярными водородными связями, вообще не может существовать в высокоэластическое состоянии до температуры её разложения. Большие различия в свойствах полимеров могут наблюдаться даже в том случае, если различия в строении макромолекул на первый взгляд и невелики. Так, стереорегулярный полистирол — кристаллическое вещество с температурой плавления около 235 °С, а нестереорегулярный (атактический) вообще не способен кристаллизоваться и размягчается при температуре около 80 °С.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 2368; Нарушение авторских прав?; Мы поможем в написании вашей работы!