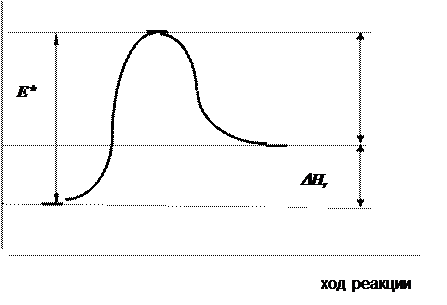КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теория переходного состояния. Активированный комплекс
|
|
|
|
Расчёты показывают, что для многих химических реакций, если они протекают по механизму непосредственного превращения молекул исходных веществ в продукты, энергии, сообщаемой молекулам при термической активации, недостаточно для преодоления энергетического барьера. Иными словами, при таком механизме энергия активации даже при очень высоких температурах настолько велика, что реакции не должны протекать с заметной скоростью. Тем не менее, химические реакции и в природе, и в промышленных и лабораторных установках идут и часто идут очень быстро. Следовательно, одной теории активных столкновений недостаточно для объяснения причин протекания и механизмов реакций.
В 1930-х г.г. Э.Вигнером, М.Поляни, Г.Эйрингом и М.Эвансом была создана теория, позволяющая объяснить протекание реакций при малых тепловых скоростях молекул. Она носит название теории переходного состояния (или теории абсолютных скоростей реакций). Основные положения этой теории:
1) Взаимодействие молекул не сразу приводит к образованию молекул продуктов. Вначале образуется т. н. “переходное состояние” или активированный комплекс.
2) Активированный комплекс представляет собой неустойчивое образование, в которое входят все атомы столкнувшихся и вступивших во взаимодействие молекул. Время жизни активированного комплекса очень мало; оно измеряется малыми (миллионными, десятимиллионными и т. д.) долями секунды. Расстояния между атомами в активированном комплексе несколько больше, чем в обычных молекулах, поэтому для его образования требуется дополнительная энергия.
3) Энергия активации в связи с этим рассматривается как энергия, необходимая для образования активированного комплекса.
|
|
|
4) Через какое-то время после возникновения активированный комплекс распадается с образованием молекул продуктов; при этом выделяется энергия.
5) Выделяющаяся при распаде активированного комплекса энергия может полностью или частично затрачиваться на активацию других молекул исходных веществ.
Наглядное представление о протекании реакции во времени в соответствии с теорией переходного состояния может дать энергетический профиль реакции, например, экзотермической(рис. 12.6).
По оси ординат откладывается энергия системы Е, а ось абсцисс - это так называемая координата реакции. Среднему запасу энергии теплового движения молекул исходных веществ соответствует уровень Е исх, энергии, запасаемой в активированном комплексе - уровень Е АК. Тогда разность Е АК - Е исх равна величине энергетического барьера, который должны преодолеть молекулы для того, чтобы вступить во взаимодействие энергия активации. Наглядное представление о нём даёт кривая, соединяющая уровни Е исх и Е АК. Высота энергетического барьера зависит от природы реагирующих веществ, энергии, необходимой для образования активированного комплекса (энергии активации), а также от средней энергии теплового движения молекул Е исх.
Рис. 12.6. Энергетический профиль экзотермической реакции |
При повышении температуры уровень Е исх поднимается, величина энергетического барьера становится меньше и во взаимодействие может вступить большее число молекул. Это и служит причиной ускорения реакции с повышением температуры. При понижении температуры, наоборот, уровень Е исх опускается и величина энергетического барьера возрастает, что приводит к уменьшению скорости реакции.
При распаде активированного комплекса с образованием молекул продуктов выделяется энергия, которой соответствует разность Е АК - Е прод, где Е прод - средний запас энергии молекул продуктов. Часть этой выделяющейся энергии, равная разности Е АК - Е исх, пойдёт на активацию новых молекул исходных веществ, а избыток Е исх - Е прод выделится в окружающую среду в виде экзотермического теплового эффекта реакции DНr.
|
|
|
Для эндотермических реакцийэнергетический профиль выглядит несколько иначе (рис. 12.7). Видно, что в этом случае энергетический уровень Е исх ниже, чем уровень Е прод. В результате этого энергии Е АК - Е прод, выделяющейся при распаде активированного комплекса, недостаточно для того,
Рис. 12.7. Энергетический профиль эндотермической реакции |
чтобы вызвать активацию новых молекул реагирующих веществ. Поэтому для продолжения реакции необходим подвод энергии извне, в виде эндотермического теплового эффекта.
Существование активированного комплекса подтверждается экспериментальными данными. Так, например, для одной из несложных модельных реакций взаимодействия атома водорода с молекулой водорода
Н2 + Н ® Н + Н2,
значение энергии активации близко к 36,8 кДж/моль. Если бы реакция шла через стадию полной диссоциации молекул Н2, а не через стадию образования активированного комплекса Н2·Н, то потребовалась бы энергия активации 435,1 кДж/моль.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 8392; Нарушение авторских прав?; Мы поможем в написании вашей работы!