
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диссоциация карбоновых кислот
|
|
|
|
Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты, из-за стабилизации карбоксилат – аниона, вызванной делокализацией p-электронов. Другими словами, карбоксилат-ион стабилизирован вследствие резонанса:

Степень делокализации изменяется в ряду RCОО- >> RCOОH >> RОH, RO-

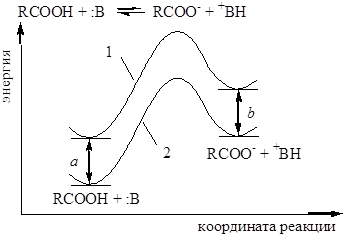
Энергия а - стабилизация, вызванная делокализацией в RCOOH; b - стабилизация, обусловленная делокализацией в RCOО-; 1 - гипотетическая кривая, делокализация отсутствует; 2 - истинная кривая, имеется делокализация.
Кислотность выражают количественно через константу диссоциации Ка или через рКа. Константы диссоциации большинства карбоновых кислот составляют около 10-5 (например, для уксусной кислоты 1,8∙10-5), что свидетельствует о довольно высокой концентрации неионизированной формы кислоты. Поэтому большая часть карбоновых кислот относится к слабым кислотам. Кислотность больше для тех кислот, в молекуле которых имеется заместитель, стабилизирующий карбоксилат-анион. Электроноакцепторные заместители в молекуле карбоновой кислоты, оттягивающие электроны от карбоксильной группы, стабилизируют карбоксилат-ион и увеличивают способность его образования, т.е. увеличивают силу кислоты. Электронодонорные заместители оказывают противоположное действие.

Влияние заместителей на кислотность показано в таблице 21.1.
Таблица 21.1
Влияние заместителей на кислотность
| Кислота | рКа |
| СН3СООН | 4.8 |
| СН3СН2СООН | 4.8 |
| ClСН2СООН | 2.9 |
| Cl2СНСООН | 1.3 |
| Сl3CСООН | 0.7 |
| FСН2СООН | 2.6 |
| F3CСООН | 0.2 |
2.Образование солей. Органические кислоты образуют соли с металлами, их оксидами, карбонатами, гидрокарбонатами и щелочами, например:
СН3СООН + NaOH ® СН3СОО-Na+ + H2O
3.Образование галогенангидридов. Под действием галогенидов фосфора (PCl5, PCl3, PBr3) карбоновые кислоты образуют галогенангидриды (гидроксил замещается на галоген):
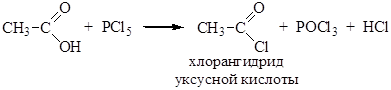
Хлорангидриды могут также быть получены действием на карбоновые кислоты тионилхлорида:

4. Реакция с аммиаком. При комнатной температуре карбоновые кислоты образуют с аммиаком аммонийные соли, которые при нагревании превращаются в амиды карбоновых кислот:

|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 3066; Нарушение авторских прав?; Мы поможем в написании вашей работы!