
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Первое начало термодинамики. Адиабатный процесс
|
|
|
|
Уравнение Менделеева–Клайперона описывает зависимость функций состояния идеального газа, но не дает ответа о причине совершения газом работы. Из закона сохранения энергии можно заключить, что теплота, подводимая к газу, идет на совершение работы и на изменение его внутренней энергией. Под внутренней энергией идеального газа понимают кинетическую энергию движения молекул.
Первое начало термодинамики записывается следующим образом:
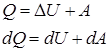 , ,
| (62) |
где Q – количество теплоты; U – внутренняя энергия; A – работа, совершаемая газом.
Следует отметить, что при изотермическом процессе внутренняя энергия остается постоянной и приращение ее равно нулю, при изохорном процессе все тепло идет во внутреннюю энергию, и только при изобарном процессе тепло идет и на изменение внутренней энергии и в работу, поэтому изобарный процесс из всех изопроцессов наиболее теплосодержательный.
Для изопроцессов первое начал термодинамики в дифференциальном виде запишется:
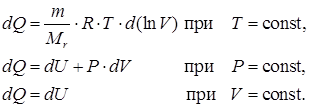
| (63) |
Как известно, теплоемкостью тела называется величина, равная количеству теплоты, необходимого на нагревания единицы содержания тела на единицу температуры. Исходя из определения теплоемкости можно вводить три величины теплоемкости: удельная (на единицу массы), объемная (на единицу объема тела) и молярную (на количество вещества в молях):
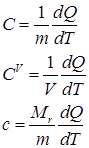 . .
| (64) |
Объемная теплоемкость применяется в теплотехнике, где используются постоянные объемы теплоносителей (ядерные реакторы и т.д.). В термодинамике газов используется молярная теплоемкость.
Как видно из (63) и (64) при изохорном процессе:
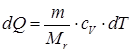 , ,
| (65) |
где cV – теплоемкость при постоянным объеме.
Если подставить в первое начало термодинамики уравнение состояния в полных дифференциалах:
 , ,
| (67) |
с наложением условия изобарности:
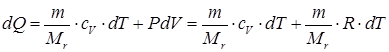 . .
|
и вычислить молярную теплоемкость при постоянном давлении по определению, получим закон Майера:
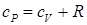 . .
| (68) |
Для теоретического вычисления теплоемкости рассмотрим все варианты движения одной молекулы, которые называют степенями свободы молекулы. Во-первых, любая молекула может двигаться поступательно, летая по всем трем координатным направлениям. Во-вторых, для молекулы многоатомного газа разрешено вращательное движение, и в-последних, для молекул, с слабыми химическими связями возможны колебательные движения атомов.
Каждый из вариантов движения равновероятно осуществим с точки зрения затрат энергии. Поэтому внутренняя энергия одной молекулы, после подстановки в закон Больцмана:
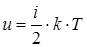 . .
| (69) |
где 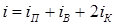 – число степеней свободы, равное сумме поступательных (iП), вращательных (iВ) и удвоенных колебательных (iК) степеней свободы. После умножения на постоянную Авогадро и подстановкой в определение молярной теплоемкости при изохорном процессе:
– число степеней свободы, равное сумме поступательных (iП), вращательных (iВ) и удвоенных колебательных (iК) степеней свободы. После умножения на постоянную Авогадро и подстановкой в определение молярной теплоемкости при изохорном процессе:
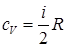 . .
| (70) |
Молекула одноатомного идеального газа может иметь только три поступательных степени свободы (i =3). Вращательных степеней свободы молекула одноатомного газа в рамках теории теплоемкости иметь не может, поскольку молекулы считаем материальными точками, а точка вращаться не может. Молекула двухатомного идеального газа может быть описана тремя моделями: модель жесткой гантели, модель пружинно-поршневой гантели и модель из двух атомах на пружинке. В модели жесткой гантели атомы расположены на жестком абсолютно несжимаемом стержне. Такая молекула имеет, кроме трех поступательных, ее две вращательных степени свободы (i =5). В модели пружинно-поршневой гантели атомы расположены на упругом стержне и могут совершать колебания в одном направлении (i =7). В модели двух атомов на пружинке молекула имеет по три поступательных и вращательных степеней свободы и одну колебательную (i =8). Поэтому от выбора вида модели будет зависеть конкретный расчет теплоемкости.
Ранее рассмотренные изопроцессы дают в правой части уравнения первого начала термодинамики постоянные или равные нулю значения внутренней энергии или работы газа. Остался один процесс, совершаемый над идеальным газом, при котором к газу подводится постоянное количество теплоты или не подводится вообще. В первом случае (Q =const) процесс называют политропным, во втором (Q =0) – адиабатным. Остановимся на адиабатном процессе подробно.
При адиабатном процессе, газ совершает работу за счет изменения внутренней энергии:
 , ,
| (71) |
где T 1 и T 2 – температуры начала и конца процесса.
Адиабатный процесс на практике не осуществим, но многие быстрые процессы можно считать близкими к адиабатному. Например, быстрое выпускание газа из баллона, взрыв бомбы, распространение звука в газе, конец такта сжатия поршневого насоса при накачке шин и т.д.
Для вывода уравнения адиабаты в первое начало термодинамики в дифференциальном виде (62) подставим уравнение Менделеева–Клайперона в полных дифференциалах (67) и работу газа (54):
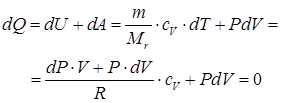 . .
|
Далее, после приведения к объему знаменателю и приведению подобных слагаемых:
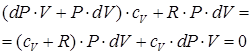 . .
| (72) |
Подстановкой в (72) закона Майера и делением обеих частей уравнения на произведение давления на объем, всегда при положительной температуре отличного от нуля, получаем уравнение адиабаты в дифференциальном виде:
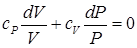 . .
| (73) |
Интегрируя дифференциальное уравнение (73) получаем уравнение адиабаты:
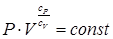 . .
| (74) |
Отношение теплоемкости при изобарном процессе к теплоемкости при изохорном процессе называют показателем адиабаты: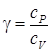 . Подстановка уравнения Менделеева–Клайперона в уравнение (74) дает уравнение адиабаты в зависимости от других функций состояния идеального газа:
. Подстановка уравнения Менделеева–Клайперона в уравнение (74) дает уравнение адиабаты в зависимости от других функций состояния идеального газа:
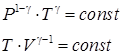 . .
| (75) |
Константы в уравнениях (74) и (75) разные, соотношения между ними можно получить проведя указанную подстановку уравнения состояния в уравнение (74).
Произведя деление уравнений (74) на (75) в произвольной последовательности можно получить уравнение адиабаты по двум точкам параметров состояния идеального газа:
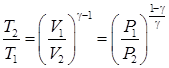 . .
| (76) |
Аналогично получается работа, совершаемая газом, при адиабатном процессе:
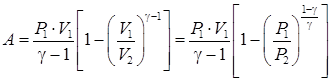 . .
| (77) |
Обобщением рассмотренного выше адиабатного процесса, являетсся политропный процесс, описываемый аналогично адиабатному, уравнением адиабаты с точностью до решения уравнения (72) и первого начала термодинамики до константы:
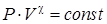 , ,
| (78) |
где χ – безразмерная величина, показатель политропы. Всем ранее изученным процессам, соответствуют разные показатели политропы: при χ=0 имеем изобарный процесс; при χ=1 – изотермический процесс; при χ=γ – адиабатический процесс и при 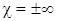 – изохорный процесс.
– изохорный процесс.
Вычислим молярную теплоемкость c при политропным процессом. Перепишем первое начало термодинамики из определения молярной теплоемкости и работы, совершаемой газом:
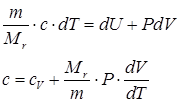 . .
| (79) |
Соотношение между температурой газа и его объемом приполитропном процессе найдем из уравнения (78) и уравнения Менделеева–Клайперона:
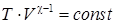 , ,
|
дифференцирую его, получаем:
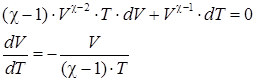 . .
|
Подстановка последнего выражения в (79) и уравнения состояния имеем:
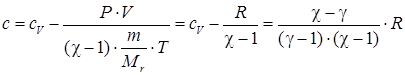 . .
| (80) |
Для изопроцессов из формулы (80) следует:
1) для изотермического процесса (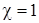 ) –
) – 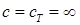 ;
;
2) для изобарного процесса ( ) –
) – 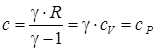 ;
;
3) для изохорного процесса (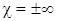 ) –
) – 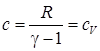 ;
;
4) для адиабатного процесса (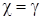 ) –
) – 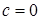 .
.
Работа, совершаемая идеальным газом, при политропном процессе:
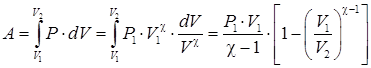 . .
| (81) |
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1967; Нарушение авторских прав?; Мы поможем в написании вашей работы!