
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диссоциация комплексных соединений. Константа образования и нестойкости комплексов
|
|
|
|
Как уже сказано выше, химические связи комплексообразователя с лигандами и ионами внешней сферы различны. В первом случае химическая связь имеет преимущественно ковалентный, а во втором – ионный характер. Вследствие этого в водных растворах комплексные соединения легко диссоциируют с отщеплением внешней сферы.
1) [Ag(NH3)2]Cl → [Ag(NH3)2]+ + Cl- - первичная диссоциация комплексного соединения (как сильного электролита).
В то же время диссоциация комплексного иона идет в сравнении с первичной диссоциацией в незначительной степени, т.е. комплексный ион диссоциирует обратимо как слабый электролит:
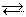 [Ag(NH3)2]+ Ag+ + 2NH3 – вторичная диссоциация комплекса. Вторичная диссоциация комплекса может быть охарактеризована константой равновесия, называемой константой нестойкости (КН):
[Ag(NH3)2]+ Ag+ + 2NH3 – вторичная диссоциация комплекса. Вторичная диссоциация комплекса может быть охарактеризована константой равновесия, называемой константой нестойкости (КН):
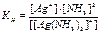 .
.
Константа нестойкости характеризует устойчивость комплекса: чем больше значение КН, т.е. чем больше концентрация в растворе ионов, на которые диссоциирует комплекс, тем слабее, более неустойчив комплекс, и наоборот.
Например, сравним КН следующих комплексов:
| Комплекс | КН |
| [Ag(NO3)2]- | 1,3 ∙ 10-2 |
| [Ag(NH3)2]+ | 6,8 ∙ 10-8 |
| [Ag(CN)2]- | 1 ∙ 10-21 |
Самый прочный комплекс – последний – [Ag(CN)2]-, поскольку его константа нестойкости самая маленькая.
При изучении комплексных соединений используют также величину, обратную константе нестойкости. Эта величина называется константой устойчивости (Ку) или константой образования (Кобр) комплекса:
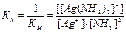 .
.
Чем больше значение Ку, тем более устойчив данный комплекс. Значения КН и Ку комплексов приводятся в справочниках при 25оС.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 873; Нарушение авторских прав?; Мы поможем в написании вашей работы!