
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фотометрические методы анализа
|
|
|
|
Лекция
Фотометрические методы анализа относятся к оптическим методам анализа, т. е. методам, основанным на взаимодействии вещества с электромагнитным излучением (метод абсорбционной спектроскопии).
Как известно, взаимодействие сопровождается поглощением энергии, в результате чего в зависимости от энергии излучения могут происходить изменения в ядрах, электронах, атомах и молекулах. А соответственно изменяются какие-либо параметры взаимодействующей системы. Именно на этом основаны физико-химические или физические методы исследования вещества. Нас интересует взаимодействие анализируемого объекта с излучением в бл.УФ, видимой, бл.ИК областях спектра.
При этом выделяют следующие группы методов:
1. Атомно-адсорбционный анализ – основанный на поглощении световой энергии атомами анализируемых веществ.
2. Молекулярно-адсорбционный анализ – анализ по поглощению света молекулами анализируемого вещества и сложными ионами (в бл.УФ, видимой, бл.ИК). К нему относим фотоэлектроколориметрию, спектрофотометрию, ИК-спектроскопию.
3. Анализ по поглощению и рассеиванию световой энергии взвешанными частицами анализируемого вещества, т.е. дисперсными системами (турбидиметрия, нефелометрия).
4. Люминесцентный анализ – основанный на измерении излучения, выделенного возбужденными частицами исследуемого объекта.
Таблица 1
Электронный спектр излучения (поглощения)
| Спектральная область | Длина волны, λ, нм | Энергия Е, эВ | Процессы, протекающие в результате поглощения (или излучения) |
| Ультрофиолетовая: Вакуумная Близкая | <200 200-400 | 102 - 10 | Электронные переходы |
| Видимая | 400-700 | 10 - 1 | |
| Инфракрасная: Близкая Фундаментальная Далекая | 700-1500 1500-75000 7,5·104 – 106 | 1 – 10-2 | Колебание молекул Вращение молекул |
В молекулярно-адсорбционном анализе используют только такие участки спектра, в которых процесс поглощения не сопровождается нарушением целостности молекул (бл.УФ, видимая, бл.ИК области спектра). Фотометрический анализ позволяет решать не только чисто аналитические задачи, т.е. определить концентрацию вещества в растворе, но и изучать равновесия в растворах комплексных соединений, если хотя бы один из продуктов реакции обладает светопоглощением.
–Методы, основанные на измерении избирательного поглощения светового излучения в видимой, бл.УФ, бл.ИК областях спектра истинными рас творами исследуемого вещества (т.е. однородными нерассеивающими системами). Для этого определяемый компонент переводят в поглощающее свет соединение, количество продукта реакции (или результат реакции) фиксируют путем измерения его светопоглощения с помощью физических приборов. Чаще всего работают в видимой области спектра, переводя определяемый компонент (R: определяемый ион металла) при помощи соответствующего реагента в окрашенное соединение (к.с.), избирательно поглощающее электромагнитное излучение.
При пропускании света через раствор такого соединения происходит поглощение отдельных квантов света, т.е. интенсивность светового потока уменьшается. 
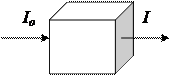 Изменяется внутренняя энергия молекул, происходит возбуждение внешних валентных электронов, т.е. их переход на высший энергетический уровень.
Изменяется внутренняя энергия молекул, происходит возбуждение внешних валентных электронов, т.е. их переход на высший энергетический уровень.
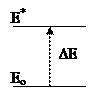 ∆Е=Е* – Ео=hγ=h
∆Е=Е* – Ео=hγ=h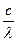 – (1), cоотношение, выведенное Эйнштейном. h – постоянная Планка; h=6,62·10-27 эрг-сек или h=6,625·10-34 Дж·с.
– (1), cоотношение, выведенное Эйнштейном. h – постоянная Планка; h=6,62·10-27 эрг-сек или h=6,625·10-34 Дж·с.
Т.е. для возбуждения электрона нужна определенная энергия – ∆Е. Энергия поглощаемого фотона (кванта) определяется тем же самым уравнением (1). Таким образом, энергия фотона определяет его длину волны (λ, нм). Поглощаются не все фотоны, а лишь те, энергия которых близка к ∆Е, т.е.
Екванта=Евозб. электрона=∆Е (2)
|
|
|
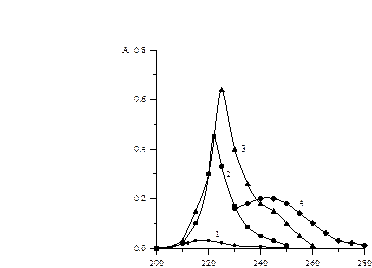
Выгодно использовать свет с определенной длиной волны (λ) – монохроматичный. Устройство, позволяющее получить монохроматичное излучение, называют монохроматором. В качестве монохроматора используют:
1. светофильтр;
2. призма;
3. дифракционная решетка.
Избирательное поглощение органических соединений в определенной области спектра связано с наличием в молекуле определенных групп атомов. Они содержат одну или несколько кратных связей или неподеленные пары электронов (НЭП). Такие группы атомов, определяющие окраску веществ, если поглощение происходит в видимой области спектра, называют хромофорами.
Примеры хромофорных групп:
1. Карбонильная,
2. карбоксильная,
3. этиленовая,
4. азометиновая 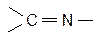 ,
,
5. нитрозо-группа  ,
,
6. нитритная группа 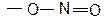 ,
,
7. бензол 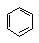 ,
,
8. нитратная 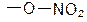 .
.
Присутствие одной и той же группы атомов в молекулах, иногда принадлежащих к разным классам соединений, сопровождается проявлением одного и того же, характерного для нее поглощения, лишь в некоторой мере искаженного иным окружением этой группы.
| Хромофорная группа | Соединение | λмакс., нм |
| Карбонильная | Ацетон (спирт) Ацетальдегид (спирт) | 270,0 293,4 |
| Карбоксильная | Уксусная кислота (H2O) |
Иногда в молекуле рядом с хромофором находится активная группа атомов, которая сама по себе не определяет поглощение, но может усиливать интенсивность поглощения, смещать максимум поглощения в длинноволновую область спектра. Такие группы (-NH2, -N(CH3)2, -OH, -OCH3) называются ауксохромами.
Растворы солей неорганических соединений элементов первых периодов системы в большинстве своем не обладают характерным поглощением в УФ-й, видимой и ИК-областях спектра. Точнее, наблюдается в этих областях только поглощение некоторых анионов, но катионы (вернее их акво-комплексы) обычно "бесцветны". Это зависит от того, что данные катионы имеют, как правило, устойчивую замкнутую оболочку, образовавшуюся после того, как атом, переходя в катион, потерял все наименее прочно связанные электроны, и для возбуждения оставшихся электронов недостаточно даже энергии УФ излучения. Электронная система анионов менее стабильна (их полосы поглощения попадают в УФ область). Окраска акво-комплексов катионов, имеющих незаполненные d- орбитали, обусловлена возможностью легких переходов между энергетически близкими d- орбиталями. Поэтому, растворы солей, например, меди, никеля, кобальта, железа и т.д. окрашены, а цинка и кадмия бесцветны, поскольку их ионы имеют заполненный d- подуровень.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 783; Нарушение авторских прав?; Мы поможем в написании вашей работы!