
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Получение изопрена из 2-метилпропена и формальдегида
|
|
|
|
Процесс получения изопрена этим методом двух стадиный. Первая стадия – конденсация 2-метилпропена с формальдегидом:
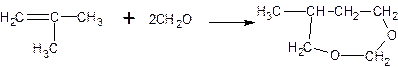
С образованием 4,4-диметил-1,3-диоксана, это реакция Принса ее проводят при температуре 70-90 °С, давлении 1-1,6МПа, катализатор кислый (H2SO4) в количестве от 1-1,5% от массы 2-метилпропена. Мольное соотношение углеводород:альдегид=0,73:1. Конверсия 2-метилпропена равна 88-92%, формальдегида 92-96%. Среди побочных продуктов в наибольших количествах образуется триметилкарбинол.
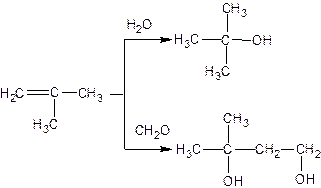
От 5-7,5 % триметилбутадиол-1,3, кроме того образуется большое количество различных примесей (диокалов, спирты, диолы, эфиры и т.д.). см. альбом стр 37-39.
Примнение серной кислоты в качестве катализатора вызывает коррозию аппаратуры и приводит к образованию кислых сточных вод. В качестве сырья используют бутан-изобутиленная фракция, содержащая не мене 40% 2-метилпропена, содержание в этой фракции циклопентадиена не должно превышать 0,0005%, и ацетиленовых менее 0,0001%
Применяемый формальдегид содержит 37% формальдегида и не более 1% метанола.
Схема в альбоме стр 42.
Вторая стадия процесса представляет собой газофазное каталитическое расщепление 4,4 – диметил-1,3-диоксана.
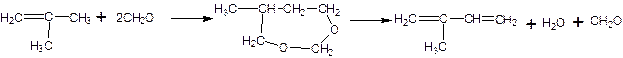
Катализатором этой стадии могут служить фосрорная кислота на алюмосиликте, оксид алюминия, с 25% оксидом кремния; смесь фосфатов и др. вещества кислотного характера.
Наилучшие результаты получены на Ca-P-kat, КБФ-36 при температуре 375-400 °С и разбавленный водяным паром 1:2. Выход изопрена составляет от 70-75% от пропущенного диоксана. Побочные реакции 2 стадии:
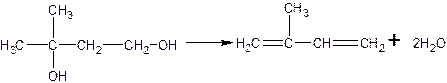
Но в тоже время образующаяся молекула может встретиться с молекулой формальдегида с образованием метилдегидропирана:
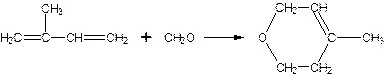
Может произойти разложение формальдегида:
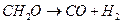
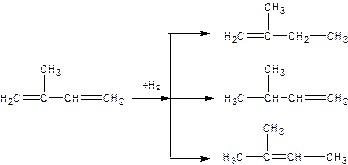
Вторая стадия протекает с поглощением тепла, подвод тепла может быть осуществлен разными способами. В процессе разработки во Франции институтом нефти использовался реактор с движущимся слоем катализатора. У нас успешно используются реакторы полочного типа со стационарным слоем катализатора. В качестве теплоносителя применяется перегретый водяной пар, который подается в реактор ступенчато, благодаря этому температурный режим реактора приближается к изотермическому. Регенерация катализатора – выжигание кокса осуществляется каждые 5-6 часов в начале катализатора и через 3 часа в конце его работы, так как по мере падения активности катализатора количество отлагающегося кокса возрастает. Продолжительность циклов реакции и регенерации одинаково. Тех. схема в альбоме стр. 47 рис. 15 и в методичке стр. 52
Одностадийный синтез изопрена
Его проводят в жидкой фазе при Т=150-160 0С, р=3 МПа в присутствии водорастворимых кислот Льюиса.
Достоинства:
1. Снижается число аппаратов
2. Снижаются капитальные затраты
3. Легче утилизировать побочные продукты
Например, третбутанол, который возвращают на реакцию, где он находится в равновесии с изобутеном:
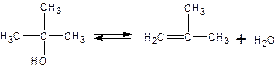
Второй вариант. Синтез изопрена осуществляют в газовой фазе при Т=200-350 0С. Процесс гетерогенно-каталитический, селективность 80 % по формальдегиду и 90 % по изобутену. Достоинства:
1. Снижение коррозии аппаратуры
2. Высокое качество получаемого изопрена.
Третий вариант. Получение изопрена из ацетилена и ацетона
В Италии разработан процесс получения изопрена из ацетона и ацетилена по реакции открытой Фаворским и усовершенствованной Назаровым. Различают следующие стадии:
1. Этинилирование ацетона
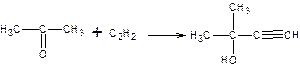
В результате получают 2-метилбутин-3-ол-2. Реакцию ведут при Т=10-40 0С р=2 МПа. В качестве катализатора используется водный раствор КОН. Реакцию проводят в среде жидкого аммиака. Протекает почти количественно и практически необратимо. Конверсия составляет 95%. Полученный 2-метилбутин-3-ол-2 отгоняется виде азеотропной смеси с водой содержащей 74 % 2-метилбутин-3-ола-2.
2. Селективное гидрирование:
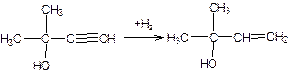
Вторую стадию ведут при Т=30-80 0С и давлении водорода от 0,5 до 1 МПа в присутствии ингибитора. Катализатор – коллоидный палладий на носителе. Ингибитор используется для предотвращения получения насыщенного спирта. Конверсия 2-метилбутин-3-ол-2 – полная, выход 2-метилбутен-3-ола-2 более 90 %. Насыщенных продуктов менее 1 %. 2-метилбутен-3-ол-2 получают виде азеотропа с водой.
3. Дегидротация 2-метилбутен-3-ол-2 в изопрен:
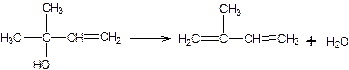
На оксиде алюминия Т=260-300 0С. Катализатор регенерируют через 100 часов работы путем выжигания углистых отложений. Селективность процесса более 99%.
Получение изопрена из пропилена
Исследования показали, что для получения изопрена с высоким выходом, пиролизу надо подвергать только определенные изомеры демиризованного пропилена – это 2 –метилпентен-2, 3-метилпентен-2 или 2-этилпентен-1. Это объясняется тем, что расщепление димера происходит селективно преимущественно по связи С-С находящейся в 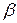 -положении по отношению к двойной связи, так как эта связь обладает наименьшей электронной плотностью. Был разработан трехстадийный процесс:
-положении по отношению к двойной связи, так как эта связь обладает наименьшей электронной плотностью. Был разработан трехстадийный процесс:
1. Димеризация пропилена:
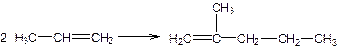
Этот процесс осуществляется при Т=150-250 0С и р=20-30 МПа. В присутствии катализатора 3-изобутилалюминия или 3-изопропилалюминия. Конверсия пропилена – 70-85 %. Процесс экзотермичен, поэтому необходим отвод теплоты. Используют трубчатые реактора и отвод тепла осуществляется подачей в межтрубное пространство хладагента.
2. Изомеризация:
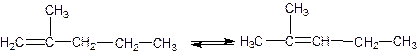
Различают два варианта этой стадии:
1. Жидкофазный процесс, Т=80 0С, катализатор – серная кислота или катионит КУ-1 или алюмосиликаты. Выход 75-84,2 %, селективность 94-98 %.
2. Парофазный процесс на твердых катализаторах. В качестве катализатора используется фосфорная кислота на носителе, алюмосиликаты, катиониты, оксид алюминия при Т=200-250 0С. Конверсия от 46 до 60 % на алюмосиликате, до 70 % на оксиде алюминия при селективности 95-97 % соответственно. Срок работы катализатора 100 часов и 200 часов соответственно. Регенерация – выжигание кокса.
3. Пиролиз 2-метилпентена-2 (диметилирование)
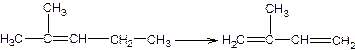
Эта стадия наиболее трудна, так как на ряду с деметилированием протекают реакции расщипления и образуется большое количеств побочных продуктов. Селективность низкая. В чисто термических условиях процесс ведут при Т=700-900 0С и р=0,01 МПа. В качестве разбавителя используют азот и водяной пар, конверсия 35 % при селективности 40-46 %. При использовании водяного пара селективность выше. При использовании в качестве катализатора НВr Т снижается – 650-700 0С. Селективность 66 %, хороший эффект дает соотношение промотора и НВr. В качестве промотера используют труднокорректируемое вещество 2,3-диметилбутен-2. Этот метод считается перспективным.
Недостатки:
1. Низкая селективность третей стадии
2. Применение весьма агрессивного и дорогого катализатора НВr на третей стадии.
Поэтому сравнение процессов производства изопрена показала, что наиболее экономным является способ производства изопрена из 2 –метилпропена и формальдегида
Хлоропрен
Среди хлорсодержащих мономеров получивших широкое применение в производстве синтетических каучуков и пластмасс наиболее важным является хлоропрен:
Хлоропрен – жидкость с температурой кипения 59,4 0С с характерным запахом, в воде растворяется плохо, но смешивается со многими органическими растворителями. Хлоропрен горюч и токсичен. При малых концентрациях вызывает раздражение слизистых оболочек. В промышленности его получают двумя способами:
1. Из углеводородов С4 нормального строения, а именно бутадиен-1,3 или бутан-бутеновой фракции
2. Из ацетилена через промежуточное образование винилацетилена.
Первый способ. Проводят газофазное хлорирование углеводородов С4 при Т=400 0С. При хлорировании дивинила Т=270-320 0С. Берут избыток углеводорода:
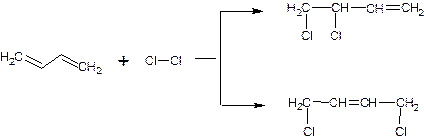
Реакционные газы на выходе из хлоратора быстро охлаждают и направляют в отпарную колону, где происходит отделение хлорорганических продуктов от непрореагирующего углеводорода и хлороводорода возвращают в процесс. Образующиеся хлорорганические продукты – смесь моно- и дихлорбутенов подвергают ректификации с целью разделения моно- от дихлорпроизводных. Монохлорпроизводные затем подвергаются пиролизу при Т=600 0С. При этом образуются дивинил и бутены в смеси с НCl. Всю эту смесь возвращают в процесс на хлорирование. Смесь дихлорпроизводных подвергают изомеризации в присутствии солей меди – чаще всего нафтенат меди в жидкой фазе:
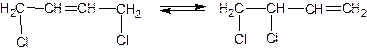
1,4 дихлоризобутен-2 изомеризуется в 3,4- дихлорбутен-1,который направляется в секционированный реактор,в котором проводят дегидрохлорирование при нагревании в присутствии 20% р-ра NaOH или КОН в хлорпрен:
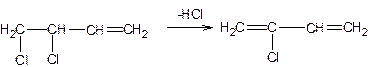
Хлорпрен отделяют от непрореагировавших продуктов и подвергают ректификации.
Второй способ. Хлорпрен получается жидкофазным гидрохлорированием винилацетилена, предварительно полученного димеризацией ацетилена
Первая стадния
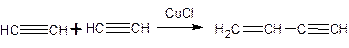
Катализатор 35-50% раствор хлоридов меди(I) или хлорида аммония в соляной кислоте.
Побочная реакция:
1) Образование высших полимеров ацетилена
2) Образование продуктов гидратации
3) Образование продуктов гидрохлорирования ацетилена и винилацетилена
Вторая стадия гидрохлорирование винилацетилена с образованием хлоропрена:
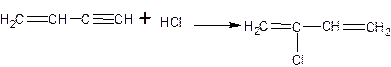
Температура процесса 60-80 ºC, время процесса 15сек. Катализатор используют тотже что и на первой стадии.
Далее происходит гидратация винилацетилена с образованием метилвинилкетона
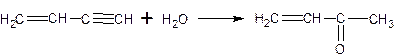
Побочный процесс: димеризация хлорпрена с образованием циклических соединений
Механизм реакции предложен Карозерсом, катализатор- CuCl
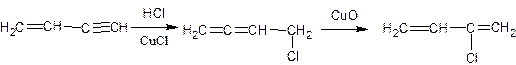
образуется 4 хлорбутадиен-1,2, который изомеризуется в хлорпрен
Долгопольский и сотрудники полагают что гидрохлорирование винилацетилена происходит через образование промежуточного комплекса соединения винилацетилена с компонентами катализатора,в процессе комплексообразования важную роль играет хлорид меди (I), поэтому его концентрация определяет производительность катализатора, повысить которую можно за счет повышения в нем содержания хлорида меди и соляной кислоты. Однако с увеличением кислотности катализатора усиливается образование побочных продуктов. Во избежание побочного образования 1,3 дихлорбутена-2 хлорпрен непрерывно выводят из зоны реакции. Сырой продукт стабилизируют пирокатехином 0,5-1% и подвергают ректификации. Выход хлоропрена достигает 80%, образуется 1,4дихлорбутен-2,дегидрохлорированием его превращают в хлорпрен. Т=250-270о С
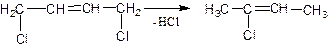
Реакцию проводят в газовой фазе на селикагеле или каолине с выходом хлорпрена 67-75%.
Технологическая схема в мет. стр 59. кирпичников стр 86
Изобутилен(2 метилпропен) – при нормальных условиях бесцветный газ с неприятным запахом, нерастворяется в воде, растворяется в этиловом спирте и диэтиловом эфире. Изобутилен применяют для получения полиизобутилена и бутилкаучука,а также для производства изопрена методом конденсации изобутилена с формальдегидом,кроме того изобутилен используют в качестве добавки к смазочным маслам,для пропитки в качестве электроизоляционных материалов.
Методы получения:
1) Дегидротацией изобутанола при Т= 380о С
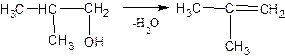
2) Выделение изобутилена из бутанбутеновой фракции газов крекинга. Этот способ экономически выгоден.
3) Дегидрирование изобутана. Дегидрирование проводят в присутствии алюмо хромового катализатора при Т=500-550оС
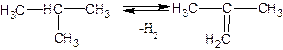
Смесь бутенов не может быть разделена простой ректификацией из-за близости температур кипения, поэтому используют химические методы разделения:
- Выделение изобутелена из фракции С4 с помощью серной кислоты.
- Выделение изобутелена из фракции С4 на ионообменных смолах.
- Выделение изобутелена из фракции С4 при помощи низших спиртов.
Первый метод разделения. При обработки смеси бутенов серной кислотой при Т=35-40 ºС нормальные бутены не вступают в реакцию, реагирует только изобутилен с образованием третбутилсерной кислоты:
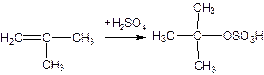
Побочно образуется небольшое количество полимеров:
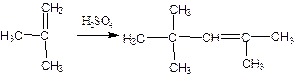
Гидролиз третбутил серной кислоты приводит к образованию третбутанола:
который тут же дегитратируется в изобутилен:
Схема выделения изобутилена:
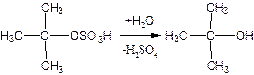
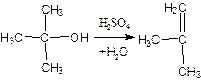
Гидролиз и дегидротация осуществляется в колонне регенераторе, в котором пропускают водяной пар из верхней части колонны отбирают изобутилен, содержащий примеси третбутанола, полимера и др побочных веществ. Изобутилен отделяют от примесей и конденсируют. Из нижней части колонны выходит 45% серная кислота, которую регенерируют упариванием до исходной 65% кислоты. Выход изобутилена 90-95% от поступившей на разделение.
2 метод разделения -более совершенный. Проводят прямую гидратацию на катионите КУ-2 в третбутанол, Т= 90-100оС,Р=1-1,5МПА
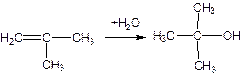
Достоинства:
1) Не используется кислота,т.е отсутствует коррозионно-активная среда.
2) Нет стадии регенерации кислоты
3) Возможно многократное использование КУ-2
4) Высокая частота получаемого изобутена
Затем третбутанол на том же катализаторе при Т=100-105оС и Р=0,34МПа дегидратируется в изобутилен
3 метод разделения. Метанол избирательно образует с изобутиленом метилтретбутиловый эфир.
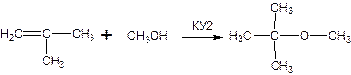
Процесс проводят в присутствии ионитных катализаторов, затем проводят разложение по обратимой реакции в присутствии катализаторов кислотного типа при Т=100-3000С, Р=1 МПа. Для подавления побочных реакции разложение ведут при разбавлении водяным паром. Перспективный способ.
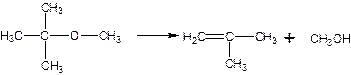
4 метод разделения. Дегидрирование изобутанола. У нас в стране изобутилен получают дегидрированием изобутанола, катализатор Al-Cr, Т=550-5800С
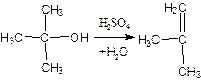
Обьемная скорость 120-150 час -1
Термодинамика дегидрирования изобутанола, аналогично дегидрирование н-бутана. Процесс дегидрирования изобутана идет пи более низкой температуре, что объясняется более низкой энергии связи С-Н у третичного атома углерода. Процесс проводят в псевдоожиженном слое катализатора, выход изобутилена на пропущенный изобутан достигает 38-42% при селективности 80%
Изобутан-изобутеленовая фракцию выделяют из контактного газа дегидрирования, аборбцией и ректификацией, разделение изобутан-изобутеленовой фракции осуществляется серной кислотой.
Изобутилен полученный этим методом в 5 раз дешевле, чем полученный дегидрированием изобутанола оксосинтезом.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1598; Нарушение авторских прав?; Мы поможем в написании вашей работы!