
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Етіологія
|
|
|
|
Цукровий діабет ІІ типу
В основі діабету ІІ типу лежить первинна резистентність до інсуліну, яка в більшості випадків має спадкову природу. Серед механізмів інсулінорезистентності головними є:
1. Рецепторні: недостатність інсулінових рецепторів або їх нечутливість до інсуліну.
2. Пострецепторні: порушення передачі сигналу від інсулінових рецепторів до внутрішньоклітинних ферментних систем.
3. Пререцепторні:
А). Панкреатичні:
· MODY пов'язан з аутосомно-домінантним успадкуванням дефекту глюкокінази у В-клітинах, яка зумовлює їх чутливість до глюкози.
· Зниження чутливості В-клітин до глюкози може бути пов'язано і з відсутністю чи дефектом GluТ-2.
· Відсутність D-клітин знімає гальмування з А- і В-клітин.
· Нечутливість А-клітин до гальмівних впливів інсуліну чи глюкози.
· Накопичення аміліну і гіаліну в острівцях знижує чутливість В-клітин до стимулюючих впливів глюкози.
В). Позапанкреатичні:
· Вироблення антитіл до інсуліну.
· Активація інсулінази.
Інсулінорезистентність в першу чергу зменшує вплив інсуліну на глікогенез і майже не впливає на стимуляцію інсуліном ліпогенезу. Тому виникає ожиріння, яке підсилює інсулінорезистентність, оскільки зменшується відстань між рецепторами до інсуліну на адипоцитах, що пригнічує їх чутливість до гормону. Можлива первинна нечутливість центру голоду до кахексину, що виробляється адипоцитами і за нормальних умов пригнічує відчуття голоду при накопиченні ліпідів у жирових клітинах.
Для інсулінонезалежного діабету характерним є розвиток гіперглікемічної (гіперосмолярної) коми, яка розвивається у людей похилого віку, що не мають необхідного лікування і догляду. Кома виникає на фоні значної гіперглікемії (55-200 мМ/л) і гіпернатріємії. Осмолярність позаклітинної рідини збільшується до 500 мосмоль/л, що є наслідком гіперглікемії, гіпернатріємії та згущення крові при неможливості адекватної компенсації втрат води при діабетичній поліурії. Гіперосмолярність позаклітинної рідини призводить до втрати води клітинами, що порушує їх діяльність і, в першу чергу, нормальне функціонування нейронів головного мозку.
Мітогенний вплив гіперінсулінемії на фібробласти, макрофаги та гладком'язові клітини стінки судин на фоні гіперхолестеринемії, гіперліпідемії, глікірування білків плазми, активації агрегації тромбоцитів призводить до прискореного розвитку атеросклерозу, що проявляється макроангіопатіями. Виникає ішемічна хвороба серця, порушення мозкового кровообігу та облітеруючий атеросклероз артерій нижніх кінцівок, який веде до їх ішемії та некрозу. Часто такі хворі вмирають від інфаркту міокарда або інсульту.
Лекція д.м.н., професора Кришталя М.В.: Порушення кислотно-основного стану
Нормальна концентрація іонів водню в позаклітинній рідині становить 40 некв/л, що відповідає рН – 7,4. Така концентрація Н+ в 100 тис. разів менша ніж концентрація К+ і в 1 млн. разів менша ніж концентрація Na+. Нормальні коливання рН від 7,35 до 7,45 відповідають змінам концентрації Н+ тільки в 10 некв/л, а зміни рН в межах від 7,0 до 7,8, які є сумісними з життям, відповідають змінам концентрації іонів водню тільки на 86 некв/л. Підтримка концентрації Н+ на такому низькому рівні і в таких вузьких межах коливань пов`язана з тим, що іони водню мають дуже високу біологічну активність. Порушення кислотно-основного стану (КОС), тобто зсув рН за межи норми, призводить до зміни активності ферментів, проникності мембран, чутливості рецепторів, активності БАР, секреції гормонів, стану колоїдів, нервово-м`язової збудливості, порушення синтезу АТФ тощо.
В той же час при метаболізмі жирів, білків та вуглеводів щодоби утворюється 15-20 тис. мілімолей (мМ) СО2. Частково розчиняючись у воді, СО2 утворює вугільну кислоту. Крім того в реакціях проміжного обміну за нормальних умов утворюється приблизно 50-100 мекв нелетких кислот, з яких 1/3 становить сірчана кислота, що утворюється при метаболізмі метіоніну та цистеїну; 1/3 – молочна, ацетооцтова та b-оксимасляна кислоти, що утворюються при неповному окисленні вуглеводів та жирів; ще 1/3 нелетких кислот утворюється при метаболізмі фосфоліпідів, фосфопротеїдів і солей з органічними катіонами, які метаболізуються.
Кількість кислот, що утворюються, залежить від вмісту білка в їжі та різко зменшується при молочно-рослинній дієті. Значне збільшення продукції органічних кислот відбувається при гіпоксії, голодуванні та цукровому діабеті.
Механізми підтримання сталості КОС. У нормі рН міжклітинної рідини та крові дорівнює 7,4, цитоплазми – 7,0-7,2, а активованих лізосом – 5,0-5,5. При цьому рН дистильованої води при температурі 37° С дорівнює 6,8. Таким чином, рН позаклітинної рідини має більш лужну реакцію ніж вода, яка є універсальним біологічним розчинником. Наявність градієнта концентрації іонів водню між різними компартментами організму та їх суворе підтримання в дуже вузьких межах, з одного боку, необхідне у зв`язку з тим, що фізіологічні реакції можуть відбуватися тільки при певних значеннях рН, а з іншого боку, забезпечується відповідними фізикохімічними (буфери та іонообмін) і фізіологічними (легені та нирки) механізмами.
Головним фізикохімічним механізмом підтримання сталості рН є буферні системи, які представляють собою суміш слабкої кислоти або слабкої основи з їх солями. При додаванні до буферного розчину сильної кислоти більшість іонів водню зв`язується із сполученою основою та утворює нейтральну сіль та слабку кислоту, яка не дисоціює. Це знижує кількість вільних іонів водню та запобігає зсуву рН, як, наприклад, у наступній реакції: HCl + NaHCO3 = H2CO3 + NaCl.
Якщо прийняти всю буферну ємність крові за 100%, то бікарбонатний буфер становить 53%, з яких бікарбонат плазми складає 35% і бікарбонат еритроцитів - 18%. 35% складає ємність гемоглобінового буфера, 7% - білкового буфера плазми, 3% - органічних фосфатів еритроцитів, 2% - неорганічних фосфатів плазми і еритроцитів.
Таким чином, найважливішим буфером крові є бікарбонатний буфер. У міжклітинній рідині, об`єм якої втричі перевищує об`єм крові, буферна ємність майже виключно визначається бікарбонатним буфером. Крім того, унікальною властивістю цього буфера є його відкритий характер. Це видно з рівняння Гендерсона-Хассельбалха:
[іонізована форма]
рН = рК +lg ------------------------------, яке для системи НСО3- - Н2СО3
[неіонізована форма]
[НСО3-] (метаболічний компонент; контролю-
ється нирками)
приймає вигляд: рН = 6,1 + lg ------------------------------------------------------------
[H2CO3] (респіраторний компонент; контролю-
ється легенями).
Оскільки Н2СО3 утворюється при гідратації розчиненого СО2, а концентрація останнього дорівнює рСО2, помноженому на коефіцієнт розчинності (0,03 мМ/л на 1 мм рт. ст.), то рівняння приймає вигляд:
[НСО3-]
рН = 6,1 + lg -------------------.
[0,03 рСО2]
Парціальний тиск СО2 у артеріальній крові людини знаходиться у рівновазі з таким у альвеолярному повітрі. Він дорівнює приблизно 40 мм рт. ст. при 37°С. Таким чином, кількість СО2, розчиненого в плазмі, а отже і концентрація Н2СО3, дорівнює:
[СО2]розч. = 0,03 рСО2 = 0,03 . 40 = 1,2 мМ/л.
За рахунок того, що легені, виводячи СО2 (респіраторний компонент буфера), підтримують кількість розчиненого СО2, а отже і Н2СО3, на постійному рівні, можна легко розрахувати концентрацію бікарбонату в позаклітинній рідині, необхідну для підтримання нормального рН.
[NaHCO3]
Так як відомо, що 7,4 = 6,1 + lg ----------------, то відповідно
[H2CO3]
[NaHCO3]
lg ---------------- = 1,3. Оскільки 1,3 = lg 20, то при нормальному рН
[H2CO3]
[NaHCO3]
крові співвідношення ---------------- = 20. Звідси, знаючи вміст у крові
[H2CO3]
Н2СО3, рівняння можна записати у такому вигляді:
24 мМ/л NaHCO3
7,4 = 6,1 + lg ----------------------------.
1,2мМ/л Н2СО3
Таким чином, ефективність роботи бікарбонатного буфера по підтриманню рН на нормальному рівні залежить від збереження співвідношення [бікарбонат]/ [СО2]розч. в межах близьких до 20, а резервні можливості цього буфера при нормальному рСО2 будуть найбільшими при концентрації бікарбонату в плазмі біля 24 мекв/л. Сталість респіраторного компоненту цього буфера залежить від роботи легень і дихального центру, а - метаболічного компоненту визначається діяльністю нирок. Відкритий характер і швидка регенерація бікарбонатного буфера забезпечує те, що переважна більшість кислот і лугів, які з`являються в організмі, нейтралізуються саме бікарбонатним буфером.
Механізми і форми порушень КОС. Оскільки буферна ємність позаклітинної рідини, а отже і її рН, визначаються головним чином станом бікарбонатного буфера, то очевидно, що зміна співвідношення респіраторного і метаболічного компонентів цього буфера призведе до порушення КОС організму. Так, ацидоз є патологічним станом, який характеризується зниженням рН або має тенденцію до зниження рН внаслідок зменшення співвідношення між метаболічним і респіраторним компонентами бікарбонатного буфера. В свою чергу алкалоз є патологічним станом, який характеризується підвищенням рН або має тенденцію до підвищення рН внаслідок збільшення співвідношення між метаболічним і респіраторним компонентами бікарбонатного буфера. Якщо внаслідок порушення виведення легенями СО2 виникне збільшення рСО2 понад 40 мм рт. ст., то це призведе до розвитку газового ацидозу. Якщо ж внаслідок гіпервентиляції рСО2 зменшиться, то виникне газовий алкалоз. Відповідно, при первинному зниженні концентрації бікарбонату в плазмі крові нижче 24 мекв/л виникне негазовий ацидоз, а при первинному підвищенні вмісту бікарбонату – негазовий алкалоз. Якщо при цьому рН, завдяки роботі механізмів компенсації, буде залишатися в межах норми, то тоді ацидоз і алкалоз будуть називатися компенсованими. Якщо ж внаслідок недостатності механізмів компенсації рН вийде за межі норми, то ацидоз і алкалоз будуть називатися декомпенсованими.
Взаємозв¢язок між КОС і електролітним обміном. Концентрація Н2СО3 в нормі залежить, як відомо, від рСО2 в альвеолярному повітрі та від газообміну в легенях. Виникають питання: від чого залежить концентрація бікарбонату, чому вона саме така і чому може змінюватися? Для того, щоб відповісти на ці питання, треба згадати, що згідно з законом електронейтральності, графічним вираженням якого є іонограма Гембла (рис. 1), сума катіонів у біологічних рідинах завжди дорівнює сумі аніонів, а всі катіони і аніони поділяються на:
1) фіксовані, вміст яких в організмі може змінюватися тільки внаслідок їх введення або виведення (до них відносяться Na+, K+, Ca2+, Mg2+, Cl-, HPO42- та інші);
2) напівфіксовані, які утворюються і метаболізуються в процесі обміну вуглеводів, жирів і білків з невисокою швидкістю (NH4+, лактат, піруват, кетонові тіла, білки);
3) нефіксовані, які утворюються і зникають в процесі метаболізму практично миттєво (бікарбонат та іон водню).
Якщо вміст у біологічних рідинах іонів водню цілком визначається станом буферних систем, головним чином бікарбонатного буфера, то концентрація бікарбонату, в свою чергу, визначається співвідношенням в біологічних рідинах фіксованих і напівфіксованих катіонів і аніонів. Саме швидка зміна концентрації бікарбонату забезпечує електронейтральність біологічних рідин в умовах зміни кількості інших аніонів чи катіонів. Надлишок катіонів, в першу чергу натрію, збільшує вміст нефіксованого аніону – бікарбонату, а нестача катіонів знижує його концентрацію. Виходячи з цього, можна вважати, що негазовий ацидоз виникає внаслідок зменшення бікарбонату, яке спричинюється зменшенням співвідношення між фіксованими катіонами і аніонами, а негазовий алкалоз виникає внаслідок збільшення бікарбонату, яке спричинюється збільшенням співвідношення між фіксованими катіонами і аніонами.
Класифікація негазових зрушень КОС. В залежності від причини, що призводить до порушення співвідношення катіонів і аніонів, негазовий ацидоз поділяється на:
1) метаболічний, що виникає внаслідок надмірного утворення лактату при гіпоксії та цукровому діабеті, а також внаслідок накопичення кетонових тіл при голодуванні та діабеті;
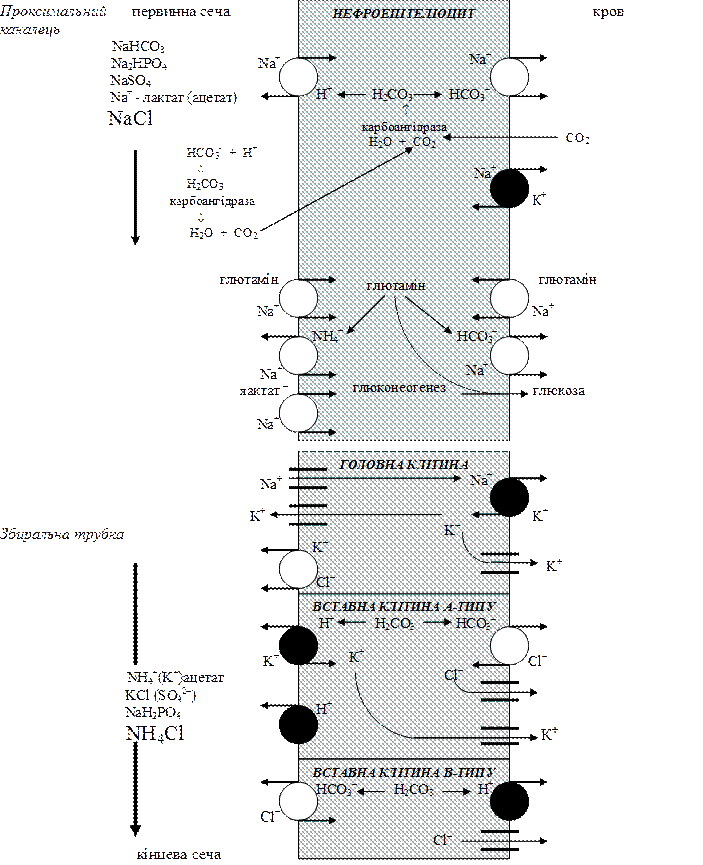
2) видільний, який може бути нирковим, що виникає або внаслідок порушення виведення аніонів нелетких кислот при значному зменшенні клубочкової фільтрації, або ж при порушенні функцій ниркових канальців. Останній ацидоз називається канальцевим і поділяється на декілька типів. Тип І (гіпокаліємічний дистальний канальцевий ацидоз) виникає при порушенні реабсорбції іонів калію в обмін на іони водню, що секретуються у вставних клітинах А-типу збиральних трубок, що проявляється неспроможністю знижувати рН сечі менше 5,3 в той час як в нормі рН може знижуватись до 4,5 (рис. 2). Тип ІІ (проксимальний канальцевий ацидоз) спостерігається при порушенні реабсорбції профільтрованого натрію бікарбонату. Під ІІІ типом розуміється ацидоз І типу в дітей. Тип ІV (гіперкаліємічний дистальний канальцевий ацидоз) пов`язаний з порушенням секреції K+ і Н+ в обмін на Na+ в головних клітинах збиральних трубок при гіпоальдостеронізмі або при резистентності до мінералокортикоїдів. Канальцевий ацидоз може виникати і при порушенні синтезу і секреції іонів амонію в проксимальних канальцях, що характерно для хронічної ниркової недостатності. Крім ниркового, до видільного відноситься також ацидоз, який виникає при підвищеному виведенні з кишечника натрію бікарбонату внаслідок діареї;
3) екзогенний, який виникає при введенні в організм кислот, наприклад, соляної або оцтової, або солей сильних кислот з катіонами, що метаболізуються, наприклад NH4Cl, який після проходження через печінку втрачає іон амонію при біосинтезі сечовини, внаслідок чого в кров потрапляє іон хлору. При вживанні етиленгліколю в організмі утворюється щавлева кислота, метанол перетворюється на мурашину кислоту, а етанол – на оцтову кислоту.
Негазовий алкалоз поділяється на:
1) видільний, який виникає або при підвищенні в нирках реабсорбції іонів натрію без супутніх іонів хлору при гіперальдостеронізмі та при тривалому введенні мінерало- чи глюкокортикоїдів, або при порушенні реабсорбції іонів хлору при введенні хлорних діуретиків, або при блюванні, коли організм втрачає Cl-;
2) екзогенний, який виникає при введенні в організм лугів чи солей з органічними аніонами, що метаболізуються, наприклад, натрію сукцинату або натрію лактату, при метаболізмі яких у кінцевому рахунку утворюється NaHCO3.
Механізми тимчасової компенсації порушень КОС. Негазовий ацидоз і алкалоз можуть тимчасово компенсуватися за рахунок зміни роботи легень (табл. 1). Так, при негазовому ацидозі внаслідок стимуляції іонами водню дихального центру виникає гіпервентиляція, що призводить до зниження рСО2, а при негазовому алкалозі спостерігається деяка затримка дихання, що дещо збільшує рСО2. При зниженні концентрації бікарбонату на 1 мекв/л рСО2 зменшується на 1,2 мм рт. ст.. Це дозволяє до певної міри зберігати нормальне співвідношення метаболічного і газового компонентів бікарбонатного буфера, а отже і підтримувати рН в межах норми, однак зменшує резервні можливості буферної системи, так як кількість NaHCO3 при цьому не відновлюється. Такий стан відповідає компенсованій стадії негазового ацидзу. Повну нормалізацію КОС позаклітинної рідини і всього організму при негазовому ацидозі та алкалозі здатні забезпечити тільки нирки.
Таблиця 1. Зміна основних параметрів КОС при його порушеннях, компенсаторних реакціях і відновленні
| Вид порушення | pН | [H+] | Основні порушення | Тимчасова компенсація | Остаточна корекція |
| Негазовий ацидоз | ¯ | | ¯ [HCO3-] | ¯ pCO2 | [HCO3-] |
| Негазовий алкалоз | | ¯ | [HCO3-] | pCO2 | ¯ [HCO3-] |
| Газовий ацидоз | ¯ | | pCO2 | [HCO3-] | ¯ pCO2 |
| Газовий алкалоз | | ¯ | ¯ pCO2 | ¯ [HCO3-] | pCO2 |
При газовому ацидозі нирки в свою чергу включаються в компенсаторні реакції, підсилюючи реабсорбцію натрію бікарбонату. Однак цей механізм менш ефективний і більш латентний, ніж гіпервентиляція. Так, при гострому респіраторному ацидозі концентрація бікарбонату плазми збільшується тільки на 1 мекв/л на кожні 10 мм рт. ст. підвищення рСО2. При хронічному газовому ацидозі на кожні 10 мм рт. ст. підвищення рСО2 бікарбонат плазми збільшується приблизно на 3,5 мекв/л. Повну і остаточну нормалізацію КОС при газовому ацидозі може забезпечити лише нормалізація системи зовнішнього дихання.
Крім того, швидке, часткове зменшення порушення нормального співвідношення фіксованих катіонів і аніонів, а отже і концентрації бікарбонатів крові, досягається за рахунок ще одного фізикохімічного механізму компенсації - іонообміну. При позаклітинному ацидозі з клітин виходять іони калію, а з кісток - іони кальцію, магнію та натрію. При цьому в клітини входять іони хлору. Кожна зміна рН на 0,1 ОД супроводжується протилежною зміною концентрації калію в плазмі приблизно на 0,6 мекв/л. Винятком є лише окремі різновиди ниркового канальцевого ацидозу та діарея, за яких організм втрачає разом з натрієм велику кількість калію. При позаклітинному алкалозі відбуваються прямо протилежні зміни. Виникає враження, ніби при ацидозі зайві іони водню заходять у клітини в обмін на іони калію. Насправді, цей процес значно складніший і точний механізм його досі лишається невстановленим, хоча, імовірно, він пов`язаний із зміною активності Na+,K+–АТФази, Na+/H+ і Cl-/HCO3- протипереносників та селективних калієвих каналів.
Значення нирок в остаточній корекції негазових порушень КОС визначається тим, що вони забезпечують виведення нелетких кислот; регенерують метаболічний компонент бікарбонатного буфера, який був витрачений на нейтралізацію сильних нелетких кислот; реабсорбують весь бікарбонат, який профільтрувався у первинну сечу. Проте дуже часто під виведенням кислот помилково розуміють екскрецію іонів водню. Однак виведення протонів без аніонів, по-перше, неможливе, а по-друге, воно не мало б ніякого сенсу, оскільки їх кількість в організмі залежить тільки від стану буферів. До того ж, кислоти, які вводяться в організм або утворюються в процесі метаболізму, потрапляють в нирки переважно вже в забуференому стані у вигляді натрієвих солей. Тому нема і можливості здійснювати екскрецію кислот як таких. Не можна виводити кислоти з організму і у вигляді натрієвих солей, оскільки це призвело б до втрати води з розвитком гіповолемії.
Виходячи з того, що головною патогенетичною ланкою нереспіраторних зрушень КОС організму є порушення співвідношення в позаклітинній рідині між фіксованими і напівфіксованими катіонами і аніонами, слід зрозуміти, що роль нирок у компенсаторних реакціях організму при негазовому ацидозі та алкалозі полягає у відновленні нормального співвідношення фіксованих катіонів і аніонів плазми крові. В цьомупроцесі роль нирок є визначальною, оскільки тільки вони здатні забезпечити ізоіонію крові.
При ацидозі задача нирок полягає у поверненні в кров відносно більшої кількості натрію ніж аніонів нелетких кислот. При алкалозі нирки виконують протилежну дію. Цю функцію нирки здійснюють за допомогою механізмів селективної реабсорбції та секреції катіонів і аніонів. Селективна реабсорбція натрію забезпечується обміном його на іони амонію, які утворюються в проксимальних канальцях нефрону, на іони водню, що утворюються та секретуються в проксимальних канальцях, товстій висхідній частині петлі Генле і у вставних клітинах А-типу збиральних трубок, а також – на іони калію, які секретуються в головних клітинах коркових збиральних трубок. При алкалозі вставні клітини В-типу коркових збиральних трубок секретують в сечу бікарбонат в обмін на хлор і секретують у кров іони водню і хлору. В цих обмінах приймають участь селективні іонні канали та переносники (рис. 2).
Натрій, більша частина якого реабсорбується у проксимальному відділі нефрону, повертається в кров у вигляді бікарбонату натрію. Бікарбонат, що потрапляє разом з натрієм в кров, та іони водню, що секретуються в просвіт канальців в обмін на натрій, утворюються в процесі реакції, що каталізується нирковою карбоангідразою. Секреція іонів водню в проксимальному відділі та в петлі Генле забезпечуе реабсорбцію NaHCO3, який профільтрувався з крові у первинну сечу. Частина іонів водню взаємодіючи з Na2HPO4, який профільтрувався, перетворює його на NaH2PO4, що дозволяє реабсорбувати іон натрію у вигляді NaHCO3.
Збереження основної кількості натрію та регенерація тим самим бікарбо-натного буфера, витраченого на нейтралізацію нелетких кислот при ацидозі, забезпечується нирковим амоніогенезом. Раніше прийнято було вважати, що в процесі ниркового амоніогенезу з глутаміну і частково з інших амінокислот утворюється аміак (NH3), який у просвіті ниркових канальців з`єднується з іоном водню і утворює амоній (NH4+), що є засобом виведенняз організму іонів водню. Однак тепер відомо, що рК системи аміак-амоній дорівнює 9,2. Це означає, що при рН 7,4 понад 99% аміака знаходиться у протонованому стані. Оскільки внутрішньоклітинне рН=7,0-7,2, то всередені клітин ниркових канальців вміст амонію в 10 тис. разів більше, ніж аміаку. Отже, амоніогенез не може бути засобом забуферювання та виведення з сечею іонів водню. Стало зрозумілим, що нирковий амоніогенез, разом з ацидогенезом і секрецією калію, є засобом, що дозволяє виводити з організму надлишок аніонів нелетких кислот без втрати іонів натрію, які реабсорбуються в обмін на іони амонію, які новоутворюються в нефроцитах і секретуються в сечу. Разом амоніогенез і карбоангідразна реакція забезпечують регенерацію бікарбонатного буфера.
Частина органічних аніонів реабсорбується епітелієм ниркових канальців та метаболізується в них до глюкози, яка потрапляє в кров. Решта органічних аніонів та надлишок всіх неорганічних аніонів виводиться з організму у вигляді амонійних і калієвих солей, а також у меншій кількості у вигляді, так званих, титрованих кислот, що являють собою переважно дігідрофосфати.
Регуляція ниркових ацидо-, амоніо- та глюконеогенезу, а також активності селективних іонних переносників і каналів здійснюється як місцево, під впливом метаболічних факторів (гіперкаліємія, рН, рСО2 та інші), так і дистантно – за допомогою нейрогуморальних факторів, серед яких зараз відомі катехоламіни, допамін, альдостерон, ангіотензін ІІ, глюкокортикоїди, інсулін, вазопресин, паратгормон та інші, механізми впливу яких на ниркові процеси при порушеннях КОС вивчаються.
Відновлення, завдяки роботі нирок, нормального співвідношення фіксованих катіонів і аніонів плазми крові автоматично відновлює нормальну концентрацію бікарбонату, а отже і нормалізує КОС організму.
Патогенетична роль механізмів компенсації порушень КОС. Механізми компенсації, що включаються при порушеннях КОС, можуть грати і патогенетичну роль. Так, при негазовому ацидозі виникають гіперкаліємія, гіперкальціємія та гіпокапнія, а при негазовому алкалозі - гіпокаліємія і гіпокальціємія. Гіперкаліємія може викликати зупинку серця, а гіпокаліємія - м`язову слабкість, гіпотонію, аритмії. Гіпокальціємія здатна призвести до судом і тетанії. Гіпокапнія супроводжується головокружінням, сонливістю, зниженням тонусу судин і може викликати втрату свідомості. Виведення кальцію з кісток при тривалому ацидозі призводить до остеопорозу і нефролітіазу. Видалення при алкалозі з організму надлишка NaHCO3 може спричинити гіповолемію.
Напруження регуляторних систем організму, яке супроводжує порушення КОС призводить до їх дизбалансу, що викликає різноманітні патологічні зміни. Так, негазовий ацидоз викликає викид катехоламінів і активацію симпатичного відділу вегетативної нервової системи з одночасним підвищенням тонусу парасимпатикусу і зниженням чутливості a- і b-адренорецепторів. Все це викликає вегето-судинну дистонію, бронхоспазм, підвищення секреції слизу, блювання, пронос. При негазовому алкалозі підвищується збудливість b-адренорецепторів серця, судин, бронхів, кишечника; знижується тонус вагуса, що супроводжується тахікардією, зниженням артеріального тиску, уповільненням перистальтики кишечника.
Патологічний вплив порушень КОС на обмін вуглеводів. Помірний компенсований ацидоз значно підвищує зв`язування інсуліну з рецепторами і знижує спорідненість тканин до глюкагону (Кришталь Н.В., 1989). Значний декомпенсований ацидоз спричинює інсулінорезистентність. Як хронічний негазовий ацидоз, так і хронічний негазовий алкалоз викликають гіперглікемію натще та знижують толерантність до глюкози. Першопричиною діабетогенної дії хронічного ацидозу є виснажлива стимуляція В-клітин гіперглікемією, яка є наслідком підсилення неоглюкогенезу обумовленого гіперпродукцією глюкокортикоїдів. Алкалоз спричинює первинну пригнічуючу дію на В-клітини та активує А-клітини острівців Лангерганса (Кришталь Н.В., Гареева Э.Г., 1993).
Принципи корекції порушень КОС полягають у лікуванні захворювань, які стали першопричиною виникнення порушення рСО2 або [HCO3-]. При негазовому ацидозі чи алкалозі необхідно виявити причину порушення нормального співвідношення між фіксованими катіонами і аніонами та усунути її. Якщо це неможливо зробити швидко, то доцільним буде нормалізація буферних систем організму і усунення супутніх розладів водно-мінерального обміну та симптоматичне лікування.
Рис. 1. Іонограма Гембла. Залежність концентрації НСО3- від співвідношення інших аніонів і катіонів:
А – норма;
Б – гіпонатріємічний ацидоз (видільний);
В – лактат - чи кетоацидоз (метаболічний);
Г – гіперхлоремічний ацидоз (екзогенний);
Д – гіпохлоремічний алкалоз (видільний);
Е – гіпернатріємічний алкалоз (екзогенний).
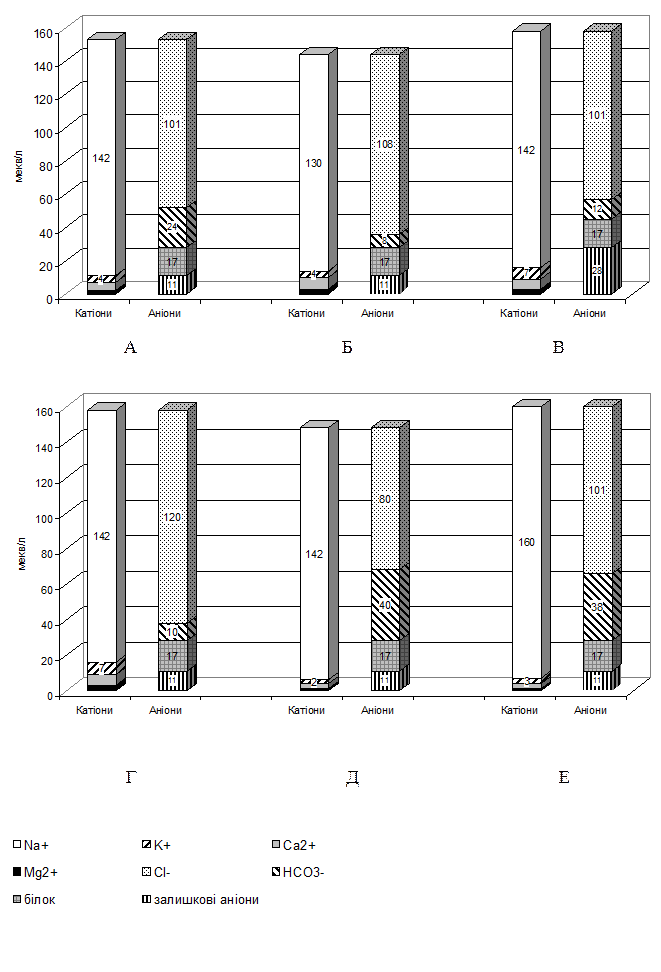 Рис. 2. Нирковий ацидогенез, амоніогенез і глюконеогенез.
Рис. 2. Нирковий ацидогенез, амоніогенез і глюконеогенез.
Лекція д.м.н., професора: Порушення водно-електролітного обміну
Водно-електролітний обмін (ВЕО) – цездатність організму підтримувати в собі постійну кількість води з певним перерозподілом її між водними секторами або компартментами із суворим підтриманням їх іонного складу.
Нормальна життєдіяльність клітин, які є основною морфо-функціональною одиницею людського організму, може здійснюватись лише за умови оточення їх водним розчином постійного складу, який Клод Бернар назвав внутрішнім середовищем організму. Вода, яка є універсальним біологічним розчинником, знаходиться також і в середині клітин, що забезпечує обмін речовин і метаболізм. Причому, якщо склад внутрішньоклітинних розчинів дещо відрізняється в різних органах і організмах, то іонний склад міжклітинної рідини завжди однаковий і схожий з океанською водою (табл. 1). Це пов¢язане з тим, що перші клітини виникли і міліарди років розвивались у первісному океані, неорганічний склад якого багатоклітинні організми навчилися підтримувати штучно, щоб забезпечити гомеостаз своїх клітин.
Таблиця 1. Середній склад основних іонів у біологічних рідинах людини
| Рідина | Na+,мекв/л | К+, мекв/л | Cl-, мекв/л | НСО3-,мекв/л |
| Внутрішньоклітинна | 12-38 | 100-150 | 4-50 | |
| Плазма | 4,5 | |||
| Міжклітинна | 4,4 | |||
| Шлунковий сік | ||||
| Вміст тонкої кишки | ||||
| Вміст товстої кишки | ||||
| Діарейна рідина | ||||
| Піт |
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1197; Нарушение авторских прав?; Мы поможем в написании вашей работы!