
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гідратація іонів у водному розчині
|
|
|
|

| 
|
| Рис. 6.3. Гідратація іонів у водному розчині |
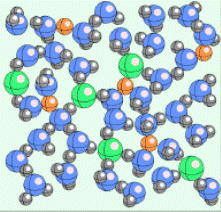
Полярні молекули води активно взаємодіють із іонами, формуючи навколо них гідратаційну оболонку. Кисневі кінці молекул води повернуті до катіонів, а водневі - до аніонів (рис. 6.3). Згідно сферичної моделі гідратації іонів Gurney (1962) можна виділити дві зони в гідратаційній оболонці навколо іону (рис. 6.4)
  
| 
|
| Рис. 6.4. Сольватаційна оболонка навколо іона | |
| В розбавленому розчині | В концентрованому розчині сольватаційнісфери зближуються, друга гідратаційна оболонка зникає, зникають вільні, не пов’язані із сольватацією, молекули води. |
Ближня до іону високо-впорядкована зона (перша сольватаційна оболонка) характеризується тісним зв‘язком молекул води із іоном, їхньою радіальною орієнтацією відносно іону і переміщується разом із іоном при його русі. Вона має низьку ентропію і малу густину. Дальше від іону вона поступово переходить у невпорядковану зону, де молекули води розміщуються хаотично під впливом як електричного поля іону, так і навколишньої води із острівками тетраедричної структури. Ця друга сольватаційна зона має максимальну ентропію і високу густину.
Гідратизація – це специфічна хімічна реакція, що супроводжується сильним зниженням вільної енергії. (вільна енергія сольватації ~ -400 кДж·мол-1 при 25°С).
Вивільнення іону із першої сольватаційної оболонки потребує значної енергії - енергії сольватації. Для NaCl ця енергія складає -765 кДж/моль. Кількість молекул води в першій сольватаційній оболонці називається числом сольватації. Звичайно, катіони характеризуються більшою гідратацією, ніж аніони, при одному і тому ж розмірі та заряді. Це пов’язано із тим що позитивна область водного диполя більш розмита, розсіяна в порівнянні із негативною. Невеликі, позитивно зяряджені катіони, такі як Lі+, Na+, H3O+, Ca2+, Ba2+, Mg2+ є сильно гідратизованими, що веде до організації молекул води (структуризації), а значить до зниження ентропії і загальної густини розчину та росту в’язкості. В протилежність цьому, великі катіони та деякі аніони викликають зворотні ефекти, пов’язані із руйнуванням структури розчину (K+, NH3+, Rb+, Cl-, Br-, NO3-). Гідратизація сильно збільшує електростатичний радіус катіонів і аніонів (відповідно, 0,9 Å і 0,1 Å на одиницю заряду).
|
|
|
Гідратаційний радіус деяких іонів наказаний на схемі на рис. 6.5. Максимальний приріст спостерігається в протону H+, Be2+, Li+.

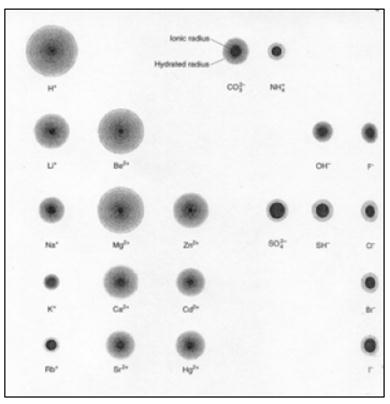
Рис. 6.5. Схема, що показує співвідношення іонного та гідратаційного радіусів іонів.
Комбінація гідратизації і діелектричної сталої викликає надзвичайно розчинну здатність води по відношенню до іонний сполук в широкому інтервалі P і T.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1031; Нарушение авторских прав?; Мы поможем в написании вашей работы!