
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Мультиферментные комплексы
|
|
|
|
Наиболее эффективно происходит регуляция в так называемых мульти-ферментных комплексах. Эти комплексы представляют собой несколько ферментов, катализирующих ряд согласованных реакций, причем конечные продукты одной ферментативной реакции являются исходными субстратами для следующей ферментативной реакции. Различают три типа мультиферментных комплексов:
• ферменты растворены в цитоплазме и контакт субстратов с ними осуществляется посредством диффузии;
• ферменты соединены друг с другом за счет белок-белковых взаимодействий;
• ферменты соединены друг с другом и иммобилизованы на внутриклеточных или цитоплазматических мембранах.
В каждом мультиферментном комплексе имеется, по крайней мере, один аллостерический фермент, осуществляющий регуляцию суммарной реакции всего ферментного ансамбля. Чаще всего этот фермент катализирует скорость первой (самой медленной) реакции, а его отрицательным модулятором является конечный продукт всего процесса в целом.
Ниже представлена схема, изображающая мультиферментную систему, в которой продукт последней реакции является отрицательным эффектором аллостерического фермента Е^
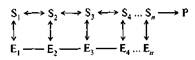
Мультиферментные системы могут включать в себя до 20 различных ферментов, функционирующих в определенной последовательности.
В настоящее время изучены многие мультиферментные комплексы, функционирующие на разных этапах метаболизма. Одним из таких комплексов является совокупность ферментов, катализирующих синтез пиримидинов из ас-партата в бактериальных клетках. Аллостерическим ферментом в данном случае является аспартат-карбомоилаза, катализирующая первую стадию процесса, а именно превращение аспартата в карбомоиласпартат.
Регуляция ферментативной активности может осуществляться за счет ограниченного протеолиза. Многие протеиназы, функционирующие вне клеток, например в крови или в пищеварительном тракте, синтезируются в виде неактивных предшественников. Активация их связана с гидролизом некоторых пептидных связей в полипептидной цепи. В качестве примера можно привести ферменты свертывания крови, а также такие ферменты пищеварительного тракта, как трипсин и химотрипсин и др.
Регуляция ферментативной активности может осуществляться за счет ковалентной обратимой модификации новосинтезированных белковых макромолекул. Это связано в первую очередь с ферментативным присоединением к ним низкомолекулярных химических группировок в результате фосфорилиро-вания, гликозилирования, метилирования и т. д. Присоединение фосфатной группы к гидроксилу аминокислотного остатка полипептидной цепи может как увеличить, так и снизить ферментативную активность. Примером тому может служить фосфорилаза — фермент, катализирующий отщепление остатков глюкозы от гликогена. В исходном состоянии он неактивен, но при фос-форилировании, осуществляемом посредством фермента протеинкиназы, происходит его активация и вовлечение в процесс метаболизма глюкозы. Напротив, фермент гликогенсинтаза активен в исходном состоянии, а при фос-форилировании его активность резко снижается.
Эффективным инструментом регуляции каталитической активности является молекулярная гетерогенность ферментов, обусловленная как генетическими, так и эпигенетическими факторами.
В настоящее время около половины идентифицированных ферментов находятся в клетках и тканях в виде множественных молекулярных форм, имеющих единую субстратную специфичность, но отличающихся по физико-химическим или иммунологическим свойствам. Генетическая основа молекулярной гетерогенности обусловлена наличием нескольких генов, каждый из которых кодирует одну субъединицу фермента или одну его молекулярную форму. Кроме того, различные молекулярные формы одного и того же фермента могут кодироваться в одном генном локусе, имеющем множественные аллели. Генетически детерминированные молекулярные формы называются изоэнзи-мами. Посттрансляционные модификации ферментов, обусловленные локальным протеолизом, ковалентными модификациями, белок-белковыми взаимодействиями и т.д., являются причиной образования множественных молекулярных форм, не являющихся истинными изоэнзимами, но играющими существенную роль в метаболических процессах. Наиболее часто встречаются так называемые конформеры — молекулярные формы, имеющие одинаковую первичную структуру, но отличающиеся по своей конформации. Это возможно в том случае, если эти конформации достаточно устойчивы, т. е. соответствуют уровню свободной энергии, близкой к минимальной. Только такие кон-формационные варианты белков, которые воспроизводимо фиксируются посредством электрофоретических, хроматографических или иных методов, могут рассматриваться как конформеры.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 5995; Нарушение авторских прав?; Мы поможем в написании вашей работы!