
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Способы выражения концентрации, имеющие размерность
|
|
|
|
Объёмно-весовая концентрация Сг/л – показывает, какая масса растворенного вещества, выраженная в граммах, содержится в единице объёма раствора Vр-р:
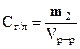 (4)
(4)
Молярная концентрация или молярность, СМ – количество растворённого вещества в молях, отнесённое к объёму раствора, выраженному в литрах:
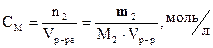 (5)
(5)
. Нормальная концентрация или нормальность, СN – количество эквивалентов, nэ2 растворённого вещества, содержащееся в одном литре раствора:
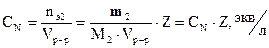 (6)
(6)
Для сложных химических соединений Z вычисляется следующим образом:
а) для кислот Z соответствует основности кислоты, т. е. числу атомов водорода в составе кислоты, обмениваемых в данной реакции на металл или нейтрализуемых основанием.
б) для оснований Z соответствует кислотности основания, т.е. числу гидроксильных групп в составе основания, обмениваемых на кислотный остаток или нейтрализуемых кислотой.
в) для солей Z рассчитывают как произведение числа атомов и степени окисления металла в составе соли.
г) в реакциях окисления-восстановления Z- число электронов, переданных в ходе полуреакции окисления или восстановления соответственно восстановителю или окислителю.
Титр (Т) определяет количество граммов растворённого вещества
в 1 мл раствора. Фактически
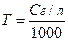
Расчёт титра на основе нормальности раствора выполняют по формуле:
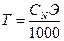
где СN, экв/л– нормальная концентрация раствора, Э, г/экв. – эквивалентнаяя масса растворённого вещества.
Например, для 3н раствора Н3РО4
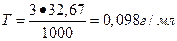
Моляльная концентрация или моляльность, также известная как практическая шкала концентраций, m– количество растворённого вещества в молях, отнесённое к массе растворителя:
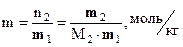 (7)
(7)
Практическая шкала концентраций имеет ряд преимуществ. Моляльная концентрация не зависит от температуры раствора. Изменение содержания какого-либо компонента раствора или добавление ещё одного не влечёт за собой изменения концентрации остальных. Всё это обусловило широкое применение практической шкалы концентраций в горном деле и добывающей промышленности.
|
|
|
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 462; Нарушение авторских прав?; Мы поможем в написании вашей работы!