
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекарственные растения и сырье, содержащие дубильные вещества
|
|
|
|
Тема лекции
Лекция № 11
1. Понятие о дубильных веществах.
2. Распространение дубильных веществ в растительном мире.
3. Роль дубильных веществ для жизни растений.
4. Классификация дубильных веществ.
5. Биосинтез, локализация и накопление дубильных веществ в растениях.
6. Особенности сбора» сушки и хранения сырья, содержащего дубильные вещества.
7. Физические и химические свойства дубильных веществ.
8. Оценка качества сырья, содержащего дубильные вещества. Методы анализа.
9. Сырьевая база лекарственных растений, содержащих дубильные вещества.
10.Пути использования сырья, содержащего дубильные вещества.
11..Медицинское применение и препаратов, содержащих дубильные вещества.
12.Лекарственные растения и сырье, содержащие дубильные вещества
Понятие о дубильных веществах
Дубильные вещества ДВ (танниды) - это сложные смеси растительных высокомолекулярных полимеров фенольных соединений с молекулярной массой от 500 до 3000, обладающие вяжущим вкусом, способные образовывать прочные связи с белками, превращая невыделанную шкуру животных в дубленую кожу.
Сущность процесса дубления заключается в образовании прочных водородных связей между фенольными гидроксилами ДВ и атомами водорода и азота молекул белка - коллагена. В результате возникает прочная поперечно связанная структура - кожа, устойчивая к воздействию тепла, влаги, микроорганизмов, ферментов, т.е. не поддающаяся гниению.
Полифенольные соединения с более низкой М.м. (менее 500) только адсорбируются на белках, но не способны образовывать устойчивые комплексы, и в качестве дубителей не используются. Высокомолекулярные полифенолы (с М.м. более 3000) также не являются дубителями, так как их молекулы слишком велики и не проникают между фибриллами коллагена.
Таким образом, главное отличие ДВ от других полифенол ьных соединений - это способность образовывать прочные водородные связи с белками.
Термин «дубильные вещества» был впервые использован французским ученым Сегеном в 1796 году для обозначения присутствующих в экстрактах некоторых растений веществ, способных осуществлять процесс дубления. Другое название ДВ - «танниды» — происходит от латинизированной формы кельтского названия дуба - «тан», кору которого издавна использовали для обработки кож.
Первые научные исследования в области химии ДВ относятся ко второй половине 18 века. Они были вызваны практическими запросами кожевенной промышленности. Первая опубликованная работа - работа Гледича в 1754 году «Об использовании плодов черники, как сырья для получения дубильных веществ». Первой монографией была монография Деккера в 1913 году, которая обобщала весь накопленный материал по дубильным веществам. Поиском, выделением и установлением структуры ДВ занимались отечественные ученые Л. Ф. Ильин, А. Л. Курсанов, М. Н. Запрометов, Ф. М. Флавицкий, Г. Поварнин А. И. Опарин и др.; зарубежные ученые Г. Проктер, К. Фрейденберг, Э. Фишер, П. Каррер и др.
Распространение дубильных веществ в растительном мире
ДВ широко распространены в растительном мире. Встречаются преимущественно в высших растениях, наиболее распространены в представителях двудольных, где они накапливаются в максимальных количествах. Однодольные обычно не содержат ДВ, в папоротниках ДВ встречаются, а у хвощей, мхов, плаунов их почти нет, или они находятся в минимальных количествах. Наиболее высоким содержанием ДВ отличаются семейства: сумаховые -Anacardiaceae (сумах дубильный, скумпия кожевенная), розоцветные - Rosaceae (кровохлебка лекарственная, лапчатка прямостоячая), буковые - Fagaceae (дуб черешчатый и скальный), гречишные - Polygonaceae (горец змеиный и мясо-красный, вересковые - Ericaceae (толокнянка, брусника), березовые - Betulaceae (ольха серая и клейкая) и др.
Содержание таннидов в растениях доходит до 20-30%, наивысшее содержание ДВ найдено в патологических образованиях - галлах (до 50-70%).
Роль дубильных веществ для жизни растений
Биологическая роль для жизни растений до конца не выяснена. Существует несколько гипотез:
1). ДВ выполняют защитную функцию, т.к. при повреждении растений они образуют комплексы с белками, которые создают защитную пленку, препятствующую проникновению фитопатогенных организмов. Обладают бактерицидными и фунгицидными свойствами;
2). ДВ участвуют в окислительно-восстановительных процессах, являются переносчиками кислорода в растениях;
3). ДВ - одна из форм запасных питательных веществ. На это указывает их локализация в подземных органах и коре;
4). ДВ - отбросы жизнедеятельности растительных организмов.
Классификация дубильных веществ
Так как ДВ это смеси различных полифенолов, из-за разнообразия их химического состава классификация затруднена.
Наибольшее признание получила классификация Г. Поварнина (1911) и К. Фрейденберга (1920), основанная на химической природе ДВ и их отношении к гидролизующим агентам. Согласно этой классификации ДВ делятся на 2 большие группы:
1) гидролизуемые ДВ;
2) конденсированные ДВ.
1. Гидролизуемые ДВ
Гидролизуемые ДВ - это смеси сложных эфиров фенолкарбоновых кислот с сахарами и несахаридами. В водных растворах под действием кислот, щелочей и ферментов они способны гидролизоваться на составные фрагменты фенольной и нефенольной природы. Гидролизуемые ДВ можно разделить на 3 группы.
1.1. Галлотаннины -эфиры галловой, дигалловой кислот и других ее полимеров с циклическими формами Сахаров.
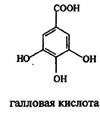
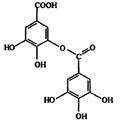
м-дигалловая кислота (депсид - D)
Важнейшие источники галлотаннинов, применяемых в медицине - галлы турецкие, образующиеся на дубе лузитанском и китайские, образующиеся на сумахе полукрылатом, листья сумаха дубильного и скумпии кожевенной.
Танин представляет собой гетерогенную смесь веществ различного строения. Встречаются моно-, да-, три-, тетра-, пента- и полигаллоильные эфиры.
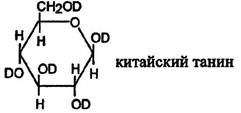 По мнению Л. Ф. Ильина, Э. Фишера и К. Фрейденберга китайский танин представляет собой пента-М-дигаллоил-β-D-глюкозу, т.е. β-D-глюкозу, гидроксильные группы которой этерифицированы М-дигалловой кислотой.
По мнению Л. Ф. Ильина, Э. Фишера и К. Фрейденберга китайский танин представляет собой пента-М-дигаллоил-β-D-глюкозу, т.е. β-D-глюкозу, гидроксильные группы которой этерифицированы М-дигалловой кислотой.
По мнению П. Каррера китайский танин представляет собой гетерогенную смесь веществ различного строения, гидроксильные группы глюкозы могут быть этерифицированы галловой, дигалловой и тригалловой кислотами.
К. Фрейденберг предполагал, что у турецкого таннина в среднем одна из пяти гидроксильных групп глюкозы свободна, другая этерифицирована М-дигалловой кислотой, а остальные - галловой кислотой.
ДВ этой, группы содержатся и преобладают в корневищах и корнях кровохлебки» корневищах змеевика, бадана, соплодиях ольхи, коре дуба, листьях гамамелиса.
1.2. Эллаготапнины -эфиры эллаговой и других кислот, имеющих с нейбиогенетическое родство, с циклическими формами Сахаров. Содержатся в корке плодов гранатника, коре эвкалипта, кожуре грецкого ореха, листьях и соцветиях кипрея (иван-чая).
1.3. Несахаридные эфиры фенолкарбоновых кислот -эфиры галловой кислоты с хинной, хлорогеновой, кофейной, оксикоричной кислотами и с флава-нами.
Пример: теогаллин, обнаруженный в листьях чая китайского, представляющий собой эфир хинной и галловой кислот (3-О-галлоилхинная кислота ).
2. Конденсированные ДВ
Конденсированные ДВ не обладают эфирным характером, полимерная цепь этих соединений образована посредством углерод-углеродных связей (-C-С-), что обусловливает их прочность к воздействию кислот, щелочей и ферментов. При действии минеральных кислот они не расщепляются, а увеличивают М.м. с образованием продуктов окислительной конденсации - флобафенов или красеней красно-коричневого цвета.
Конденсированные ДВ -это продукты конденсации катехинов (флаван-3-олов), лейкоантоцианидинов (флаван-3,4-диолов), реже оксистильбенов (фенилэтиленов).
Образование конденсированных ДВ может идти двумя путями. По К. Фрейденбергу, оно сопровождается разрывом пиранового кольца катехинов, и С2-атом одной молекулы соединяется углерод-углеродной связью с С6- или C8-атомом другой молекулы.
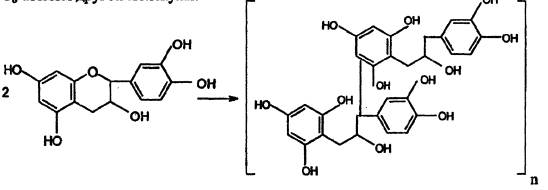
По Д. Е. Хатуэю, конденсированные ДВ образуются в результате ферментативной окислительной конденсации молекул по -типу «голова к хвосту» (кольцо А к кольцу В) или «хвост к хвосту» (кольцо В к кольцу В) по положениям 6'-8; 6 -2` и др.
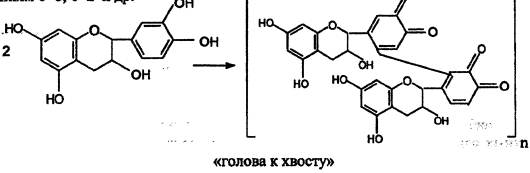
Конденсированные ДВ содержатся и преобладают в коре калины, корневищах лапчатки, плодах черники, черемухи, траве зверобоя, листьях чая.
В состав смесей ДВ входят также простые фенолы (резорцин, пирокатехин, пирогаллол, флороглюцин и др.) и свободные фенолкарбоновые кислоты (галловая, эллаговая, протокатеховая и др.).
Чаще всего в растениях встречается смесь гидролизуемых и конденсированных ДВ с преобладанием той или иной группы, поэтому классифицировать их по типу ДВ достаточно сложно, В некоторых видах сырья почти одинаковое содержание обеих групп ДВ (например, корневища змеевика).
Биосинтез, локализация и накопление дубильных веществ в растениях
Биосинтез гидролизуемых ДВ идет по шикиматному пути, конденсированные ДВ образуются по смешанному пути (шикиматному и ацетатно-малонатному). ДВ находятся в растворенном состоянии в вакуолях растительных клеток и отделены от цитоплазмы белково-липоидной мембраной - танопластом, при старении клеток адсорбируются на клеточных стенках.
Локализуются в клетках эпидермиса, обкладочных клетках, окружающих сосудисто-волокнистые пучки (жилки листьев), в паренхимных клетках сердцевинных лучей, коры, древесины и флоэмы.
ДВ накапливаются, главным образом, в подземных органах многолетних травянистых растений (корневища бадана, змеевика, лапчатки, корневища и корни кровохлебки), в корен древесине деревьев и кустарников (кора дуба, калины), в плодах (плоды черемухи, черники, соплодия ольхи), реже в листьях (листья скумпии, сумаха, чая).
Накопление таннидов зависит от генетических факторов, климатических и экологических условий. У травянистых растений, как правило, минимальное количество ДВ отмечается весной в период отрастания, затем их содержание увеличивается и достигает максимума в период бутонизации и цветения (например, корневища лапчатки). К концу вегетации количество ДВ постепенно снижается. У кровохлебки максимум ДВ накапливается в фазу развития розеточных листьев, в фазу цветения их содержание снижается, а осенью вновь увеличивается. Фаза вегетации влияет не только на количество, но и на качественный состав ДВ. Весной, в период сокодвижения, в коре деревьев и кустарников и в фазу отрастания у травянистых растений преимущественно накапливаются гидролизуемые ДВ, а осенью в фазу отмирания растений - конденсированные ДВ и продукты их полимеризации - флобафены (красени).
Наиболее благоприятными для накопления таннидов являются условия умеренного климата (лесная зона и высокогорный альпийский пояс).
Наибольшее содержание ДВ отмечено у растений, произрастающих на плотных известковых почвах, на рыхлых черноземных и песчаных почвах их содержание меньше. Способствуют накоплению ДВ богатые фосфором почвы, богатые азотом почвы снижают содержание таннидов.
Особенности сбора, сушки и хранения сырья, содержащего дубильные вещества
Заготовку сырья проводят в период максимального накопления ДВ.
Собранное сырье сушат на воздухе в тени или в сушилках при температуре 50-60 градусов. Подземные органы и кору дуба можно сушить на солнце.
Хранят в сухих, хорошо проветриваемых помещениях без доступа прямых солнечных лучей по общему списку в течение 2-6 лет.
Физические и химические свойства дубильных веществ
ДВ выделяются из растительного сырья в виде смеси полимеров и представляют собой аморфные вещества желтого или желто-бурого цвета, без запаха, вяжущего вкуса, очень гигроскопичные. Хорошо растворяются в воде (особенно в горячей) с образованием коллоидных растворов, растворимы также в этиловом и метиловом спирте, ацетоне, этилацетате, бутаноле, пиридине. Не растворимы в хлороформе, бензоле, диэтиловом эфире и других неполярных растворителях, оптически активны.
Легко окисляются на воздухе. Способны образовывать прочные межмолекулярные связи с белками и другими полимерами (пектиновые вещества, целлюлоза и др.). Под действием фермента таназы и кислот гидролизуемые ДВ распадаются на составные части, конденсированные ДВ - укрупняются.
Из водных растворов осаждаются желатином, алкалоидами, основным ацетатом свинца, бихроматом калия, сердечными гликозидами.
Как вещества фенольной природы, ДВ легко окисляются перманганатом калия в кислой среде и другими окислителями, образуют окрашенные комплексы с солями тяжелых металлов, трехвалентного железа, бромной водой.
Способны легко адсорбироваться на кожном порошке, целлюлозе, клетчатке, вате.
Оценка качества сырья, содержащего дубильные вещества,
Методы анализа
Для получения суммы ДВ растительное сырье экстрагируют горячей водой в соотношении 1:30 или 1:10.
Качественный анализ
Используют качественные реакции (осаждения и цветные) и хроматографическое исследование.
1. Специфической реакцией является реакция осаждения желатином, используют 1%-ный раствор желатина на 10%-ном растворе хлорида натрия. Появляется хлопьевидный осадок или муть, растворимые в избытке желатина. Отрицательная реакция с желатином свидетельствует об отсутствии ДВ.
2. Реакция с солями алкалоидов, используют 1% раствор солянокислого хинина. Появляется аморфный осадок за счет образования водородных связей между гидроксильными группами ДВ и атомами азота алкалоида.
Эти реакции дают одинаковый эффект независимо от группы ДВ, Ряд реакций позволяют определить группу ДВ.
Качественные реакции на ДВ
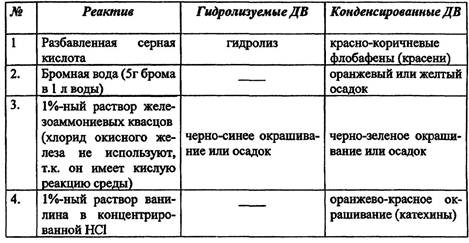
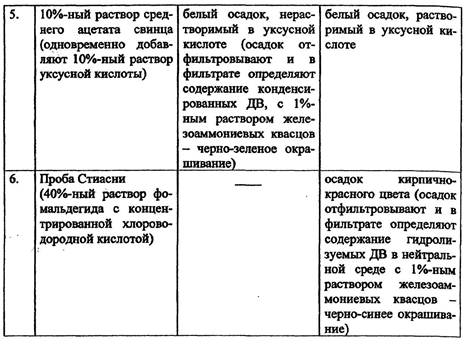
Реакция с 1%-ным спиртовым раствором железоаммониевых квасцов - эта реакция фармакопейная, проводится как с отваром из сырья (ГФ-XI - кора дуба, корневище змеевика, соплодия ольхи, плоды черники), так и для открытия ДВ непосредственно в сухом сырье (ГФ-XI - кора дуба, кора калины, корневища бадана).
Количественное определение
Известно около 100 различных методов количественного определения ДВ, которые можно разделить на следующие основные группы.
1. Гравиметрические или весовые — основаны на количественном осаждении ДВ желатином, ионами тяжелых металлов или адсорбцией кожным (гольевым) порошком.
Для технических целей во всем мире стандартным является гравиметрический метод с применением гольевого порошка - весовой единый метод (ВЕМ).
Водный экстракт ДВ делят на две равные части. Одну часть экстракта выпаривают и высушивают до постоянной массы. Другую часть экстракта обрабатывают кожным порошком и фильтруют. ДВ адсорбируются на кожном порошке и остаются на фильтре. Фильтрат и промывные воды выпаривают ивысушивают до постоянной массы. Содержание ДВ рассчитывают по разнице в массе сухих остатков.
Метод неточный, т.к. кожный порошок адсорбирует и низкомолекулярные фенольные соединения, довольно трудоемкий и дорогой.
2. Титринетрические методы. К ним относятся:
а) Желатиновый метод - основан на способности ДВ образовывать нерастворимые комплексы с белками. Водные извлечения из сырья титруют 1% раствором желатина, в точке эквивалентности комплексы желатино-таннаты растворяются в избытке реактива. Титр устанавливают по чистому таннину. Точку эквивалентности определяют путем отбора наименьшего объема титрованного раствора, вызывающего полное осаждение ДВ.
Метод наиболее точный, т.к. позволяет определить количество истинных ДВ. Недостатки: длительность определения и трудность установления точки эквивалентности.
б) Перманганатометрический метод ( метод Левенталя в модификации А. П. Курсанова). Это фармакопейный метод, основан на легкой окисляемости ДВ перманганатом калия в кислой среде в присутствии индикатора и катализатора индигосульфокислоты, которая в точке эквивалентности переходит в изатин, и цвет раствора меняется от синего до золотисто-желтого.
Особенности определения, позволяющие оттитровать только макромолекулы ДВ: титрование проводится в сильно разбавленных растворах (извлечение разбавляется в 20 раз) при комнатной температуре в кислой среде, перманганат калия добавляется медленно, по каплям, при интенсивном перемешивании.
Метод экономичный, быстрый, прост в исполнении, но недостаточно точный, т.к. перманганат калия окисляет частично и низкомолекулярные фенольные соединения.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 15500; Нарушение авторских прав?; Мы поможем в написании вашей работы!