
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Испарение и кипение жидкостей
|
|
|
|
При рассмотрении уравнения Ван-дер-Ваальса было установлено, что в определенных условиях жидкость может находиться в равновесии со своим паром, который в данном случае называется насыщенным. Такое равновесие устанавливается само собой, если жидкость находится в закрытом сосуде. Процесс установления равновесия происходит следующим образом.
С поверхности жидкости вылетает часть молекул, образуя над жидкостью пар. Для выхода из жидкости испаряющиеся молекулы должны преодолеть силы притяжения со стороны оставшихся молекул, т.е. совершить работу против этих сил. Кроме того, должна быть совершена работа против сил давления уже образовавшегося пара, равная 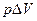 , где
, где  - изменение объема, занимаемого данным количеством молекул при переходе в пар. Вся эта работа совершается только за счет кинетической энергии теплового движения молекул, следовательно, выход молекул, способных совершить эту работу, приводит к уменьшению числа быстрых молекул в жидкости. Жидкость охлаждается. Однако наступает момент, когда число покидающих жидкость молекул, сравнивается с числом молекул, возвращающихся в жидкость, что происходит вследствие хаотического движения их в паре.
- изменение объема, занимаемого данным количеством молекул при переходе в пар. Вся эта работа совершается только за счет кинетической энергии теплового движения молекул, следовательно, выход молекул, способных совершить эту работу, приводит к уменьшению числа быстрых молекул в жидкости. Жидкость охлаждается. Однако наступает момент, когда число покидающих жидкость молекул, сравнивается с числом молекул, возвращающихся в жидкость, что происходит вследствие хаотического движения их в паре.
Переход молекул из жидкости в пар называется испарением, а обратный переход из пара в жидкость – конденсацией.
Плотность пара в состоянии равновесия с жидкостью отвечает вполне определенному давлению, которое называется упругостью насыщенного пара. Упругость насыщенного пара растет с температурой, так как, чем выше температура, тем большее число молекул имеют энергетическую возможность покинуть жидкость и перейти в пар.
Поскольку при испарении жидкость должна охлаждаться, то для проведения процесса испарения при постоянной температуре к жидкости необходимо подводит тепло.
Количество теплоты, которое необходимо подвести для испарения определенного количества жидкости в изотермическом режиме называется скрытой теплотой испарения.
Скрытой она называется потому, что подвод ее не сопровождается повышением температуры жидкости. Количество теплоты, необходимое для изотермического испарения одного моля жидкости называется молярной скрытой теплотой испарения. Соответственно, удельная скрытая теплота испарения – это теплота, необходимая для испарения единицы массы жидкости. Удельная теплота получается делением молярной на молярную массу. Обратный процесс – конденсация – сопровождается выделением теплоты. Очевидно, что скрытая теплота конденсации равна скрытой теплоте испарения.
Испарение жидкости является одним из видов фазовых переходов, поэтому скрытая теплота испарения называется еще теплотой фазового перехода. Скрытая теплота испарения количественно характеризует силы связи между молекулами, чем больше эти силы, тем выше теплота испарения.
При критической температуре, когда исчезает различие между жидкостью и паром, скрытая теплота испарения равна, очевидно, нулю, следовательно, с повышением температуры скрытая теплота испарения должна уменьшаться.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 593; Нарушение авторских прав?; Мы поможем в написании вашей работы!