
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фазовое равновесие. Линия равновесия
|
|
|
|
Рассмотрим процесс массопередачи в котором аммиак, представляющий собой распределяемый компонент, поглощается из его смеси с воздухом чистой водой, т.е. ввиду отсутствия равновесия переходит из газовой фазы Фу, где его концентрация у, в жидкую фазу Фу, имеющую начальную концентрацию х = 0. С началом растворения аммиака в воде начнется переход части его молекул в обратном направлении со скоростью, пропорциональной концентрации аммиака в воде и на границе раздела фаз. С течением времени скорость перехода аммиака в воду будет снижаться, а скорость обратного перехода возрастать, причем такой двусторонний переход будет продолжаться до тех пор, пока скорости переноса в обоих направлениях не станут равны друг другу. При равенстве скоростей установится динамическое равновесие, при котором не будет происходить видимого перехода вещества из фазы в фазу.
При равновесии достигается определенная зависимость между предельными, или равновесными концентрациями распределяемого вещества в фазах для данной температуры и давления, при которых осуществляется процесс массопередачи.
В условиях равновесия некоторому значению x отвечает строго определенная равновесная концентрация в другой фазе, которую обозначим через y *
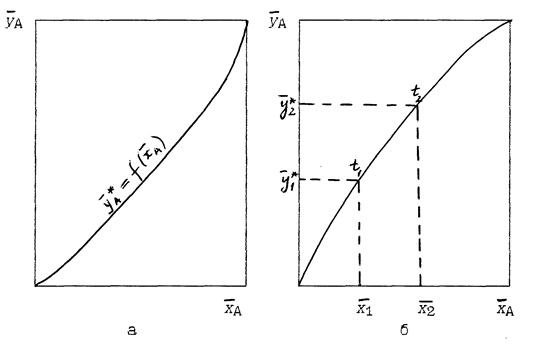
Рис. 1.1. Диаграммы равновесия:
а - при р=сопst и t=сопst
б - при р=сопs
Соответственно концентрации у отвечает равновесная концентрация х*. В общем виде связь между концентрациями распределяемого вещества в фазах при равновесии выражается зависимостью:
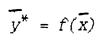
или

Любая из этих зависимостей изображается графически линией равновесия, которая является кривой (рис.2.1) или, в частном случае, прямой линией.
Отношение концентраций фаз при равновесии называется коэффициентом равновесия:
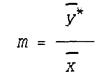
Значение т выражает тангенс угла наклона линии равновесия и является величиной переменной.
Зная линию равновесия для конкретного процесса, и рабочие, т.е. неравновесные концентрации фаз в соответствующих точках, можно определить направление и движущую силу массопередачи в любой точке аппарата. На основе этих данных может быть рассчитана средняя движущая сила, а по ней и скорость процесса массопередачи.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2431; Нарушение авторских прав?; Мы поможем в написании вашей работы!