
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Правило фаз. Знание равновесия в процессах массопередачи позволяет установить пределы, до которых могут протекать эти процессы
|
|
|
|
Знание равновесия в процессах массопередачи позволяет установить пределы, до которых могут протекать эти процессы. Что такое равновесная система?
Замкнутая система, состоящая из одной, двух и более фаз, называется равновесной, если на протяжении неограниченного времени в ней не происходит никаких качественных и количественных изменений.
Из этого определения следует, что необходимым условием фазового равновесия является постоянство температуры и давления во всех фазах этой системы. При неравенстве температуры равновесие будет нарушаться из-за теплообмена, а при неравенстве давления - из-за массообмена между фазами.
В основе равновесия лежит известное правило фаз:
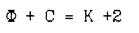
или
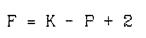
где: С(F) - число степеней свободы системы;
К - число компонентов системы;
Ф(Р) - число фаз.
Правило фаз указывает, какое число параметров можно изменять без нарушения равновесия системы. Так, например, в случае однокомпонентной трехфазной системы (лед - вода - водяной пар) К = 1 и Ф = 3, поэтому:

т.е. система не имеет степеней свободы, она инвариантна; ее существование возможно только при давлении 0,5 кПа и температуре 0,0076°С.
Если удалить из системы лед, то оставшаяся двухфазная система (К=1, Ф=2) будет иметь одну степень свободы (С = 1), она моновариантна, т.е. допускает без нарушения равновесия изменять либо температуру, либо давление.
Рассмотрим систему, состоящую из двухкомпонентной (бинарной) жидкой смеси и паров, образующихся при ее кипении. В данном случае характеристическими параметрами системы, кроме температуры и давления, являются еще составы жидкости и пара.
Если компоненты жидкой смеси абсолютно нерастворимы друг в друге, то: К = 2, Ф = 3, С = 1, т.е. система моновариантна. Изменение давления над этой системой влечет за собой изменение температуры кипения и состава паровой фазы.
Если рассматриваемая смесь состоит из компонентов с неограниченной взаимной растворимостью, то К = 2, Ф = 2, С = 2, т.е. система бивариантна. В такой системе определенному давлению и заданному составу жидкой фазы всегда соответствует определенная температура кипения и определенный состав паровой фазы.
При кипении смеси состоящей из 3 компонентов с неограниченной взаимной растворимостью, мы имеем систему с 3 степенями свободы (К=3, Ф=2, С=3). То есть кроме температуры и давления может быть еще произвольно задана концентрация одного компонента в жидкой фазе или парах; остальные параметры равновесной системы однозначны.
Правило фаз, как показывают примеры, дает лишь качественную характеристику равновесной системы. Необходимые же для изучения и теоретического расчета процессов массообмена количественные соотношения компонентов сосуществующих фаз (их составы) в равновесных системах большей частью не поддаются теоретическому расчету, а определяются экспериментальным путем. Для распространенных на практике систем количественные данные о равновесных составах фаз приведены в справочниках. По этим данным строят в требуемых системах координат диаграммы равновесия
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 357; Нарушение авторских прав?; Мы поможем в написании вашей работы!