
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Объединенное уравнение первого и второго законов термодинамики с учетом полезной работы
|
|
|
|
Лекция 4. Третий закон термодинамики
Вопросы для самопроверки
1. Рассмотрите классификацию термодинамических процессов. Какие процессы называются положительными, отрицательными и равновесными?
2. Поясните схемы циклического процесса в простейшей тепловой машине.
3. Какие формулировки второго закона термодинамике вам известны.
4. Что обозначает постулат «вечный двигатель второго рода» невозможен.
5. Сформулируйте второй постулат Клаузиуса. Поясните физический смысл теплоемкости и энтропии.
6. Рассмотрите принцип расчета ∆S в различных равновесных процессах.
7. Как рассчитать ∆S фазовых превращений веществ, процессов изотермического сжатия – расширения идеального газа, процессов смешения идеальных газов?
8. В каком случае изменение энтропии является критерием самопроизвольности процесса?
9. Как изменяется энтропия вещества при его нагревании и охлаждении?
10. Поясните, почему энтропия является функцией состояния. Что значит энтропия – экстенсивное свойство системы?
4.1 Объединенное уравнение первого и второго законов термодинамики с учетом полезной работы
4.2 Тепловая теорема Нернста, постулат Планка. Абсолютное значение энтропии
4.3 Статистический характер второго закона термодинамики. Энтропия и термодинамическая вероятность
Известно что, математическое выражение первого закона термодинамики для макро- и микропроцессов имеет следующий вид:
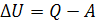 ; (4.1)
; (4.1)
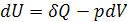 . (4.2)
. (4.2)
С учетом полезной работы последнее выражение можно представить так:
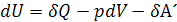 , (4.3)
, (4.3)
поскольку для обратимого термодинамического процесса
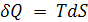 ,
,
то 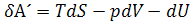
В результате получается объединенное уравнение первого и второго законов термодинамики с учетом полезной работы 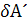 .
.
|
|
|
Проведем анализ объединенного уравнения первого и второго законов для двух наиболее характерных типов термодинамических процессов.
Для изохорно-изотермического процесса:
а) 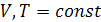 ,
,
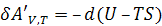 . (4.4)
. (4.4)
Обозначим 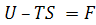 .
.
Тогда 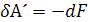 , (4.5)
, (4.5)
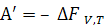 . (4.6)
. (4.6)
Для изобарно-изотермического процесса:
б) 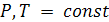 ,
,
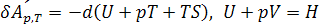 (4.7)
(4.7)
Обозначим  ,
,
тогда 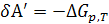 (4.8)
(4.8)
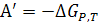 (4.9)
(4.9)
Таким образом, полезная работа изохорно-изотермического процесса равна убыли свободной энергии Гельмгольца 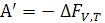 , полезная работа изобарно-изотермического процесса равна убыли свободной энергии Гиббса
, полезная работа изобарно-изотермического процесса равна убыли свободной энергии Гиббса 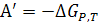 .
.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2625; Нарушение авторских прав?; Мы поможем в написании вашей работы!