
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Свободная энергия Гельмгольца, энергия Гиббса
|
|
|
|
Лекция 5. Энергия Гельмгольца, энергия Гиббса
5.1 Свободная энергия Гельмгольца, энергия Гиббса
5.2 Фундаментальное уравнение Гиббса и вспомогательные термодинамические функции
5.3 Изменение энергии Гиббса с температурой и давлением
Из цикла Карно известно, что η < 1 (т.е. в работу превращается не вся теплота). Поэтому даже в равновесном термодинамическом процессе всё изменение внутренней энергии нельзя превратить в работу.
Изучая природу внутренней энергии Гельмгольц пришел к выводу, что она неоднородна и состоит из двух частей:
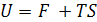 , (5.1)
, (5.1)
где F –«свободная» энергия, способная к превращениям и производству полезной работы, функция (энергия) Гельмгольца, изохорно-изотермический потенциал (V и T = const), изохорный потенциал TS –«связанная» энергия, которая в работу не превращается и теряется в виде теплоты в окружающую среду. Функцию F Гельмгольц ввел в практику в 1882 году.
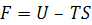 (5.2)
(5.2)
Так как  ,
,
то 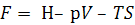 , (5.3)
, (5.3)
Значит 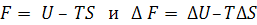 (5.4)
(5.4)
где ∆ F − изменение энергии Гельмгольца.
При V=const и T=const в стандартных условиях последняя формула может быть представлена в виде:
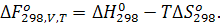
Энергия Гельмгольца, также как внутренняя энергия и энтропия – функция состояния системы.
Критерием самопроизвольности изохорно-изотермического процесса являются неравенства ∆FV,T < 0, 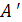 > 0. При ∆ FV,T > 0 и
> 0. При ∆ FV,T > 0 и 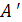 < 0 имеет место обратный процесс, в состоянии химического равновесия ∆ FV,T = 0,
< 0 имеет место обратный процесс, в состоянии химического равновесия ∆ FV,T = 0, 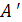 = 0 (
= 0 (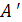 - максимальная полезная работа).
- максимальная полезная работа).
Однако чаще в термодинамике приходится иметь дело с изобарно-изотермическими процессами (Р и T = const), поэтому удобнее пользоваться функцией (энергией) Гиббса.
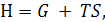 (5.5)
(5.5)
 , (5.6)
, (5.6)
где GР,Т – функция Гиббса, свободная энтальпия, изобарно-изотермический потенциал, изобарный потенциал.
Энергия Гиббса – наиболее важная и часто употребляемая на практике термодинамическая функция. Введена в термодинамику Гиббсом в 1875 году.
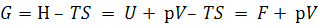 (5.7)
(5.7)
G определяется через известные термодинамические функции.
При р,Т= const:
 , (5.8)
, (5.8)
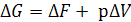 (5.9)
(5.9)
В стандартных условиях изменение энергии Гиббса может быть представлено следующим образом:
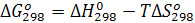 (5.10)
(5.10)
Критерием самопроизвольности прямого изобарно-изотермического процесса являются неравенства ∆GР,Т < 0 и A′ > 0; при ∆ GР,Т > 0 и A′ < 0 протекает обратный процесс, в состоянии химического равновесия ∆ GР,Т = 0 и A′ = 0.
Энергия Гельмгольца и энергия Гиббса – функции состояния, поэтому ∆F и ∆G не зависят от пути и от характера протекания процесса, а определяются только начальным и конечным состоянием системы:
 , (5.11)
, (5.11)
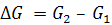 . (5.12)
. (5.12)
Для кругового процесса их изменение = 0:
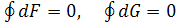 (5.13)
(5.13)
Абсолютные значения F и G определить невозможно (т.к. они зависят от U и Н), обычно определяют величины их изменения ∆F и ∆G (кДж/моль или ккал/моль) путем измерения работы равновесного процесса. Протеканию прямого процесса в термодинамической системе способствуют: ∆Н < 0 и∆S>0, ∆G = ∆Н – T∆S, что приводит к уменьшению ∆G в выражении:
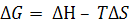 .
.
|
|
|
Дата добавления: 2014-01-07; Просмотров: 3907; Нарушение авторских прав?; Мы поможем в написании вашей работы!