
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Уравнение Клапейрона–Менделеева
|
|
|
|
Между параметрами состояния идеального газа существует связь, называемая уравнением состояния. Французский инженер Б. Клапейрон (1799–1864) обобщил экспериментальные газовые законы и установил связь между параметрами (уравнение Клапейрона):
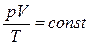 .
.
Русский ученый Д.И. Менделеев (1834–1907) объединил уравнение Клапейрона с законом Авогадро. Согласно закону Авогадро, при одинаковых 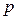 и
и 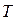 моль любого газа занимает одинаковый молярный объем
моль любого газа занимает одинаковый молярный объем 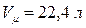 , поэтому Менделеев сделал вывод, что постоянная в правой части равенства будет одинакова для всех газов. Эта общая для всех газов постоянная обозначается
, поэтому Менделеев сделал вывод, что постоянная в правой части равенства будет одинакова для всех газов. Эта общая для всех газов постоянная обозначается 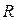 и называется универсальной газовой постоянной.
и называется универсальной газовой постоянной.
Числовое значение 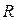 можно определить, подставив в формулу
можно определить, подставив в формулу 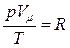 значения параметров при НУ. Согласно расчетам,
значения параметров при НУ. Согласно расчетам, 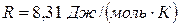 .
.
Перейдем к произвольной массе газа 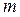 . При тех же условиях она будет занимать объем
. При тех же условиях она будет занимать объем 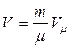 . Тогда
. Тогда
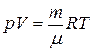 . (7.4.1)
. (7.4.1)
Это уравнение является уравнением состояния идеального газа (уравнением Клапейрона – Менделеева).
Введем постоянную 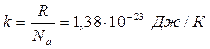 , называемую постоянной Больцмана. Тогда
, называемую постоянной Больцмана. Тогда
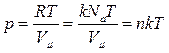 , (7.4.2)
, (7.4.2)
где  концентрация молекул. Следовательно, из 7.4.2 следует, что давление идеального газа при данной температуре прямо пропорционально концентрации его молекул, а плотность
концентрация молекул. Следовательно, из 7.4.2 следует, что давление идеального газа при данной температуре прямо пропорционально концентрации его молекул, а плотность 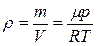 обратно пропорциональна температуре.
обратно пропорциональна температуре.
В системе СИ давление измеряется в Паскалях 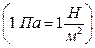 . Кроме того, для измерения давления используется ряд величин:
. Кроме того, для измерения давления используется ряд величин:
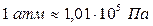 ,
, 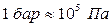 ,
, 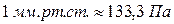 .
.
Число молекул, содержащихся в 1 м3 газа при нормальных условиях, называется числом Лошмидта: 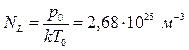 .
.
 Пример 7.4.1. В баллоне объемом
Пример 7.4.1. В баллоне объемом 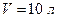 находится гелий под давлением
находится гелий под давлением 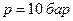 и при температуре
и при температуре 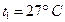 . После того, как из баллона было взято
. После того, как из баллона было взято 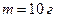 гелия, температура в баллоне понизилась до
гелия, температура в баллоне понизилась до 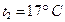 . Определить давление газа, оставшегося в баллоне.
. Определить давление газа, оставшегося в баллоне.
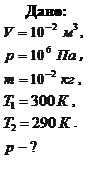
 Решение:
Решение:
 Для начального состояния уравнение Менделеева – Клапейрона имеет вид:
Для начального состояния уравнение Менделеева – Клапейрона имеет вид: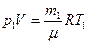 . Поскольку объем гелия в конечном состоянии будет таким же (ограничен объемом сосуда), то для конечного состояния
. Поскольку объем гелия в конечном состоянии будет таким же (ограничен объемом сосуда), то для конечного состояния 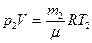 . Из этих уравнений найдем массы:
. Из этих уравнений найдем массы: 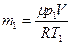 и
и 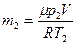 .
.
Учитывая, что 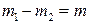 , получим
, получим 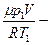
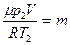 .
.
Выразим искомое давление: 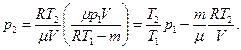
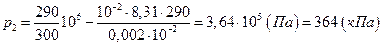 .
.
Ответ: 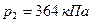 .
.
Пример 7.4.2. Найти молярную массу воздуха, считая, что он состоит (по массе) из одной части кислорода и трех частей азота.

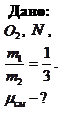 Решение:
Решение:
 Свойствами идеального газа могут обладать не только химически однородные газы, но и газовые смеси. Чтобы применить уравнение состояния для газовой смеси, ей необходимо приписать некоторую, хотя и лишенную химического смысла, молярную массу
Свойствами идеального газа могут обладать не только химически однородные газы, но и газовые смеси. Чтобы применить уравнение состояния для газовой смеси, ей необходимо приписать некоторую, хотя и лишенную химического смысла, молярную массу 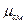 . Величину
. Величину 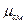 выбирают такой, чтобы она удовлетворяла уравнению состояния идеального газа, записанному для смеси:
выбирают такой, чтобы она удовлетворяла уравнению состояния идеального газа, записанному для смеси: 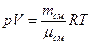 . Откуда давление смеси
. Откуда давление смеси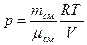 .
.
Запишем уравнение Клапейрона – Менделеева для каждой из компонент смеси: 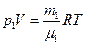 и
и 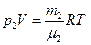 . Выразим парциальные давления газов, входящих в смесь:
. Выразим парциальные давления газов, входящих в смесь: 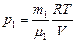 и
и 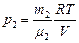 . По закону Дальтона давление смеси газов равно сумме
. По закону Дальтона давление смеси газов равно сумме
их парциальных давлений: 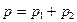 . Следовательно,
. Следовательно, 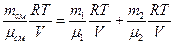 .
.
Учитывая, что масса смеси 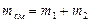 , получим
, получим 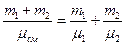 .
.
Искомая молярная масса смеси равна
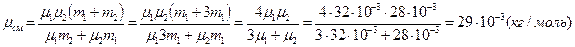 .
.
Ответ: 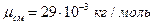 .
.
Пример 7.4.3. Плотность смеси азота и водорода при температуре 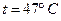 и давлении
и давлении 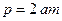 равна
равна 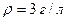 . Найти концентрацию молекул азота и водорода в смеси.
. Найти концентрацию молекул азота и водорода в смеси.
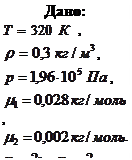
 Решение:
Решение:
 Запишем уравнение состояния идеального газа для смеси газов:
Запишем уравнение состояния идеального газа для смеси газов: 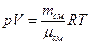 . Учтем, что молярная масса смеси
. Учтем, что молярная масса смеси  (см. пример 7.4.2), поскольку
(см. пример 7.4.2), поскольку 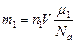 и
и 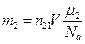 , то
, то 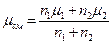 .
.
Подставим значения молярной массы смеси в уравнение Клапейрона – Менделеева.
Тогда 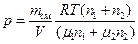 или
или 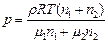 (1), где
(1), где 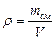 – плотность смеси.
– плотность смеси.
С другой стороны, давление смеси газов равно 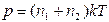 (2). Решая совместно (1) и (2), найдем
(2). Решая совместно (1) и (2), найдем 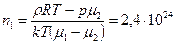 (м-3) и
(м-3) и 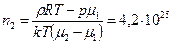 (м-3).
(м-3).
 Ответ:
Ответ: 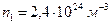 ,
, 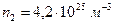 .
.
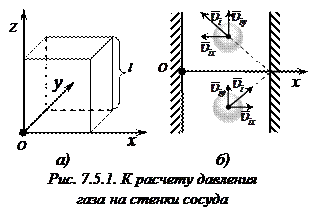 7.5. Основное уравнение молекулярно-кинетической теории идеальных газов
7.5. Основное уравнение молекулярно-кинетической теории идеальных газов
Применим статистический метод для расчета давления газа на стенки сосуда, в котором он находится. Давление газа на любую стенку равно отношению силы, с которой молекулы газа действуют на эту стенку, к площади ее поверхности:
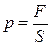 . (7.5.1)
. (7.5.1)
Пусть газ находится в сосуде кубической формы с ребром 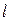 (рис. 7.5.1, а). Рассмотрим стенку, перпендикулярную оси Ox (рис. 7.5.1, б). Найдем силу, с которой на нее будет действовать одна молекула газа. Обозначим
(рис. 7.5.1, а). Рассмотрим стенку, перпендикулярную оси Ox (рис. 7.5.1, б). Найдем силу, с которой на нее будет действовать одна молекула газа. Обозначим 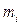 массу одной молекулы,
массу одной молекулы, 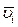 скорость молекулы. Молекулы газа могут менять направление скорости только при ударе о стенки (считаем, что взаимные столкновения к этому не приводят). Изменение импульса молекулы при ударе равно
скорость молекулы. Молекулы газа могут менять направление скорости только при ударе о стенки (считаем, что взаимные столкновения к этому не приводят). Изменение импульса молекулы при ударе равно 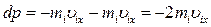 . С другой стороны, изменение импульса молекулы равно импульсу силы, действующей на нее со стороны стенки. Обозначим силу, действующую на стенку сосуда со стороны молекулы
. С другой стороны, изменение импульса молекулы равно импульсу силы, действующей на нее со стороны стенки. Обозначим силу, действующую на стенку сосуда со стороны молекулы 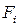 . Тогда по третьему закону Ньютона сила, с которой стенка будет действовать на молекулу, равна
. Тогда по третьему закону Ньютона сила, с которой стенка будет действовать на молекулу, равна 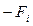 . Следовательно,
. Следовательно, 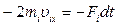 , где
, где 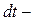
время взаимодействия молекулы со стенкой. Таким образом, сила, с которой молекула будет действовать на стенку сосуда при ударе, равна 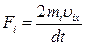 .
.
Время взаимодействия молекулы со стенкой неизвестно. Поэтому заменим кратковременно действующую ударную силу 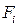 эквивалентной ей средней силой
эквивалентной ей средней силой 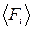 так, чтобы импульс средней силы за время
так, чтобы импульс средней силы за время 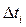 между двумя последовательными ударами молекулы об одну и ту же стенку равнялся импульсу ударной силы:
между двумя последовательными ударами молекулы об одну и ту же стенку равнялся импульсу ударной силы:
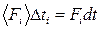 . Учитывая, что
. Учитывая, что 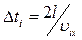 (молекула возвращается, предварительно
(молекула возвращается, предварительно
отразившись от противоположной стенки), выразим 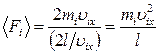 . В любой
. В любой
момент времени вдоль каждой координатной оси вследствие хаотичности движения перемещается 1/3 всех молекул. Средняя сила, действующая на стенку со стороны молекул газа, находящихся в сосуде, 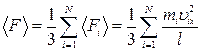 .
.
Давление, производимое газом на эту стенку:
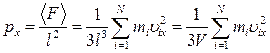 ,
,
где 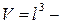 объем сосуда.
объем сосуда.
Так как давление газа на все стенки сосуда одинаково (закон Паскаля), то
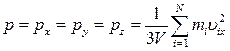 . С учетом того, что
. С учетом того, что 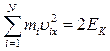 , (
, (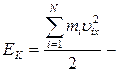 суммарная кинетическая энергия молекул газа),
суммарная кинетическая энергия молекул газа),
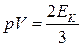 . (7.5.2)
. (7.5.2)
Это уравнение называется основным уравнением МКТ: произведение давления идеального газа на его объем равно двум третьим величины кинетической энергии поступательного движения всех его молекул.
Глава 8. Статистические распределения
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 3633; Нарушение авторских прав?; Мы поможем в написании вашей работы!