
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Концентрационные гальванические элементы
|
|
|
|
Особенностью концентрационного гальванического элемента, рис.4, является то, что оба электрода выполнены из одного и того же метала.
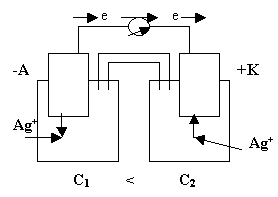
Рис.4
Эти электроды отличаются друг от друга только концентрациями солевых растворов.
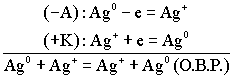
(По формуле Нерста) рассчитаем ЭДС концентрационного элемента.
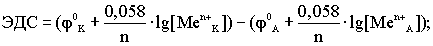
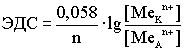
Недостатки концентрационных гальванических элементов:
· разрушаемый анод,
· малая ЭДС.
Концентрационные элементы используются в тех случаях, где необходима малая ЭДС.
Окислительно - восстановительные (ОВ) гальванические элементы
Особенностью данных элементов является то, что окислительно - восстановительный процесс протекает только в растворах. Оба электрода являются инертными, или пассивными, т.е. сами они не принимают участия в ОВ процессах, а выполняют роль проводников электронов.
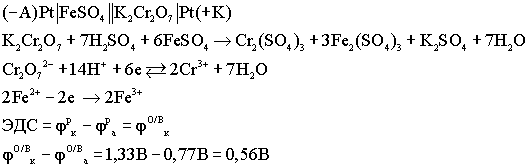
Топливные элементы(ТЭ)
Электрохимические реакции очень медленные. Для ускорения процессов
советский инженер Давтян предложил ввести в окислительно - восстановительные гальванические элементы катализаторы.
Суть топливных элементов заключается в том, что электроды являются одновременно и катализаторами. Топливо, т.е. восстановитель и окислитель, хранится вне гальванических элементов и подаётся на электроды по мере необходимости, рис.5.
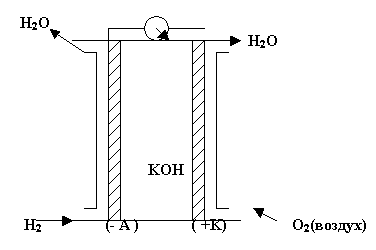
Рис.5
Электроды выполняются из пористого Ni или пористой Pt, то есть тех металлов, которые являются катализаторами электродных процессов. В качестве электролита используется раствор гидроксида калия.
Схема кислородно- водородного ТЭ может быть записана в виде:
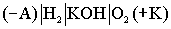 .
.
На аноде элемента протекает реакция окисления водорода:
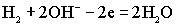 .
.
На катоде восстанавливается кислород:
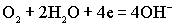 .
.
Суммированием анодной и катодной реакций получаем уравнение токообразующей реакции:
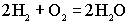 ,
,
в результате которой химическая энергия непосредственно превращается в электрическую.
Пример применения топливных элементов - использование их в мобильниках фирмы Toshiba.
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 693; Нарушение авторских прав?; Мы поможем в написании вашей работы!