
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Селективные ингибиторы ЦОГ-2 диарилсульфоны
|
|
|
|
 Целекоксиб (Celecoxib, Celebrex) Целекоксиб был создан в 90-е годы XX века и дал начало целому классу высокоспецифических ингибиторов ЦОГ-2 – «коксибов».
Целекоксиб (Celecoxib, Celebrex) Целекоксиб был создан в 90-е годы XX века и дал начало целому классу высокоспецифических ингибиторов ЦОГ-2 – «коксибов».
МД: Целекоксиб в 375 раз избирательнее блокирует ЦОГ-2, по сравнению с ЦОГ-1 изоформой фермента. Полагают, что это связано с наличием в молекуле целекоксиба 2 участков, жестко фиксированных под углом: полярная сульфонанилидная группа молекулы блокирует гидрофильный боковой карман ЦОГ-2, а арилпиразольная часть молекулы при этом занимает основной гидрофобный канал фермента. В связи с тем, что молекула ЦОГ-1 не имеет гидрофильного бокового кармана целекоксиб не способен плотно войти в активный центр фермента и связь лекарства с ЦОГ-1 достаточно непрочная. Она реализуется только при приеме высоких доз целекоксиба (блокада ЦОГ-2 развивается уже при назначении целекоксиба в дозе 0,2 мг/кг или 150-200 мг/сут, тогда как для блокады ЦОГ-1 требуется доза 200 мг/кг или около 14000 мг/сут).
Таблица 7. Сравнительная характеристика НПВС
| Лекарство | Антипиретический | Противовоспалительный | Анальгетический | Эффект. | ЦОГ-1† ЦОГ-2 |
| Аспирин (АСК) | ËË | ËË | ËË | 1,00 | |
| Дифлунизал | ▬ | ËË | ËËË | 1,40 | |
| Парацетамол | ËË | ▬ | ËË | 1,00 | |
| Фенилбутазон | Ë | ËËËË | ËË | 3,00 | |
| Ибупрофен | ËË | Ë | ËË | 3,25 | 5,0-10,0 |
| Напроксен | ËË | ËËË | ËËË | 2,60 | 10,0-18,5 |
| Индометацин | ËË | ËËËË | ËËË | 1,30 | 22,3-33,0 |
| Сулиндак | Ë | ËË | ËË | 30,9 | |
| Диклофенак | ËËË | ËËË | ËËË | 1,0 | 2,2 |
| Пироксикам | ËËË | ËËË | ËË | 12,5-33,0 | |
| Теноксикам | ËË | ËËË | ËË | 15,0 | |
| Кеторолак | Ë | ËË | ËËËË | 30,00* | |
| Мефенам. к-та | ËËË | Ë/▬ | ËË | 0,75 | |
| Набуметон | Ë | ËËË | ËË | 2,00-3,00 | 0,14 |
| Целекоксиб | ▬ | ËËË | Ë | 0,003-0,01 |
Примечание: † – чем меньше отношение ЦОГ-1/ЦОГ-2=-lg[IC50 ЦОГ-1/IC50 ЦОГ-2], тем селективнее средство в отношении ЦОГ-2.
ФК: Целекоксиб обладает очень низкой растворимостью в воде, поэтому создать парентеральную форму лекарства чрезвычайно сложно. При пероральном приеме биодоступность целекоксиба составляет около 75%, прием пищи может снизить скорость абсорбции на 20-30%, но биодоступность при этом становится полнее и возрастает на 7-20%. В крови целекоксиб на 97% связан с белками крови. После однократного приема в дозе 200 мг величина максимальной концентрации в сыворотке крови составляет 1500 нг/мл и в 5 раз превосходит границу минимального терапевтического уровня (300 нг/мл). Поскольку период полуэлиминации лекарства составляет 10-12 ч, снижение концентрации до минимального терапевтического уровня происходит за время чуть более 2t½, т.е. прием целекоксиба можно проводить 1 раз в день.
Метаболизм целекоксиба протекает в печени (>90%) в основном за счет изоформы цитохрома Р4502С9. Данный цитохром не принимает участия в метаболизме подавляющего большинства лекарств (например, аминогликозидов, антиконвульсантов и пероральных сахаропонижающих средств), поэтому при лечении целекоксибом не требуется коррекции дозы лекарств, которые принимаются совместно с ним.
ФЭ: Для целекоксиба характерны выраженный противовоспалительный и анальгетический эффекты. По своей эффективности целекоксиб в дозе 100-400 мг/сут не уступает АСК, напроксену и диклофенаку. Интересно отметить, что противовоспалительный и анальгетический эффекты лекарства не носят дозозависимого характера. При использовании в дозе менее 100 мг/сут эффект лекарства отсутствует, в диапазоне доз от 100 до 400 мг/сут он возникает, но дальнейшее повышение дозы с 400 мг/сут до 1200 мг/сут практически не приводит к усилению эффекта.
Поскольку целекоксиб практически не влияет на ЦОГ-1, он не изменяет агрегацию тромбоцитов и не приводит к развитию дезагрегантного действия.
Показания к применению и режимы дозирования: Целекоксиб применяют для лечения хронических воспалительных поражений органов опорно-двигательного аппарата:
· остеоартроз – по 100-400 мг/сут в 1 прием;
· ревматоидный артрит – по 200-800 мг/сут в 1-2 приема.
Поскольку имеются теоретические предпосылки возможного участия ЦОГ-2 в процессах канцерогенеза в области колоректальной зоны, развитии болезни Альцгеймера, то некоторые авторы рассматривают целекоксиб как перспективное средство для профилактики этих заболеваний у лиц старшей возрастной группы.
НЭ: Вследствие высокой селективности в отношении ЦОГ-2 и сохранении нормального функционирования физиологической изоформы ЦОГ-1 целекоксиб считают более безопасным НПВС, по сравнению с неселективными ингибиторами ЦОГ.
Целекоксиб реже вызывает образование язвенных дефектов на слизистой оболочке ЖКТ, не приводит к развитию кровотечений вследствие снижения агрегации тромбоцитов и не оказывает токолитического действия (не снижает тонус миометрия). У лиц с артериальной гипертензией его прием не сопровождается дестабилизацией давления.
Однако, первоначальные надежды на полную безопасность селективных ингибиторов ЦОГ-2 и самого целекоксиба в целом не оправдались. В настоящее время установлено, что его прием сопровождается возникновением следующих нежелательных эффектов:
· Как уже упоминалось ранее, целекоксиб не вызывает развитие язвенного поражения слизистых ЖКТ, но он задерживает процесс заживления уже существующих язвенных дефектов. Полагают, что это связано с тем, что контроль над процессами репарации и митоза эпителия ЖКТ осуществляют простагландины, которые образуются под влиянием ЦОГ-2.
· Сульфонанилидная группа целекоксиба способна вызывать кожные аллергические реакции и перекрестную сенсибилизацию к сульфаниламидным средствам и пероральным сахаропонижающим лекарствам из группы производных сульфонилмочевины.
· У 1% людей, которые длительно принимали целекоксиб развивалась острая почечная недостаточность.
· Для целекоксиба, также как и для нимесулида в исследовании CLASS (2000 г.) была доказана способность индуцировать развитие тромбозов. Как полагают, это обусловлено тем, что синтез тромбоксана А2 контролируется преимущественно ЦОГ-1, а синтез простациклина – ЦОГ-2. Поэтому, на фоне блокады ЦОГ-2 в организме может возникнуть преобладание уровня тромбоксана над простациклином и агрегация тромбоцитов будет возрастать, вплоть до развития нефатального инфаркта миокарда.
Следует отметить, впрочем, что более поздние исследования, выполнявшиеся в 2002 г, не подтвердили выводов исследования CLASS. Поэтому, вопрос о влиянии целекоксиба на гемостаз остается до настоящего времени открытым.
· Прием целекоксиба у женщин приводит к развитию обратимого бесплодия (частота которого была в 2 раза выше, чем в контрольной популяции женщин, не принимавших ингибиторы ЦОГ-2).
ФВ: капсулы по 100 и 200 мг.
Рофекоксиб (Rofecoxib, Vioxx) Также как и целекоксиб относится к мощным селективным ингибиторам ЦОГ-2. Механизм действия рофекоксиба аналогичен таковому у целекоксиба, но роль блокатора гидрофобного основного канала у него выполняет арилфуранозная часть молекулы.
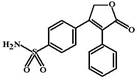 ФК: Рофекоксиб хорошо абсорбируется из ЖКТ, но при повышении дозы его абсорбция падает. Как полагают, это связано с особенностями растворения лекарства. В отличие от целекоксиба он хуже связывается с белком (»87%), но тем не менее его период полуэлиминации больше, чем у целекоксиба и составляет около 17 часов (поэтому рофекоксиб можно назначать 1 раз в сутки). Метаболизм рофекоксиба протекает при участии изоформы цитохрома Р4503А4, которая активно окисляет лекарство как в печени, так и в стенке кишечника.
ФК: Рофекоксиб хорошо абсорбируется из ЖКТ, но при повышении дозы его абсорбция падает. Как полагают, это связано с особенностями растворения лекарства. В отличие от целекоксиба он хуже связывается с белком (»87%), но тем не менее его период полуэлиминации больше, чем у целекоксиба и составляет около 17 часов (поэтому рофекоксиб можно назначать 1 раз в сутки). Метаболизм рофекоксиба протекает при участии изоформы цитохрома Р4503А4, которая активно окисляет лекарство как в печени, так и в стенке кишечника.
ФЭ: Рофекоксиб обладает хорошо выраженным анальгетическим, противовоспалительным и антипиретическим эффектами. При этом, подобно другим селективным ингибиторам ЦОГ-2 он лишен антиагрегантной активности.
Применение и дозирование: Рофекоксиб используют для лечения остеоартроза и ревматоидного артрита в дозе 25 мг/сут однократно.
НЭ: В целом нежелательные эффекты рофекоксиба аналогичны эффектам целекоксиба.
ФВ: таблетки по 12,5 и 25 мг.
Средства, влияющие преимущественно на липоксигеназный путь
метаболизма эйкозаноидов.
Классификация:
I. Ингибиторы 5-липоксигеназы: зилеутон;
II. Антагонисты лейкотриеновых cysLT1-рецепторов: зафирлукаст, монтелукаст, верлукаст, пранлукаст, циналукаст, иралукаст, побилукаст.
Зилеутон (Zileuton, Zyflo) Зилеутон был первым лекарственным средством, которое оказывало влияние на функционирование липоксигеназного пути метаболизма эйкозаноидов.
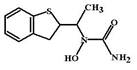 МД: В воспаленной ткани часть арахидоновой кислоты, которая образовалась из фосфолипидов мембран клетки, метаболизируется по липоксигеназному пути. При этом фермент 5-ЛОГ окисляет арахидоновую кислоту вначале до 5-гидропероксиэйкозатетраеновой кислоты, а затем гидролизует этот продукт до лейкотриена А4 (см. схему 3).
МД: В воспаленной ткани часть арахидоновой кислоты, которая образовалась из фосфолипидов мембран клетки, метаболизируется по липоксигеназному пути. При этом фермент 5-ЛОГ окисляет арахидоновую кислоту вначале до 5-гидропероксиэйкозатетраеновой кислоты, а затем гидролизует этот продукт до лейкотриена А4 (см. схему 3).
Дальнейший метаболизм LTA4 может протекать по 2 альтернативным путям, выбор каждого из которых зависит от вида клетки, где протекает химическая реакция.
В нейтрофилах и моноцитах при участии кислорода и фермента гидролазы образуется LTB4. В эозинофилах, базофилах и тучных клетках LTA4 подвергается конъюгации с SH-глутатионом до LTC4, который в дальнейшем расщепляется до LTD4 и LTE4. Наиболее интенсивно процессы синтеза лейкотриенов протекают в воспаленных тканях бронхиального дерева. Так, у лиц с бронхиальной астмой они в 5-10 раз интенсивнее, чем у здоровых людей.
В тканях-мишенях лейкотриены воздействуют на специальные мембранные рецепторы и вызывают возникновение ответных реакций (см. таблицу 8.):
Таблица 8. Эффекты лейкотриенов и типы лейкотриеновых рецепторов.
| Лейкотриен | Ткань-мишень | Рецептор: эффект |
| LTC4, LTD4, LTE4 | мышцы бронхов | cysLT1: сокращение бронхов, пролиферация клеток |
| железы бронхов | cysLT1: гиперсекреция слизи | |
| сосуды | cysLT1: усиление проницаемости и отек cysLT2: “, затем ” АД, коронарного кровотока | |
| эозинофилы | cysLT1: хемотаксис в очаг воспаления | |
| n. vagus | cysLT1: выделение Ach и развитие бронхоспазма | |
| LTB4 | нейтрофилы | LT: хемотаксис в очаг воспаления |
Таким образом, лейкотриены способствуют развитию бронхоспазма и приступа бронхиальной астмы. По силе бронхоспастического эффекта они в 1000 раз превосходят гистамин (эталонное средство для моделирования астмы у животных)[20].
Зилеутон обратимо связывается с активным центром 5-ЛОГ и блокирует синтез всех лейкотриенов.
ФЭ: Оказывает противоастматическое действие. Прием зилеутона снижает синтез лейкотриенов и в результате вероятность развития бронхоспазма, отека слизистой оболочки бронхов уменьшается.
Применение и дозирование: Зилеутон применяют для профилактики приступов бронхиальной астмы (особенно «аспириновой» формы астмы, которая спровоцирована приемом НПВС, ингибирующих ЦОГ-зависимые пути метаболизма арахидоновой кислоты, и компенсаторно повышающих ее ЛОГ-зависимый метаболизм). Для купирования уже развившегося приступа астмы зилеутон не используется, поскольку при этом синтез лейкотриенов уже завершился, они успели активировать рецепторы и запустить сокращение клетки. Таким образом, зилеутон – средство базисной (длительной) плановой терапии астмы.
По эффективности противоастматического действия зилеутон уступает глюкокортикостероидным средствам и b2-адреномиметикам. Применение зилеутона обычно рекомендуют при следующих ситуациях:
· При бронхиальной астме легкого персистирующего течения зилеутон применяют для монотерапии, как единственное базисное средство.
· При бронхиальной астме средней степени тяжести его используют в дополнение к базисной терапии глюкокортикостероидами, как альтернативу b2-адреномиметикам длительного действия (т.е. комбинацию «ГКС+b2-АМ» можно заменить на «ГКС+Зилеутон»). Использование зилеутона позволяет иногда понизить на 20% суточную дозу принимаемых стероидов.
Как правило, зилеутон принимают по 600 мг 4 раза в день.
НЭ: наиболее значимым нежелательным эффектом зилеутона является его гепатотоксичность, которая в значительной степени ограничивает применение препарата.
ФВ: таблетки по 600 мг.
Зафирлукаст (Zafirlukast, Accolate) МД: Зафирлукаст связывается с цистеиниловым cysLT1-типом лейкотриеновых рецепторов и блокирует их. При этом лейкотриены С4, D4 и Е4 не способны активировать эти рецепторы и вызывать соответствующие эффекты со стороны гладких мышц бронхов.
ФЭ: Зафирлукаст предупреждает развитие приступа бронхиальной астмы, уменьшает отек слизистой оболочки бронхов. К сожалению, уже развившийся приступ астмы зафирлукаст не способен устранить, т.к. после активации лейкотриеновых рецепторов процесс сокращения бронхов запускается при помощи внутриклеточных посредников независимо от того, остается ли рецептор связан с лейкотроиеном или же он вытесняется лекарством.
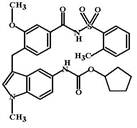 У зафирлукаста обнаружено слабое противовоспалительное действие – он угнетает синтез провоспалительных цитокинов: IL-4,5 и GM-CSF (см. таблицу 2.) и поэтому подавляет процессы хронического воспаления, которые имеют место в бронхиальном дереве при астме.
У зафирлукаста обнаружено слабое противовоспалительное действие – он угнетает синтез провоспалительных цитокинов: IL-4,5 и GM-CSF (см. таблицу 2.) и поэтому подавляет процессы хронического воспаления, которые имеют место в бронхиальном дереве при астме.
По эффективности прием зафирлукаста сопоставим с приемом ингаляционных стероидов в дозе 400-500 мкг/сут (в беклометазоновом эквиваленте). Поэтому, если ранее пациент принимал кортикостероиды в дозе до 400 мкг/сут при переходе на зафирлукаст их можно отменить, а если суточная доза стероидов была выше 400 мкг/сут, то ее можно понизить на 200-400 мкг/сут.
ФК: Зафирлукаст хорошо всасывается при приеме внутрь. Совместный прием с пищей на 40% снижает биодоступность зафирлукаста. Метаболизм лекарства протекает в печени при участии цитохрома Р4502С9. Образующиеся в процессе метаболизма гидроксилированные производные в 90 раз менее активны, чем сам зафирлукаст. Выведение зафирлукаста на 90% осуществляется с желчью. Следует помнить, что прием зафирлукаста сопровождается угнетением функции цитохромов Р450 (причем, не только изоформы 2С9, но и 3А4, которая принимает участие в метаболизме подавляющего большинства лекарств).
Применение: Зафирлукаст принимают как правило натощак внутрь по 20 мг 2 раза в день, при необходимости дозу можно увеличить до 40 мг 2 раза в день.
Зафирлукаст используют для профилактики приступов астмы у взрослых и детей старше 12 лет. При легком течении астмы зафирлукаст используют в виде монотерапии, а при среднетя-
желом течении обычно в дополнение к ингаляционным стероидам[21]. Следует помнить, что прием зафирлукаста не способен купировать уже начавшийся приступ астмы.
НЭ: Зафирлукаст малотоксичное средство. Основным его нежелательным эффектом (хотя и достаточно редким) является возможность развития синдрома Churg-Strauss. Данный синдром представляет собой вариант системного эозинофильного васкулита – заболевания при котором развивается аутоиммуноое воспаление сосудов малого круга кровообращения и возникают следующие симптомы: усиление приступов астмы, появление в тканях легкого облаковидных инфильтратов из эозинофилов, которые на рентгенограммах напоминают картину пневмонии, эозинофилия в периферической крови.
В последние годы было установлено, что наибольший риск развития данного синдрома у пациентов, которые до начала терапии зафирлукастом принимали глюкокортикостероиды в высоких дозах, а после назначения зафирлукаста внезапно прекратили их прием. Основой терапии синдрома Churg-Strauss является применение высоких доз глюкокортикостероидов системно (внутрь или внутривенно).
Крайне редко, прием зафирлукаста (особенно в дозах более 80 мг/сут) может приводить к развитию гепатотоксического действия и сопровождаться резким повышением уровня трансаминаз в периферической крови.
ФВ: таблетки по 0,02 и 0,04.
Монтелукаст (Montelukast, Singulair) Монтелукаст по своему механизму действия и основным фармакологическим эффектам напоминает зафирлукаст, но обладает рядом положительных особенностей:
·  Биодоступность монтелукаста не зависит от приема пищи.
Биодоступность монтелукаста не зависит от приема пищи.
· Метаболизм монтелукаста подобно зафирлукасту протекает в печени, но при этом он не угнетает функции ни одной из изоформ цитохромов Р450 и его можно применять совместно с другими лекарственными средствами, без существенной коррекции дозы этих лекарств.
· Монтелукаст малотоксичен и может применяться у детей с 2 лет.
· Действие монтелукаста сохраняется 24 часа и его можно применять 1 раз в сутки. Обычная доза у взрослых 10 мг 1 раз в сутки, у детей 6-14 лет 5 мг/сут, у детей 2-5 лет – 4 мг/сут.
ФВ: таблетки в оболочке по 10 мг, таблетки жевательные по 5 и 4 мг.
Лекарственные средства с активностью простагландинов.
Использование в медицинской практике простагландинов естественного происхождения не всегда возможно. Это связано с тем, что период их существования в организме исчисляется минутами (обычно не более 10-15 мин), после чего они разрушаются и необратимо утрачивают свою активность.
В таблице 9 суммированы сведения об основных лекарственных средствах с активностью простагландинов и их синтетических аналогах.
Таблица 9. Средства на основе простагландинов и их синтетических аналогов.
| Средство | Вид | Краткая характеристика |
| Dinoprostone | PgE2 | ФЭ: Влияет на ЕР-рецепторы в матке и усиливает ее ритмические сокращения. Действие проявляется вне зависимости от срока беременности и ее наличия. Активирует коллагеназу шейки матки. Это приводит к разрушению коллагеновой сети в шейке, увеличению содержания в ней гидрофильных гликозаминогликанов и гиалуроновой кислоты. В итоге, шейка матки размягчается. ФК: метаболизм протекает в ткани легких. Период полуэлиминации 2,5-5,0 мин. Показания: Индукция родов: гель вводят интравагинально 500 мкг, затем по 500-1000 мкг каждый час или внутривенная инфузия со скоростью 0,25 мкг/мин (если через 0,5 ч эффект не развивается скорость повышают до 0,5-1,0 мкг/мин). Абортация: суппозитории по 20 мг каждые 3-5 ч интравагинально или внутривенная инфузия с начальной скоростью 2,5 мкг/мин, через 0,5 ч при необходимости повышают до 5-10 мкг/мин. НЭ: разрав матки, приливы, тошнота, рвота, диарея. ФВ: гель 0,5 мг в шприцах по 3,0 г. |
| Dinoprost | PgF2a | ФЭ: Действует аналогично динопростону, но эффект более сильный и резкий. Показания: Применяют по тем же показаниям, что и динопростон Абортация в сроки до 15 недель: 250-1000 мг антраамниально каждые 1-2 часа. После 15 недель беременности: 40 мг однократно. Для индукции родов: внутривенная инфузия со скоростью 5,0-7,5 мкг/мин, увеличивая каждые 10-20 мин на 2,5 мкг/мин (максимальная скорость 25 мкг/мин). НЭ: со стороны ЖКТ – боли в животе, тошнота, рвота, понос; со стороны сердечно-сосудистой системы – тахикардия, колебания АД, бронхоспазм. ФВ: раствор 0,5% в ампулах по 1 мл. |
Alprostadil

| PgE1 | ФЭ: Вызывает расширение сосудов и сокращает гладкие мышцы внутренних органов. При введении в половой член это приводит к повышению кровенаполнения пещеристых тел и сокращению сфинктеров вблизи устьев вен, что способствует возникновению и поддержанию эрекции. Снижает агрегацию и усиливает дезагрегацию тромбоцитов. ФК: Метаболизм протекает в сосудах легких. Период полуэлиминации 0,5-1,0 мин. Показания: Лечение эректильной дисфункции. Вводят интрауретрально по 125-250 мкг однократно (в сутки не более 2 раз). Возможно интракавернозное введение (в ткань пещеристых тел пениса). Лечение облитерирующих заболеваний сосудов нижней конечности (атеросклероз, эндартериит, тромбангиит и др.). Вводят внутривенно по 10-40 мг в виде инфузии в течение 1-3 часов. НЭ: Боль в половом члене, приапизм (возникает у 4% лиц), гематомы при интракавернозном введении, чувство жара в половом члене, колебания АД, аритмии. ФВ: порошок в ампулах по 0,00002; 0,01 и 0,04; пеллеты для пенильной аппликации по 125, 250 и 500 мкг. |
Latanoprost

| Аналог PgF2a | ФЭ: Является пролекарством. Эстеразами передней камеры глаза гидролизуется до фенилпростановой кислоты, которая избирательно активирует FP-рецепторы сосудов склеры, вызывая их расширение. При этом активируется отток внутриглазной жидкости по увеасклеральному тракту (сосудам, которые напрямую соединяют сосудистую оболочку глаза и склеру), минуя традиционный путь через угол передней камеры глаза и Шлемов канал. В итоге, внутриглазное давление понижается. Показания: Для контроля внутриглазного давления при открытоугольной глаукоме. Вводят по 1 капле в глаз вечером. Эффект развивается через 3-4 часа и сохраняется до 24 часов. НЭ: Ощущение инородного тела в глазу, изменение пигментации радужки (потемнение), увеличение глазной щели. ФВ: раствор 0,005% во флаконах по 1 мл. |
Misoprostol
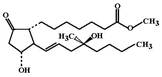
| Аналог PgE1 | ФЭ: Является пролекарством. После приема внутрь, в стенке ЖКТ подвергается биотрансформации в мизопростоловую кислоту, которая избирательно активирует ЕР-простагландиновые рецепторы париетальных и слизистых клеток желудка. В итоге, снижается как базальная, ночная, так и стимулированная пищей скорость секреции желудочного сока и соляной кислоты. Возрастает продукция слизи и бикарбонатов. Эффект развивается через 30 мин и сохраняется в течение 3 ч. Вызывает сокращение гладкой мускулатуры кишечника и миометрия. ФК: Относительно стабильный аналог PgE1. Период полуэлиминации составляет 20-40 мин. Показания: Профилактика и лечение эрозивно-язвенных поражений слизистой оболочки ЖКТ, вызванных приемом НПВС. Принимают внутрь по 200 мкг 2-4 раза в день во время или сразу после еды и перед сном. НЭ: боли в животе, тошнота, рвота, диарея; нарушения менструального цикла, альгодисменорея. ФВ: таблетки по 0,0002 |
ПРОТИВОПОДАГРИЧЕСКИЕ СРЕДСТВА
Подагру с Пауком сам ад на свет родил:
Слух этот Лафонтен по свету распустил.
Не стану я за ним вывешивать и мерить,
Насколько правды тут, и как, и почему;
Притом же, кажется, ему,
Зажмурясь, в баснях можно верить.
И, стало, нет сомненья в том,
Что адом рождены Подагра с Пауком.
И.А. Крылов «Подагра и Паук».
Противоподагрическими называют лекарственные средства, которые применяют для купирования приступов подагры, а также для их предупреждения в межприступный период.
Подагра – наследственное метаболическое заболевание, связанное с нарушением пуринового обмена, накоплением мочевой кислоты в организме и проявляющеся повторными приступами артрита, вследствие отложения уратов в суставах и хрящах. Иногда подагра не носит наследственного характера и может быть связана с периодом интенсивного распада нуклеиновых кислот в организме (например, при распаде опухоли вследствие цитостатической терапии или радиотерапии).
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 488; Нарушение авторских прав?; Мы поможем в написании вашей работы!